Comment le DMSO soigne le cerveau et transforme la neurologie
- Obtenir le lien
- X
- Autres applications
Veuillez penser à copier ce texte
Ce texte n'a pas pu être mis en forme : il est "gelé" sur mon écran
https://www.midwesterndoctor.com/p/how-dmso-heals-the-brain-and-transforms?
Les nombreuses preuves concernant la capacité du DMSO à traiter les maladies neurologiques « incurables » — et comment l'utiliser
Rsumé de l'article :
Le DMSO est un « remède parapluie » capable de traiter un large éventail d'affections difficiles grâce à sa combinaison de propriétés thérapeutiques (par exemple, l'amélioration de la circulation, la réduction de l'inflammation, la protection des cellules contre une myriade de facteurs de stress autrement mortels et la réanimation des cellules mourantes).
Ces propriétés rendent le DMSO particulièrement adapté au traitement des troubles neurologiques « incurables » et, associées à des recherches oubliées sur les effets des troubles microcirculatoires, elles redéfinissent notre compréhension des causes des maladies neurologiques (et psychiatriques).
Le DMSO s'est révélé remarquablement prometteur pour traiter les troubles cognitifs, le brouillard cérébral et les pertes de mémoire dus à un large éventail de causes (par exemple, le vieillissement, les maladies vasculaires, l'anesthésie, les séquelles de la COVID ou une intoxication médicamenteuse), tout en améliorant la qualité du sommeil et la vivacité des rêves, souvent en résolvant la douleur, les difficultés respiratoires ou les affections neurologiques (par exemple, le syndrome des jambes sans repos) qui empêchaient un sommeil réparateur.
De nombreuses données soutiennent l'utilisation du DMSO pour les principales maladies neurodégénératives — notamment la maladie de Parkinson, la maladie d'Alzheimer, la SLA, la maladie de Huntington et la sclérose en plaques — et les maladies de mauvais repliement des protéines telles que les maladies à prions et la maladie de Niemann-Pick, où la capacité du DMSO à agir comme un chaperon chimique (stabilisant les protéines et dissolvant les agrégats toxiques) et à augmenter le drainage crânien est particulièrement pertinente.
De nombreuses affections psychiatriques (par exemple, la schizophrénie, la dépression, l'anxiété et le syndrome de stress post-traumatique) ont répondu au DMSO, de même que les crises d'épilepsie, les troubles du mouvement, l'encéphalite, la myasthénie grave et l'hydrocéphalie.
Le DMSO a également produit des améliorations remarquables du développement chez les enfants atteints du syndrome de Down dans de multiples études cliniques, ainsi que dans de nombreux autres troubles neurodéveloppementaux.
Cet article résumera les nombreuses données démontrant l'efficacité du DMSO pour les maladies neurologiques du SNC (environ 2000 études et 200 témoignages pertinents de lecteurs), partagera les découvertes pertinentes (non liées au DMSO) que nous avons faites au sujet des maladies neurologiques au fil des ans, et se conclura par des conseils pratiques sur les protocoles DMSO et les approches complémentaires qui contribuent également au traitement des troubles neurologiques courants.
Le DMSO possède des propriétés thérapeutiques remarquables pour un large éventail de pathologies complexes, et pourtant, il reste largement méconnu. C'est pourquoi j'ai consacré les deux dernières années à compiler des données démontrant que le DMSO traite de nombreuses affections, notamment les problèmes pulmonaires (comme la BPCO et l'asthme), les problèmes cutanés (dont la chute de cheveux), différents types de douleurs , l'arthrite , les lésions tissulaires (comme les entorses ou les brûlures), les problèmes oculaires (comme la perte de vision ou la sécheresse oculaire), les maladies auto-immunes , les problèmes dentaires , les maladies gastro-intestinales , les infections et les cancers (ainsi que la manière dont l'efficacité du DMSO peut être encore améliorée par son association avec des médicaments ou des thérapies naturelles ).
Chacun des articles mentionnés ci-dessus, s'appuyant sur des milliers d'études de recherche oubliées, a présenté des arguments convaincants en faveur de l'essai du DMSO. Collectivement, ils ont reçu des millions de vues, et des milliers de lecteurs ( actuellement plus de 6000 ) m'ont signalé des améliorations concernant un large éventail de pathologies dont ils souffraient, dont beaucoup ont changé leur vie ou correspondent à celles évoquées dans ce reportage de 1980 :
Plus important encore, de la même manière que Mike Wallace a réussi à relancer l'intérêt pour le DMSO en 1980 après que la FDA ait passé deux décennies à l'enterrer en grande partie, cette série a de nouveau suscité un intérêt renouvelé pour l'un des remèdes les plus accessibles et les plus efficaces à notre disposition.
Le DMSO étant particulièrement efficace pour traiter les maladies neurologiques (souvent considérées comme incurables), certains des témoignages les plus marquants que j'ai reçus concernent ce type d'affections. À titre d'exemple, j'ai eu il y a quelques jours une conversation avec le Dr James Miller, un médecin qui, inspiré par les résultats présentés ici, a commencé à l'utiliser chez un grand nombre de ses patients et a fréquemment constaté des résultats étonnants qui l'ont d'abord laissé perplexe.
JM : J’espère que vous allez bien. Je voulais juste prendre de vos nouvelles, car je n’ai pas vu beaucoup de vos publications ces derniers temps.
Moi : Désolée, j'ai disparu. J'ai travaillé d'arrache-pied pour terminer l'article sur la neurologie et le DMSO ; il y a tellement de choses à aborder.
JM : J’ai l’impression, sans données probantes, qu’environ 80 % des symptômes pour lesquels les patients consultent un neurologue disparaissent avec le DMSO. C’est ce que me disent mes patients qui choisissent d’essayer le DMSO pour leurs problèmes neurologiques.
Moi : C'est précisément pour ça que j'ai travaillé si dur sur ce projet.
De même, j'ai récemment reçu un témoignage remarquable d'un patient atteint de SLA (cette terrible maladie terminale pour laquelle nous avons vu des décennies de collectes de fonds pour la recherche) qui montre qu'il peut y avoir un réel espoir pour cette maladie incurable.
Protection cellulaire
Le DMSO est reconnu pour protéger les cellules de nombreux facteurs de stress potentiellement mortels. Par exemple, il prévient les dommages causés par le gel aux cellules, ce qui a rendu possible la cryoconservation moderne (cryomédecine). De nombreuses études montrent que cet effet protecteur s'applique à presque tous les types de tissus (et permet notamment de sauver à plusieurs reprises des doigts humains et des oreilles ou des membres d'animaux 1,2,3 des gelures ). Les cellules du système nerveux étant particulièrement sensibles aux lésions (et souvent incapables de cicatriser), les propriétés protectrices du DMSO leur sont particulièrement utiles. Les principaux mécanismes de protection sont les suivants :
• Réduction du stress oxydatif 1,2,3,4 et neutralisation des radicaux libres nocifs 1,2,3 par exemple, ceux induits par les radiations, comme les radicaux hydroxyles) par piégeage des ions chargés (par exemple, H + et formation de radicaux DMSO protecteurs (ainsi que diminution de la formation de lipofuscine dans les cellules gliales humaines, réduisant les dommages oxydatifs cumulatifs responsables du vieillissement cellulaire). Dans les tranches d'hippocampe, le DMSO a également neutralisé ce stress oxydatif 1,2 ,et dans les neurones granulaires du cervelet, il a prévenu l'apoptose et la mort cellulaire induites par le stress oxydatif en réduisant l'altération mitochondriale précoce et la fragmentation de l'ADN 1,2 (des effets bénéfiques similaires ont été observés lorsque le DMSO était associé à des inhibiteurs de CDK et de G9a 1,2 ). Des traces de DMSO protègent également les plantes des dommages causés par l'ozone et neutralisent l'acide hypochloreux réactif, le superoxyde et le peroxyde d'hydrogène (tout en agissant simultanément en synergie avec les thérapies oxydatives et sans altérer la viabilité des neutrophiles ).
Le DMSO augmente la production d'ATP dans les cellules et facilite sa production lorsque la production d'énergie est compromise (par exemple, de très faibles concentrations de DMSO, de l' ordre de 0,000025 à 0,25 %, ont démontré qu'elles augmentent le métabolisme cellulaire, notamment en orientant les métabolites de la glycolyse vers le cycle de Krebs mitochondrial ou en permettant à une partie des mitochondries de synthétiser de l'ATP en l'absence du reste de la mitochondrie 1,2,3,4,5 . Le DMSO a également prévenu l'inactivation de l'aconitase mitochondriale induite par les radicaux hydroxyles , la dépletion d' ATP et les lésions neuronales. De plus, le DMSO a augmenté le métabolisme du pyruvate et du glucose dans des tranches de cerveau , a protégé les souris d'une asphyxie à l'azote autrement mortelle et, dans une étude où des souris ont été décapitées, le DMSO a prolongé la durée de leur respiration et, par conséquent, la durée de leur activité cérébrale.
Remarque
: de nombreuses études sur les animaux sont extrêmement cruelles et je
ne les soutiens pas ; cependant, puisqu'elles ont été réalisées, j'ai
estimé qu'il était important de partager les connaissances fournies par
certaines études sur le DMSO afin qu'il ne soit pas nécessaire de les
répéter pour obtenir ces données.
• Protéger les cellules de la mort une fois l'apport sanguin interrompu (une des principales raisons pour lesquelles tant de lecteurs ont pu éviter un handicap permanent suite à un AVC ), notamment en empêchant l'afflux rapide d'ions calcium ou sodium qui déclenche fréquemment l'apoptose (mort cellulaire), et en réduisant l'activité des protéines caspases (qui déclenchent la mort cellulaire) dans les cellules épithéliales du foie, du cœur et des voies respiratoires.
Remarque : ⬖ désigne les substances naturelles utilisées en conjonction avec le DMSO.
Ces propriétés permettent donc au DMSO de :
• Protéger les neurones dans l’ ensemble du cerveau ( par exemple, dans l’hippocampe) contre un large éventail d’excitotoxines, reconnues comme une cause fréquente de neurodégénérescence 1,2,3,4,5,6,7,8,9,10 </( par exemple, dans une étude, le DMSO a restauré 66,7 à 76,1 % de l’activité électrique normale après une intoxication au glutamate), et renforcer les effets protecteurs d’ autres agents protecteurs ( par exemple , le syringarésinol , les isoquinoléinesulfonamides , la curcumine et le ginkgo biloba ) <sup> 1,2,3,4,5,6 </sup> .
Remarque : le DMSO est couramment associé à d'autres agents neuroprotecteurs tels que la curcumine ⬖ , la mélatonine ⬖ , la baicaline ⬖ , la butéine ⬖ , l'icariine ⬖ , la naringine ⬖ , le 4-PBA ⬖ et le BPV(phen) , divers médicaments chinois , des composés nitroniques et des dérivés de capsaïcine ⬖ (c'est-à-dire que dans les études qui viennent d'être énumérées, ces combinaisons ont réduit la neuroinflammation, le stress oxydatif, le stress du RE et l'apoptose tout en améliorant la fonction mitochondriale et l'autophagie dans les cellules neuronales).
Chez des rats intoxiqués au monoxyde de carbone, le glibenclamide a réduit les altérations neuronales cérébrales et le taux de dégénérescence, ainsi que le score total de lésions cardiaques (et les lésions hépatiques en association avec le pyruvate d'éthyle). 1,2 Il a également amélioré les scores de déficit neurologique, réduit la dégradation des cellules neuronales (NSE et S-100β) et diminué les taux de TNF-α et d'IL-8, deux cytokines inflammatoires. Enfin, les propriétés antioxydantes du DMSO pourraient conférer un rôle neuroprotecteur potentiel en cas d'intoxication au monoxyde de carbone. 1,2
•Protéger les cellules normales contre les chimiothérapies telles que la prévention des lésions cérébrales, du stress oxydatif, de l'inflammation et de la mort neuronale dues au cyclophosphamide (en association avec Scenedesmus obliquus ⬖ ), au cisplatine (seul ou en association avec DMFM) 1 , 2 , 3 et à la doxorubicine ( où, en association avec la curcumine ⬖, elle a empêché le « chimiocerveau »).
•Prévenir les dommages et la mort des cellules neuronales causés par divers métaux tels que le plomb (seul ou en association avec la thymoquinone ⬖ ) 1 , 2 , 3, l'aluminium (seul ou en association avec le GSK-3β, le 3MA ou le dantrolène) 1 , 2 , 3 , 4 , le cadmium , le mercure (en association avec la mélatonine ⬖ ou la curcumine ⬖ ) 1 , 2, la forme toxique du manganèse (seul ou en association avec le NAC ou le PAS-Na ou un inhibiteur de FTO) 1 , 2 , 3 , 4, des doses toxiques de lithium ( en association avec la curcumine ⬖ ), ainsi que l'arsenic ( en association avec le 3-MA ), les nanoparticules de zinc ( en association avec la quercétine ⬖ ), le chlorure de cobalt (en association avec la curcumine ⬖ ) et le fluorure ( en association avec le M3OMG ), et le thioacétamide .
Remarque
: les effets neuroprotecteurs du DMSO dans ces études incluaient des
réductions du stress oxydatif, de la mort des cellules neuronales, de la
dysrégulation du calcium, de la libération de calcium intracellulaire,
des malformations congénitales et des lésions histopathologiques du
cerveau.
• Protéger les animaux des organophosphorés, y compris des doses normalement létales de gaz neurotoxiques <sup> 1,2,3,4,5,6 </sup> ( ou pour renforcer l’efficacité des antidotes et réduire les lésions cérébrales <sup> 1,2,3 </sup> ) , et traiter les morsures de serpent et l’œdème cérébral associé chez l’homme, le chat, le cheval et le chien<sup>1,2,3,4,5,6</sup>. De même , chez deux chevaux victimes d’ un essaim d’ abeilles africaines , l’administration intraveineuse de DMSO , dans le cadre d’un protocole combiné , a permis de faire régresser les graves troubles neurologiques induits par le venin d’abeille en cinq heures.
Chez la souris et le rat, le stress oxydatif et la neurotoxicité (par exemple, dans l'hippocampe) induits par divers agents ont été neutralisés par le DMSO en association avec un autre agent thérapeutique : éthanol (nimodipine, DAPT ou MSM), 1 , 2 , 3 méthamphétamine ( curcumine ⬖ ) aflatoxine de moisissure (en association avec des extraits de Chelidonium majus ⬖ ou d'artichauts ⬖ ), 1 , 2 intoxication au gaz de pétrole liquéfié (un inhibiteur de la p38MAPK ), phtalate de diéthyle et bisphénol S ( acide vanillique ⬖ ), thrombine ( œstrogène ), triméthylétain ( carvacrol ⬖ ), tunicamycine ( 4-PBA ), chlorpyrifos ( hespéridine niosomale ⬖ ou taxifoline ⬖ ), calyculine A ( mélatonine ⬖ ) fipronil ( chlorhydrate de malvidine). ⬖ ), la thapsigargine ( Activine A ). De même, la mélatonine ⬖ a atténué la neurotoxicité du PBDE-47 (retardateur de flamme) dans les cellules PC12.
Remarque : l’ivermectine à forte dose provoque une neurotoxicité, ce qui limite son utilisation à des doses élevées. Dans un cas rapporté ,
l’administration intraveineuse de DMSO a permis une récupération
neurologique complète chez un chien comateux ayant ingéré une dose
toxique de pâte d’ivermectine.
De même, le DMSO protège également les cellules contre divers facteurs de stress non chimiques nocifs en :
• Protection des cellules (y compris à titre prophylactique) contre les dommages causés par l'exposition à des rayonnements (souvent mortels). 1 , 2 , 3 , 4 , 5 Par exemple, le DMSO a prévenu les dommages à l'ADN induits par les rayons X et gamma dans les cellules d'ovaires de hamster, les drosophiles et les organoïdes cérébraux (par exemple, en accélérant la réparation de l'ADN), 1 , 2 , 3 , 4 et a empêché les signaux nocifs (effets de voisinage) émis par les cellules irradiées dans leur environnement d'endommager les cellules non irradiées, tout en protégeant certaines bactéries de l'exposition aux rayons X. 1 , 2 , 3 De même, il a été démontré à plusieurs reprises que le DMSO réduisait les dommages chromosomiques causés par les rayonnements 1 , 2 et empêchait la création de radicaux libres nocifs par les rayonnements . Ainsi, il a été démontré que le DMSO protège les animaux (par exemple, les souris, les lapins, les chiens et les singes) contre des doses de rayonnement souvent mortelles et prévient les dommages tissulaires causés par les rayonnements (par exemple, à la moelle osseuse, à la muqueuse intestinale, aux cellules souches, aux yeux ou à la peau), 1 , 2 , 3 , 4 , 5 , 6 , 7 et, du fait qu'il prévient les dommages causés par les rayonnements dans les cellules non cancéreuses, le DMSO a été largement utilisé comme traitement complémentaire du cancer .
Remarque : le DMSO a été combiné avec de nombreuses autres substances pour protéger les animaux des dommages causés par les radiations, comme l'astragaloside-IV ⬖ (prévenant la sénescence neuronale), la rapamycine (prévenant à plusieurs reprises les malformations induites par les rayons X du développement cortical chez la progéniture du rat) 1 , 2 la thymoquinone ⬖ ( réduisant le peroxynitrite cérébral ) ou un inhibiteur de la glycogène synthase kinase-3β (prévenant la nécrose du tissu cérébral).
• Préserver la fonction des fibres nerveuses exposées aux rayonnements UV.
• Traitement d’une grande variété de brûlures (détaillées ici ) et protection du cerveau contre les dommages causés par la chaleur (ainsi que contre les lésions dues au froid mentionnées précédemment).
• Protection des cellules contre le stress osmotique et la déshydratation (et, en association avec la nimodipine , protection des cellules neurales contre le choc osmotique tout en induisant la croissance des neurites).
• Protéger les cellules gliales de la destruction par perturbation sonique via un vibrateur ultrasonique (78 % contre 13 % de survie), et en conjonction avec un antagoniste TRPV4 , protéger les neurones hippocampiques et la microglie de l'apoptose induite par les infrasons (16 Hz/130 dB).
• Prévenir l’augmentation spectaculaire de la mort des cellules germinales, le raccourcissement de la durée de vie et le stress oxydatif causés par de forts champs magnétiques statiques et prévenir de même les dommages similaires dus à une exposition continue aux ions atmosphériques générés électriquement.
• En association avec la curcumine , ⬖ protège le cerveau, les reins et le foie du fœtus des dommages causés par l’exposition aux champs électromagnétiques (CEM) de basse fréquence pendant la grossesse.
Sécurité du DMSO
Chaque substance possède une dose efficace (la quantité produisant un effet thérapeutique) et une dose toxique (la quantité provoquant un effet nocif). L'équilibre entre ces deux doses détermine souvent l'efficacité d'un traitement (par exemple, le mercure traitait partiellement la syphilis, mais pendant des siècles, il a causé bien plus de mal que de bien en raison de sa forte neurotoxicité ; de même, certaines thérapies modernes, comme la chimiothérapie, bien que souvent efficaces, entraînent de nombreux problèmes car leurs doses toxiques sont très proches des doses thérapeutiques couramment prescrites). De plus, il n'existe souvent pas de dose « idéale » universelle ; on choisit donc des doses standardisées qui fonctionnent pour la majorité de la population (ce qui conduit à ce que les patients sensibles, pour lesquels ces doses sont trop élevées, soient systématiquement victimes de préjudices et ensuite victimes de dénigrement de la part du système médical).
C’est pourquoi j’essaie d’utiliser des thérapies présentant une marge thérapeutique très large (c’est-à-dire que la dose efficace est bien inférieure à la dose toxique), mais même dans ces cas-là, il m’arrive encore de rencontrer des patients qui réagissent à ces doses « sûres » et qui ont besoin de doses beaucoup plus faibles.
Dans le cas du DMSO, ce qui m'a frappé, c'est l'étendue de sa marge thérapeutique (démontrée par sa DL50 extrêmement élevée, pratiquement non toxique, et par le fait qu'au lieu d'endommager les cellules, il les protège d'un large éventail de facteurs de stress autrement mortels). Compte tenu de cela et de la rapidité avec laquelle le DMSO se distribue et se dilue dans l'organisme, en dehors des expériences animales où de fortes doses de DMSO sont injectées , il est extrêmement improbable que le DMSO atteigne une dose toxique (ainsi, même lors d'une étude de sécurité chez l'humain où des doses extrêmes ont été utilisées pendant une période prolongée, aucun problème n'a été constaté).
Cela dit, avec du DMSO (pur), les problèmes suivants existent :
L'utilisation excessive de DMSO provoque fréquemment des démangeaisons et des irritations cutanées temporaires. On peut éviter ces désagréments en utilisant des concentrations topiques plus faibles ou un agent naturel qui prévient l'irritation causée par le DMSO ; toutefois, ces problèmes surviennent encore régulièrement en raison d'un usage excessif.
Chez certaines personnes, le DMSO créera une odeur désagréable (qui peut souvent être traitée par l'une des méthodes détaillées ici ).
Un petit nombre de personnes (environ 1 sur 2 000) sont allergiques au DMSO. C’est pourquoi il est conseillé d’utiliser le DMSO par voie topique dans un premier temps, de vérifier s’il s’agit d’une réaction allergique (et non d’une simple irritation cutanée) et, le cas échéant, de réduire la fréquence d’utilisation et d’éviter absolument toute application systémique (par exemple, par voie orale).
Le DMSO peut introduire des substances toxiques dans l'organisme. À ses débuts, on a rapporté de rares cas de personnes tombées malades pendant quelques jours après un contact cutané avec du DMSO et des pesticides (désormais interdits), ainsi qu'un cas de surdosage de nicotine . C'est pourquoi il est généralement conseillé de toujours se laver la peau à l'eau après application de DMSO (une fois sec). De nos jours, je n'ai pas eu connaissance de cas similaires.
Le DMSO transporte efficacement les allergènes à travers la peau (ce qui explique son utilisation ponctuelle pour les tests épicutanés). Comme certaines personnes sont allergiques à des substances naturelles apparemment inoffensives, cela peut parfois entraîner des problèmes (par exemple, dans le seul cas rapporté que j'ai reçu, une crise d'urticaire est apparue après l'utilisation d'une préparation à base d'arnica et de DMSO – car un nombre surprenant de personnes sont allergiques à l'arnica).
Tous les anticoagulants comportent un risque d'hémorragie excessive. Le DMSO utilisant un mode d'action différent, ce risque est bien moindre, mais il demeure possible (par exemple, trois lecteurs ont signalé une augmentation apparente de leurs saignements de nez, et j'ai trouvé un cas de réaction grave dans un rapport de cas ).
L'une des principales applications du DMSO est sa capacité à potentialiser l'effet de certains médicaments, mais cela signifie également qu'il peut accroître leur toxicité (même si, comme indiqué précédemment, le DMSO a souvent un effet antagoniste). Ce phénomène a principalement été observé avec l'alcool, les barbituriques et, dans une moindre mesure, les benzodiazépines (par exemple, une étude menée sur des chats a révélé que l'ajout de diazépam à du DMSO administré par voie intraveineuse, pourtant inoffensif, provoquait une hypotension fatale et une fibrillation ventriculaire). Des études récentes font également état d'une augmentation de la fréquence des effets secondaires de médicaments plus toxiques (par exemple, la chimiothérapie et les fluoroquinolones). Une question importante demeure : ce risque existe-t-il également avec les anticoagulants ? Si les données limitées et l'absence de signalements d'effets indésirables semblent indiquer le contraire, nous recommandons systématiquement aux patients de surveiller attentivement leur coagulation sanguine (ce qui est généralement le cas lors de traitements anticoagulants). Pour toutes ces raisons, il est généralement conseillé de prendre du DMSO au moins deux heures après la prise de médicaments afin de minimiser le risque de potentialisation indésirable.
Remarque : les problèmes liés au DMSO et à l'alcool sont abordés plus en détail ici .
Chez les patients sensibles, des réactions transitoires au DMSO (par exemple, des maux de tête) peuvent survenir en cas de surdosage. J'ai également reçu deux signalements de patients extrêmement sensibles (en raison d'une accumulation de toxines de longue date) dont l'état s'est aggravé après la prise de DMSO, ce dernier ayant mobilisé des toxines stockées.
Après plusieurs semaines d'inhalation de fortes doses de DMSO, il a été constaté qu'elles étaient nocives pour les lapins . C'est pourquoi les chercheurs travaillant sur le DMSO ( à l'exception d'une étude concluante sur le SDRA ) ont évité d'étudier le DMSO nébulisé. Cependant, les utilisateurs modernes de DMSO ont logiquement commencé à l'administrer par nébulisation et ont constaté des bénéfices significatifs (par exemple, des résultats remarquables dans le traitement de la BPCO ). Les chercheurs qui ont étudié cette technique ont conclu à un risque théorique (jamais observé) de neutralisation du surfactant par le DMSO nébulisé, pouvant entraîner un collapsus pulmonaire. Ils ont donc mis en garde contre les doses élevées (qui peuvent également libérer des particules de plastique de la plupart des nébuliseurs). À ce jour, un seul patient (un collègue) a présenté ce risque (ce patient, de par sa morphologie, était déjà à haut risque de pneumothorax). Hormis ce cas, de nombreuses personnes ont nébulisé avec succès du DMSO à des doses bien supérieures à celles que nous utilisons habituellement, sans aucun problème.
Des inquiétudes similaires existaient également concernant la grossesse, car l'injection de fortes doses de DMSO dans ou à proximité du fœtus a été associée à des troubles du développement. Cependant, très peu de recherches ont été menées dans ce domaine (bien que ces doses soient impossibles à atteindre avec les usages habituels du DMSO). Heureusement, de nombreuses femmes enceintes et allaitantes ont utilisé le DMSO sans problème.
Remarque : un prochain article compilera toutes les recherches réalisées. À l'heure actuelle, l'étude la plus probante (mais non définitive) démontrant l'innocuité du DMSO chez les femmes enceintes est celle-ci .Lorsque les cellules sont exposées à de fortes concentrations de DMSO pendant des périodes prolongées (inatteignables dans l'organisme), des lésions cellulaires et microcellulaires se produisent. Il est à noter que les seuils de toxicité du DMSO pour les cellules cancéreuses sont bien inférieurs à ceux des cellules normales, ce qui explique probablement en partie pourquoi le DMSO est un excellent outil dans le traitement du cancer .
Compte tenu de ce qui précède, pratiquement toutes les études que j'ai lues utilisant le DMSO n'ont pas rapporté d'effets indésirables liés à cette substance. Les effets indésirables graves du DMSO sont extrêmement rares et, dans la quasi-totalité des cas, ils résultaient de l'administration de DMSO par voie intraveineuse en association avec un agent d'embolisation ou des cellules souches (alors que les effets indésirables, beaucoup plus rares, liés à l'administration de DMSO par voie intraveineuse seul disparaissaient généralement après l'arrêt de la perfusion 1,2 ). Certains de ces cas étant assez préoccupants et ne correspondant pas à ce que nous avions observé jusqu'alors avec le DMSO par voie intraveineuse ( comme dans cette étude de sécurité exhaustive menée chez le singe ou ce que j'avais pu constater chez de nombreux praticiens utilisant le DMSO par voie intraveineuse), j'ai approfondi la question et en ai conclu :
Les
agents emboliques liquides présentent une toxicité propre et peuvent
parfois migrer et obstruer accidentellement d'autres parties du système
circulatoire (de nombreux rapports semblent l'indiquer, et les
étiquettes d'avertissement des produits le mentionnent également).
De
nombreux patients recevant des cellules souches DMSO par voie
intraveineuse sont des patients cancéreux extrêmement fragiles (ayant
subi une chimiothérapie à haute dose) et sont donc plus susceptibles de
réagir aux traitements, en particulier aux doses élevées. De même, une étude a montré que
si les chiens ne présentaient généralement pas de problèmes avec le
DMSO, ceux atteints d'insuffisance rénale chronique en présentaient
suite à des doses intraveineuses élevées.
• En raison de l'innocuité du DMSO, des doses intraveineuses très élevées sont utilisées. Celles-ci suffisent souvent à créer un choc osmotique qui rompt les membranes les plus fragiles (par exemple, l'hémolyse est une complication fréquente des doses intraveineuses élevées de DMSO, et dans cette étude sur les chevaux , elle a été observée parallèlement à des symptômes importants, mais temporaires, lorsque 40 % de DMSO, soit dix fois la dose normale, ont été rapidement perfusés à des chevaux).
Les concentrations utilisées lors des précédentes applications sont suffisantes pour entraîner la lixiviation des phtalates présents dans les tubulures de perfusion. Or, les phtalates peuvent provoquer des arythmies cardiaques. Un médecin utilisant du DMSO a constaté ce problème lors d'injections intraveineuses de DMSO, jusqu'à ce qu'il utilise une autre tubulure.
•Comme le DMSO augmente l’activité parasympathique par inhibition de la cholinestérase, il peut ralentir le rythme cardiaque, en particulier si une grande quantité atteint soudainement le cœur. Ainsi, bien qu’il ne modifie généralement pas le rythme cardiaque et qu’il ait été observé qu’il normalise la réactivité du système nerveux autonome , à fortes doses, il peut être arythmique (par exemple, une concentration de DMSO de 1 à 3 % a légèrement augmenté le rythme cardiaque, 1 , 2 tandis qu’une concentration de 6 à 10 % l’a considérablement diminué, mais cet effet a pu être inversé par l’atropine 1 , 2 ).
•Bien que les praticiens (ces derniers jours et dans toute la littérature sur le DMSO) utilisant des doses de DMSO IV beaucoup plus élevées que les nôtres ne semblent pas avoir rencontré de problèmes, une grande prudence dans l'identification du dosage approprié de DMSO IV est probablement justifiée.
Enfin, grâce à son innocuité largement reconnue, sa toxicité négligeable et sa capacité à transporter rapidement des substances dans tout l'organisme, le DMSO est souvent utilisé comme ingrédient « inerte » pour administrer d'autres médicaments et comme solvant ou véhicule pour faciliter l'évaluation des effets biologiques d'un grand nombre de substances (car, sans dissolution ni transport, il est souvent impossible de les tester).
Remarque : outre
l'évaluation
des effets thérapeutiques, le DMSO est également utilisé pour
administrer un agent nocif afin de déclencher une maladie <sup> 1,2,3,4,5,6,7,8,9,10,11,12 </sup> ( ce qui rend très fastidieux le tri des études sur le DMSO pertinentes sur le plan thérapeutique ) ou pour évaluer le mécanisme d' action d' une thérapie en vérifiant si l' inhibiteur spécifique administré par le DMSO bloque l'efficacité de la thérapie (par exemple, de nombreuses études de ce type existent sur l' acupuncture chinoise <sup> 1,2,3,4,5,6,7 </sup> ) .
Étant donné que des bénéfices similaires sont observés avec de nombreuses thérapies différentes combinées au DMSO (que le DMSO seul provoquerait), j'en ai conclu :
• La toxicité de nombreuses toxines a été sous-estimée en raison des effets protecteurs du DMSO qui les contrecarrent (un fait également reconnu par quelques chercheurs en neurologie).
•L'une des principales raisons pour lesquelles les bénéfices observés dans les études précliniques n'apparaissent pas dans les études cliniques (un problème extrêmement courant dans la recherche scientifique) est que le DMSO n'est plus utilisé — d'autant plus que je trouve parfois des études où le DMSO seul, plutôt que d'être simplement le témoin, est également testé par rapport à une solution saline, et dans un nombre significatif de ces études, le DMSO seul a eu un effet thérapeutique.
Enfin, en rédigeant cet article, j'ai tenté de condenser des milliers d'études pertinentes en un document accessible à tous, tout en veillant à ce que cette littérature, souvent méconnue, reste accessible aux chercheurs et auteurs souhaitant approfondir ces travaux. C'est pourquoi j'ai choisi d'inclure les études de combinaison, car elles illustrent les bénéfices communs du DMSO associé à ces agents pour un large éventail de pathologies neurologiques, et parce que la combinaison peut souvent renforcer l'efficacité du DMSO (détaillée ici ), offrant ainsi des pistes supplémentaires aux personnes souffrant des maladies neurodégénératives abordées ici. Par conséquent, chaque fois qu'un agent à effet thérapeutique est mentionné dans cet article, considérez qu'il a été combiné au DMSO . De plus, si cet agent était une thérapie naturelle (par exemple, une plante, un nutraceutique ou un extrait botanique), comme indiqué précédemment, je l'ai signalé par un ⬖ .
Causes de la maladie
Pour comprendre une maladie, deux approches différentes permettent de l'interpréter. La première, réductionniste (souvent privilégiée), consiste à la décomposer en ses plus petits éléments afin de la comprendre. La seconde, holistique, considère la maladie comme un rouage d'un système beaucoup plus vaste et cherche à identifier le processus systémique à l'origine des problèmes rencontrés.
Depuis l'œuvre fondatrice de Descartes sur le raisonnement en 1637 (il y a environ 400 ans), notre culture a adopté le modèle réductionniste et, grâce à lui, a créé d'innombrables innovations scientifiques qui ont transformé la société, telles que de nombreuses innovations médicales qui ont identifié la cause précise d'une maladie potentiellement mortelle et ont fourni un remède pour qu'elle ne soit plus fatale.
Malheureusement, si les approches réductionnistes sont souvent excellentes pour les maladies aiguës mettant la vie en danger, elles n'identifient souvent que les effets concrets de la maladie plutôt que le processus en amont qui l'a engendrée (ce qui explique que les thérapies choisies soient généralement symptomatiques plutôt que curatives). C'est pourquoi la médecine moderne est souvent qualifiée d'« excellente pour les urgences, mais catastrophique pour les maladies chroniques ». De même, une plaisanterie récurrente en neurologie veut que les neurologues soient excellents pour diagnostiquer les maladies neurologiques, mais peu compétents pour les traiter (même si des progrès thérapeutiques ont été récemment réalisés).
Remarque : on peut aussi avancer que notre médecine axée sur la biochimie (qui tente d’identifier une cible moléculaire spécifique pour chaque maladie) existe parce qu’elle permet de développer un nombre quasi infini de thérapies brevetables pour chaque maladie, alors que si l’on utilisait des remèdes systémiques capables de traiter une myriade de maladies (par exemple, des thérapies globales ou basées sur la biophysique ), il ne serait plus possible d’avoir un modèle commercial lucratif qui brevette chaque maladie.
À l'inverse, je considère de nombreuses maladies comme la manifestation d'un processus pathologique sous-jacent au sein de l'organisme et, dans de nombreux cas, je crois que la maladie spécifique qui se déclare est en grande partie le produit de l'endroit où ce processus pathologique s'est installé dans le corps de l'individu (par exemple, il était très fréquent que les effets indésirables du vaccin contre la COVID-19 affectent une zone du corps déjà affaiblie ou blessée, ce qui explique en partie la grande variété de symptômes observés).
Malheureusement, bien que cette perspective soit souvent nécessaire pour soigner une maladie, elle est diamétralement opposée non seulement à la façon dont notre société nous apprend à penser, mais aussi à l'ego humain, car les cadres réductionnistes offrent l'illusion réconfortante de la certitude et du contrôle, tandis que les perspectives holistiques nous obligent à tolérer l'ambiguïté et l'imprévisibilité afin de pouvoir voir au-delà des parties et saisir l'ensemble plus vaste — et malheureusement, l'ego humain fera tout son possible pour avoir l'impression d'être aux commandes.
La séquence des maladies
Au fil des années, j'ai constaté un schéma récurrent qui caractérise bon nombre des maladies que je rencontre :
Un élément perturbateur survient, ou un problème récurrent finit par affecter l'organisme à un point qui dépasse sa capacité de compensation.
L'organisme (ou une partie de celui-ci) entre dans un état de choc et s'arrête partiellement ou totalement.
La capacité naturelle de guérison du corps est incapable de résoudre ce blocage , et le problème devient chronique.
Cet arrêt provoque le dérèglement d'autres fonctions corporelles qui y sont liées et engendre des problèmes supplémentaires.
C’est pourquoi mon approche consiste souvent à :
Il faut d'abord identifier le problème réel et le problème sous-jacent qui l'a déclenché.
Ensuite, traitez le problème sous-jacent qui a causé le dysfonctionnement.
Vérifiez si cela résout le problème, et sinon, proposez une thérapie régénératrice qui réactive le tissu (j'en ai longuement parlé dans la série sur la réponse cellulaire au danger ).
Pour tout problème persistant, traitez la cause sous-jacente qui a prédisposé cette zone à être affectée par le processus systémique.
Identifiez les problèmes persistants dans les autres parties du corps liées au problème principal et traitez-les.
Remarque : dans d'autres cas, la situation est beaucoup plus simple et je me concentre simplement sur une thérapie adaptée au problème réel.
Grâce à ce cadre de réflexion, j'ai beaucoup réfléchi aux éléments qui provoquent les chocs qui paralysent initialement le système (par exemple, une infection, un stress prolongé, un mauvais sommeil, une blessure importante ou une compression des tissus) et j'ai essayé de comprendre pourquoi le corps de certaines personnes peut rapidement se débarrasser de ces agressions et des dommages qu'elles engendrent, tandis que chez d'autres, elles s'incrustent et deviennent rapidement permanentes.
De là, j'en suis progressivement venue à la conclusion que la circulation sanguine est essentielle et que, lorsqu'elle est perturbée, certaines parties du corps sont non seulement « choquées », mais le corps perd également sa capacité intrinsèque à retrouver un état de santé optimal après les chocs subis. Ainsi, je considère de nombreuses maladies et processus pathologiques (comme l'inflammation) non pas comme des entités indépendantes, mais plutôt comme des conséquences d'une mauvaise circulation (et je reconnais également que la raison sous-jacente pour laquelle de nombreux processus pathologiques différents présentent des symptômes similaires est qu'ils altèrent tous la circulation).
Remarque :
dans de nombreuses écoles de médecine naturelle, les carences
nutritionnelles sont identifiées comme une cause profonde de la maladie
et doivent être traitées par une supplémentation adéquate. Ma propre
expérience (confirmée par certaines études) a montré que ces maladies
guérissent souvent lorsque la circulation est rétablie dans la zone
affectée. Autrement dit, si l'augmentation des concentrations de
nutriments dans le sang irriguant la zone touchée peut résoudre le
problème, ces nutriments peuvent également être apportés en quantité
suffisante en augmentant le volume de sang irriguant cette zone.
Mon intérêt pour la circulation s'explique en partie par la fréquence à laquelle je constate ses effets spectaculaires et rapides chez les patients, en partie par la fréquence à laquelle j'identifie désormais des obstructions circulatoires pertinentes, et parce que les pionniers de cette approche ont proposé l'un des modèles de maladie les plus éclairants que j'aie rencontrés. En bref :
S’appuyant
sur les travaux antérieurs, Melvin Knisely a démontré, entre les années
1940 et 1960, que l’« agglutination sanguine » (agrégation des globules
rouges) était à l’origine de nombreuses maladies, notamment celles
nécessitant une hospitalisation. Ce phénomène réduisait généralement le
débit sanguin et interrompait la microcirculation dans les vaisseaux
trop volumineux pour permettre le passage des globules rouges
agglutinés. Parmi ses découvertes majeures, on peut citer les brûlures,
les infections sanguines comme le paludisme et le cancer, qui provoquent
une importante agglutination sanguine (affectant ensuite l’organisme de
manière systémique) ; quelques traitements (par exemple, le dextran de
faible poids moléculaire et l’hydroxychloroquine) permettant d’atténuer
cette agglutination ; et, grâce à l’observation des vaisseaux de l’œil
au microscope, il est devenu possible d’évaluer de manière non invasive
le degré d’agglutination du sang dans tout l’organisme. (Alors que, si
l’on pouvait évaluer l’agglutination dans le sang prélevé par analyse
des globules rouges vivants ou par la mesure de la vitesse de
sédimentation, cette méthode était moins précise car le comportement
d’agglutination du sang était modifié une fois hors du corps.)
En
médecine chinoise, de nombreux « schémas pathologiques » permettent
d'expliquer l'origine d'une maladie spécifique. L'un d'eux, la « stase
sanguine » (sur laquelle je dois encore écrire un article), correspond
parfaitement à la formation de boues sanguines. Fait intéressant, après la vaccination massive contre la variole , la stase sanguine a été de plus en plus considérée comme la cause principale de la plupart des maladies .
Notamment, la médecine chinoise a développé de nombreux signes
diagnostiques pour la stase sanguine, qui s'avèrent très utiles pour
identifier la formation de boues sanguines.
•Bien que Knisely ait pu constater que la formation de boues sanguines était une cause fondamentale de la maladie et que certains éléments la déclenchaient (par exemple, une chaleur ou un froid excessifs), il ne pouvait pas déterminer pourquoi elle se produisait et a émis l'hypothèse qu'elle pouvait être due à un revêtement collant sur les cellules (absent du sang normal) qui a été provisoirement identifié comme une protéine.
Dans les années 1960, Thomas Riddick, ingénieur et chimiste qui travaillait régulièrement avec des solutions colloïdales pour les épaissir ou les fluidifier (par exemple, il faut fluidifier l'argile pour qu'elle s'écoule dans les canalisations, tandis qu'il faut épaissir les eaux usées pour que leurs matières s'agglomèrent et se déposent au fond), a conclu que ses problèmes cardiaques (alors considérés comme « incurables ») pouvaient être dus à un sang « trop épais ». Il a alors essayé d'appliquer sur son corps les mêmes agents qu'il utilisait pour disperser les colloïdes industriels, et cela a fonctionné. Il en a déduit que la principale variable qu'il avait modifiée, le potentiel zêta (la répulsion électrique entre les particules colloïdales qui leur permet de résister aux forces d'agglomération dans un système liquide), pouvait être à l'origine de nombreuses maladies et était le facteur responsable de l'agglomération sanguine observée par Knisely. C’est pourquoi il l’a étudié de manière approfondie (par exemple, avec des microscopes pointés vers les yeux qui filtraient la chaleur de son ampoule incandescente afin que le sang exposé ne commence pas à se liquéfier) et a notamment conclu que l’aluminium était extrêmement dangereux car sa forte charge positive en faisait l’ion le plus capable de perturber le potentiel zêta, que les personnes ayant un faible potentiel zêta étaient exposées à un risque élevé de crise cardiaque et que les infections bactériennes et virales aggraveraient systématiquement le potentiel zêta du corps (ce qui explique qu’elles affectent plus gravement les personnes âgées, car le potentiel zêta se détériore avec l’âge).
•Un médecin souffrant d'une maladie cardiaque incurable a découvert les travaux de Riddick et, après que ceux-ci aient résolu ses problèmes cardiaques, il a constaté que, chez ses patients, la restauration du potentiel zêta avait un effet miraculeux sur quelques autres maladies, dont la démence.
Le neurologue canadien Andrew Moulden a constaté qu'il observait fréquemment des enfants présentant des signes cliniques d'AVC après la vaccination, et que les signes les plus graves étaient corrélés à un handicap développemental consécutif à la vaccination (ce qui fait écho à un siècle de rapports de cas publiés sur des problèmes des nerfs crâniens associés à l'encéphalite vaccinale, et à l'observation ultérieure de ces mêmes déficits chez les enfants autistes). Moulden en a conclu que les vaccins provoquaient des micro-AVC dans tout le corps, en raison d'agents perturbateurs du potentiel zêta présents dans les vaccins (par exemple, l'aluminium) qui agglutinent les cellules sanguines, et parce que, lors d'une réaction inflammatoire, les globules blancs de plus grande taille obstruent la microcirculation (ces phénomènes étant trop petits pour être détectés par imagerie radiologique, ce qui explique en grande partie pourquoi les tests diagnostiques ne permettent pas d'identifier de nombreuses affections neurologiques chroniques). Il a également conclu que les micro-AVC caractéristiques qu'il observait résultaient de leur localisation dans des régions du cerveau moins bien vascularisées, et qu'ils servaient donc d'indicateurs de lésions cérébrales silencieuses se produisant également dans d'autres régions du cerveau affectées par ces micro-AVC. Enfin, comme ses prédécesseurs, il a souligné que d'autres facteurs, tels que les infections, pouvaient en être la cause, mais a insisté sur le fait que ce problème était beaucoup plus fréquent avec la vaccination.
•De nombreux médecins (moi y compris) ont réalisé indépendamment que ce processus affectait probablement tous les fluides du corps, car ce sont tous des colloïdes, et que nombre des affections attribuées à la stagnation du sang (par exemple, la médecine chinoise associe la stase sanguine à l'auto-immunité) résultaient probablement d'obstructions dans d'autres fluides comme le système lymphatique.
En décembre 2019, suite à des témoignages sur des forums anonymes en ligne, j'ai commencé à craindre sérieusement que la COVID-19 (SARS-CoV-2) ne se transforme en catastrophe mondiale (en partie à cause de son évolution, et en partie parce que toutes les autorités minimisaient sa gravité, alors que des pandémies bien plus mineures et relativement insignifiantes étaient généralement exagérées à l'extrême). Dès le début, j'ai donc correspondu avec tous mes contacts soignant la maladie et j'ai rapidement constaté des caractéristiques très étranges, suggérant d'importantes perturbations du potentiel zêta dans tout l'organisme. Comme mes collègues ayant traité le SARS-CoV-1 n'avaient pas observé ces caractéristiques, j'ai émis l'hypothèse de la présence probable d'une protéine à la surface du virus, présentant une densité de charge très élevée, absente chez le SARS-CoV-1. Après avoir appris à effectuer cette analyse, j'ai réalisé que la protéine Spike correspondait à cette hypothèse.
De
ce fait, et notamment depuis la mise sur le marché du vaccin, mon
intérêt pour la compréhension du potentiel zêta s'est considérablement
accru. L'un des principaux objectifs de cette lettre d'information est
d'aider chacun à maîtriser le potentiel zêta (qui consiste
essentiellement à éliminer les ions positifs forts et à les compléter
par des ions négatifs forts), car il révolutionne de nombreux domaines
de la médecine et de la santé.
Remarque : le sujet du potentiel zêta (ainsi que les références associées) est abordé plus en détail ici .
Cependant, je dois également préciser que je ne crois pas que le potentiel zêta soit le seul facteur à l'origine de la formation de boues sanguines ; je me suis plutôt concentré sur celui-ci parce qu'il est tout simplement le plus facile à comprendre et à traiter rapidement (par exemple, je crois qu'il y a encore beaucoup de choses que nous ne comprenons pas sur le comportement du sang et des fluides dans le corps, comme en témoignent des recherches russes oubliées qui montrent que le sang circule dans le corps en spirales tourbillonnantes dirigées par le cœur, ce qui réduit la résistance vasculaire et permet à des types spécifiques de sang d'arriver là où ils sont nécessaires).
DMSO et troubles neurologiques
Le DMSO possède de nombreuses qualités qui lui permettent de traiter une grande variété de maladies, notamment :
• Il améliore la circulation sanguine.
•
Il accélère la cicatrisation des tissus lésés (ce qui, selon moi,
résulte de l'amélioration de la circulation et de la stabilisation des
gels nécessaires au processus initial de cicatrisation).
• Il réactive les cellules dormantes bloquées dans la réponse de danger cellulaire .
• C'est un puissant antioxydant et anti-inflammatoire.
• Il augmente le tonus parasympathique (grâce à son action inhibitrice sur l'acétylcholinestérase ) et apaise les circuits neuronaux dysfonctionnels (leur permettant ainsi de se réinitialiser).
• Il réduit efficacement la douleur (notamment en bloquant la transmission de la douleur et en relaxant les muscles ).
• Il protège les cellules et les tissus contre de nombreux facteurs de stress nocifs et potentiellement mortels.
•
Il constitue un vecteur efficace pour d'autres substances
thérapeutiques auxquelles il est associé (en particulier en application
topique).
De ces effets, je crois que les trois premiers (amélioration de la circulation, régénération tissulaire et réinitialisation de la réponse cellulaire au danger – et peut-être les propriétés anti-inflammatoires et antioxydantes du DMSO) sont particulièrement importants pour les troubles neurologiques (que le DMSO est reconnu depuis longtemps pour traiter) car :
Le
tissu nerveux présente la demande énergétique la plus élevée de
l'organisme et est le plus sensible à une réduction de son apport
sanguin (par exemple, les fonctions du système nerveux s'interrompent
souvent immédiatement dès que l'irrigation sanguine est coupée).
Ce tissu
est particulièrement vulnérable aux interruptions d'irrigation sanguine
et, une fois celles-ci survenues, il reste souvent bloqué dans un état
dormant, une sorte de « pénombre », semblable à la réponse cellulaire au danger (après
quoi le tissu finit par mourir). De plus, le cerveau et la moelle
épinière figurent parmi les tissus les plus résistants à la
cicatrisation et à la régénération de tout le corps.
•Comme une grande partie de la vie dépend d'un système nerveux fonctionnel, les pertes partielles de fonction dues à l'un ou l'autre des facteurs précédents entraînent des conséquences immédiates et perceptibles pour l'individu (alors que les pertes partielles de fonction des organes internes peuvent même passer inaperçues sans analyses de laboratoire).
Compte tenu de tout cela, j'ai supposé que le DMSO devait améliorer le potentiel zêta, car bien qu'il possède de nombreuses propriétés anticoagulantes prouvées (discutées ici ), bon nombre des changements qu'il a créés étaient identiques à ce qui résulterait d'une amélioration de la microperfusion via un espacement des globules rouges.
Cependant, lors de mon analyse de la littérature, j'ai constaté que le DMSO (du fait de sa neutralité électrique) n'améliore pas le potentiel zêta des globules rouges et, au contraire, le diminue légèrement . De même, le DMSO , intrinsèquement visqueux , augmente la viscosité de l'eau en modifiant sa structure 1,2,3 (ce qui est observable lors du mélange des deux).
Remarque : cette modification exothermique explique le dégagement de chaleur provoqué par le mélange du DMSO avec l'eau .
Cependant, les formulations à base de DMSO ont une faible viscosité ( 1 , 2 , 3 , 4 , 5 , 6 , 7) (ou deviennent chargées négativement lorsqu'elles sont préparées dans du DMSO). Le DMSO diminue la viscosité des ions hydrophobes en solution et, surtout, réduit l'agrégation des cellules sanguines (formation de bouchons sanguins) et la viscosité du sang, ce qui, à mon avis, est dû à :
Il agit comme un agent stabilisant (favorisant) le gel, formant ainsi des barrières d'eau entre les particules, les empêchant de s'agréger (et faisant passer des biomolécules comme l'urée d'une formation de gel opposée à une formation de gel favorable ).
Le DMSO, en réduisant les forces d'attraction entre les globules rouges identifiées par Knisely (par exemple, en neutralisant les protéines agrégées), permet ainsi au potentiel zêta existant de disperser les cellules sanguines.
Il neutralise également les facteurs d'agglomération observés dans les états pathologiques qui, autrement, provoquent l'agglutination des cellules sanguines. Par exemple :
• Le DMSO (3 %), en diminuant la viscosité sanguine (et en augmentant la mobilité moléculaire), a complètement empêché l'adhérence de S. aureus aux globules rouges (l'adhérence provoquant leur agrégation).
• Lorsque le DMSO a été mélangé à du LPS (pour modéliser une septicémie), au lieu d'augmenter la viscosité (un facteur clé de la septicémie), la viscosité sanguine a diminué, et cette diminution s'est accentuée après l'ajout de resvératrol .• Dans le cancer, le DMSO a empêché la réduction du potentiel zêta (et de la mobilité) qui se produirait autrement dans les macrophages.
• Empêche les ions positifs de perturber le potentiel zêta de la laponite chargée négativement.
• Lorsqu'elles étaient exposées à des radiations (rayons gamma), les protéines du cristallin de l'œil s'agrégeraient et la viscosité augmenterait ; le DMSO empêchait cela.
Pour s'implanter dans les poumons, les bactéries qui colonisent fréquemment les patients atteints de mucoviscidose libèrent de la cépacane, un polysaccharide qui forme des biofilms épais dans le mucus pulmonaire (déjà épais), rendant la respiration beaucoup plus difficile pour ces patients. Des études en laboratoire ont montré que le DMSO désagrège les agrégats de cépacane et réduit de moitié leur viscosité (ce qui pourrait expliquer en partie pourquoi un médecin a constaté une amélioration spectaculaire de l'état de santé de son patient atteint de mucoviscidose après la prise de DMSO). De plus, il a été observé que le DMSO, en association avec l'ivacaftor (un médicament essentiel utilisé pour traiter la mucoviscidose), réduit la viscosité du mucus pulmonaire épaissi par la fumée de cigarette.
Tout cela a été parfaitement démontré par une remarquable étude de 2009 1 , 2 réalisée par une équipe de chercheurs géorgiens étudiant les effets de l'hyperthermie (un traitement contre le cancer) sur le cerveau, car contrairement au reste du corps, le cerveau et la moelle épinière sont connus pour commencer à être endommagés par des températures plus élevées, avec un dysfonctionnement neurologique commençant à 40-41°C et des dommages thermiques histologiques (par exemple, une nécrose de coagulation) survenant chez les primates après une heure à 44°C (c'est pourquoi 43°C pendant 60 minutes est souvent considéré comme la limite de sécurité pour le traitement par hyperthermie).
Cette
étude a chauffé directement le liquide céphalo-rachidien de rats, puis a
évalué directement les modifications du flux sanguin cérébral et les
lésions consécutives. Les résultats ont montré que :
•
L’augmentation de la chaleur entraînait une augmentation de la
microcoagulation (confirmant les observations de Knisely et Riddick),
une diminution du flux sanguin et des lésions du tissu cérébral dues à
cette diminution.
•
Le DMSO a neutralisé tous ces effets, préservant le flux sanguin et le
tissu cérébral. À l’inverse, le dextran de haut poids moléculaire (une
substance utilisée par Knisely pour induire la formation de boues
sanguines) aggravait cette formation et les lésions cérébrales,
démontrant ainsi pourquoi la formation de boues sanguines peut provoquer
de nombreux troubles du système nerveux et pourquoi le DMSO est capable
de l’antidoter.
Remarque : ces résultats plaident également fortement en faveur de l'utilisation du DMSO pour atténuer les effets néfastes des coups de chaleur et des fortes fièvres.
De plus, il a également été démontré que le DMSO :
• Dans la microcirculation intestinale du rat, pour réduire l'adhérence des leucocytes induite par le chimioattractant (mais pas la vitesse de roulement ni le flux), contrecarrant ainsi le processus inflammatoire à l'origine des micro-accidents vasculaires cérébraux que Moulden avait découvert, à savoir l'obstruction des plus petits vaisseaux sanguins par de gros globules blancs.
Dans les vaisseaux microlymphatiques du mésentère intact de rat, la stimulation constante des contractions phasiques a permis d'augmenter la proportion de vaisseaux présentant des contractions phasiques spontanées, passant d'une valeur de base de 26-42 % à 43-59 %, tout en doublant approximativement la fréquence de contraction, d'environ 11 à 25 par minute. Ces contractions, en stimulant le flux lymphatique, ont entraîné une augmentation marquée de la vitesse de la lymphe — doublant approximativement dans 100 % des vaisseaux (par interférométrie de speckle) et montrant une augmentation de mouvement de 40 à 100 % dans 60 à 64 % des vaisseaux (par microscopie directe) — stimulant ainsi la fonction de drainage de la microcirculation lymphatique. Le DMSO a également complètement supprimé les effets lymphoconstricteurs de la toxine staphylococcique bactérienne (qui pouvaient évoluer vers l'oblitération des microvaisseaux), normalisé le drainage lymphatique et atténué l'impact létal global de la toxine. Enfin, les chercheurs russes à l'origine de cette découverte ont également constaté qu'une exposition de plus de 15 minutes à 30 % de DMSO induisait une lymphostase dans 20 à 40 % des vaisseaux (concentrations qui ne pourraient jamais être atteintes chez un patient sous DMSO). 1 , 2 , 3 , 4
• Pour améliorer la circulation lymphatique dans de nombreux contextes — notamment pour résoudre la lymphostase chez les patients atteints du sarcome de Kaposi et chez 115 patients présentant des plaies purulentes , faciliter le drainage lymphatique ( par stimulation électrique et acide hyaluronique ), augmenter la microcirculation rénale et le flux lymphatique , augmenter le flux lymphatique dans l'arthrose , augmenter le flux lymphatique de manière dose-dépendante (comme solvant pour le Daflon intraveineux ), faciliter la croissance de nouveaux vaisseaux lymphatiques ( avec l'acide 13-cis-rétinoïque ) et traiter le lymphœdème post-mastectomie (conformément à de multiples recommandations, études et revues 1 , 2 , 3 ). De plus, un brevet russe de détoxification a d'abord stimulé le transport humoral interstitiel et le drainage lymphatique en appliquant du DMSO combiné à une enzyme protéolytique sur les pieds, puis, 30 à 60 minutes plus tard, en filtrant le sang par plasmaphérèse.
Remarque : le DMSO est également utilisé pour administrer directement des thérapies topiques ou injectées dans le système lymphatique 1 , 2 , 3 , 4 , 5 , 6 , 7 , 8 et pour traiter un large éventail de lymphadénites (par exemple, dues au vaccin BCG, 1 , 2 , 3 , 4 , 5 , 6 , 7 , 8 , 9 , 10, à la tuberculose, 1 , 2, à l'érysipèle hémorragique , au MIS-C post-COVID , à l'amygdalite et aux infections bactériennes qui ont hospitalisé 61 enfants 1 , 2 ).
Enfin, un effet secondaire fréquent du DMSO par voie intraveineuse est l'hémolyse osmotique, qui touche principalement les globules rouges âgés (éliminés par la rate). On sait que les globules rouges âgés sont beaucoup plus sujets à l'agglutination et à l'agrégation (en partie parce qu'ils perdent leur charge négative avec l'âge) ; de ce fait, la circulation s'améliore avec leur élimination. Ceci contribue à expliquer l'observation de Jack De La Torre concernant les bolus de DMSO par voie intraveineuse chez les patients cérébro-lésés :
De plus, une hématurie due à l'hémolyse osmotique des globules rouges a été observée chez tous les patients uniquement après la dose de charge initiale de DMSO. Cette hématurie s'est stabilisée après les doses suivantes de DMSO. La dose de charge de DMSO n'a d'autre conséquence qu'une diminution de l'hématocrite d'environ 25 %, une réaction transitoire qui, paradoxalement, réduit la viscosité sanguine et les résistances vasculaires tout en augmentant le débit sanguin cérébral .
DMSO et barrière hémato-encéphalique
Parallèlement à l'augmentation de la circulation sanguine, le DMSO se diffuse rapidement dans l'organisme. Cinq minutes après application cutanée, il est présent dans le sang, trente minutes dans l'ensemble des organes et une heure dans les os. Cependant, il ne s'accumule pas dans le corps après une utilisation prolongée (par exemple, 85 % sont excrétés inchangés dans l'urine en 24 heures ) et il n'en reste pratiquement plus aucune trace une semaine après l'administration. 1,2,3
De plus, des études menées chez la souris et le rat ont montré que le DMSO, à des concentrations de 10 à 15 %, ouvre de manière réversible la barrière hémato-encéphalique (BHE), permettant ainsi à des protéines comme la peroxydase de raifort (HRP), à de nombreux médicaments, dont la pémoline, le kétoconazole (avec une augmentation de leur concentration cérébrale de neuf fois), ou le médicament contre la maladie de Parkinson, la L-dopa (qui augmente les niveaux de dopamine dans les régions tubéro-infundibulaire et néostriatale, et dont l'effet est encore potentialisé par l'association avec la carbidopa), aux lysosomes transportant des médicaments et à des acides aminés comme la tyrosine d'atteindre le tissu cérébral en plus grande quantité qu'en l'absence de DMSO. 1 , 2 , 3 , 4 , 5 , 6 , 7 , 8 , 9 , 10 , 11 , 12 , 13 , 14 , 15 , 16 , 17 , 18 , 19 , 20
Le DMSO a également augmenté d'environ 57 % le transfert d'acides aminés à travers l'espace sous-arachnoïdien vers le tissu cortical sous-jacent. Chez les poussins nouveau-nés, l'administration intraveineuse de DMSO a augmenté les concentrations cérébrales d'adrénaline et de noradrénaline d'environ 35 à 39 % et a intensifié leurs effets centraux. 1,2 De même, chez le chien, l'administration intraveineuse de DMSO à des débits de perfusion croissants a permis d'atteindre une concentration dans le LCR environ deux fois inférieure à la concentration plasmatique correspondante , confirmant une pénétration (plus lente) à travers la barrière hémato-encéphalique (BHE) vers le SNC. Cette capacité à faciliter l'administration de médicaments au cerveau sous-tend le potentiel thérapeutique du DMSO pour les troubles neurologiques (par exemple, la maladie de Parkinson) et a conduit à son regroupement avec le mannitol en tant qu'agent clinique pour améliorer l'administration de médicaments au cerveau . De même, le DMSO a été incorporé dans des formulations de nanoparticules ciblant le cerveau, telles que les micelles de poloxamère médiées par le glucose, qui ont montré un transport significativement plus élevé à travers un modèle de BHE que les micelles ordinaires. 1 , 2
Remarque :
les résultats concernant l’ouverture temporaire de la barrière
hémato-encéphalique (BHE) par le DMSO sont mitigés (par exemple, huit
études ont conclu à son inefficacité ; 1 , 2 , 3 , 4 , 5 , 6 , 7 , 8 ont montré qu’une concentration de DMSO d’au moins 1 % était nécessaire pour l’ouverture de la BHE, tandis qu’une autre a
constaté un effet minimal sur le transport de la dopamine). D’autres
études ont également mis en évidence des problèmes liés à cette
ouverture ; 1 , 2
tandis que chez le rat et le lapin, les perfusions de DMSO dans les
carotides n’ont pas altéré la BHE, les artères ni le cerveau ; 1 , 2 et une revue vétérinaire de 1985 a également noté que le DMSO permet à certaines substances, mais pas à d’autres, de traverser la BHE.
Dans des études d’IRM chez la souris, le DMSO s’est accumulé à des
concentrations 1,5 fois supérieures dans les glioblastomes que dans le
tissu cérébral normal, avec une élimination 2,2 fois plus longue, créant
ainsi des zones de forte concentration tumorale. Contrairement au gadolinium, produit de contraste toxique, le DMSO traverse librement la
barrière hémato-encéphalique intacte, permettant la visualisation de
tumeurs de bas grade invisibles à l'IRM conventionnelle. De plus, lors
de la chimiothérapie, la diminution de la rétention de DMSO signale la
réponse au traitement plus précocement que les modifications
volumétriques observées en IRM. 1,2,3,4,5,6 il a également été démontré que le DMSO améliore la pénétration de la lumière dans le
tissu cérébral, optimisant ainsi les techniques de diagnostic optique
pertinentes pour certaines affections neurologiques . 1,2
DMSO et troubles psychiatriques
Deux des critiques les plus fréquentes adressées à la psychiatrie sont que ses médicaments (souvent très toxiques) ne traitent pas la maladie sous-jacente – nécessitant une prise en charge symptomatique à vie – et que de véritables problèmes biologiques (par exemple, les effets indésirables du vaccin contre la COVID-19) sont régulièrement diagnostiqués à tort comme des troubles psychiatriques primaires. Ces deux problèmes découlent de l'hypothèse erronée selon laquelle la plupart des troubles psychiatriques ont une origine purement psychologique, alors qu'en réalité, nombre d'entre eux ont une base biologique (neurologique) évidente.
Mon point de vue est le fruit de l'observation répétée de l'apparition de symptômes psychiatriques suite à des lésions cérébrales et du constat que les thérapies médicales restaurant la santé cérébrale améliorent également les troubles psychiatriques. Par exemple, l'une de mes thérapies préférées, l'irradiation sanguine aux ultraviolets, agit en améliorant la circulation, en réduisant l'inflammation et en réactivant les cellules dormantes – autant d'effets que le DMSO produit également . Ces processus étant à la base de nombreuses maladies, et de la même manière qu'une abondante littérature scientifique soutient l'efficacité de l'irradiation sanguine aux ultraviolets dans un large éventail d'affections, y compris psychiatriques, il en va de même pour le DMSO (comme je le démontrerai tout au long de cet article).
En recensant toutes les publications existantes sur le DMSO, j'ai découvert une équipe russe (de l' Institut de l'activité nerveuse supérieure et de neurophysiologie de l'Académie des sciences de Russie ) qui a produit certaines des meilleures preuves que j'aie trouvées en faveur de cette théorie. 1 , 2 , 3 , 4 , 5 , 6 , 7 , 8
En bref, dans leurs efforts pour trouver une cause biologique aux troubles psychiatriques (qui ont une grande variété de causes apparemment sans lien entre elles), ils ont découvert que le stress chronique qui provoque des troubles psychiatriques s'accompagne d'une altération de la circulation sanguine vers le cerveau, ce qui déclenche divers processus dégénératifs, en particulier lorsque la capacité de l'individu à compenser un stress aigu à court terme est dépassée par un stress chronique et prolongé.
Pour
étudier ce phénomène, ils ont induit de manière répétée des névroses
chez des animaux en les soumettant à des stress prolongés (bruit blanc,
flashs lumineux et chocs électriques pendant plus de trois semaines).
Ils ont ensuite mesuré directement le débit sanguin dans le territoire
de l'artère cérébrale moyenne par biomicroscopie (fenêtre crânienne) et
par la méthode de clairance de l'hydrogène, puis examiné directement les
cerveaux.
Remarque : le terme « névrose »
est un terme psychiatrique ancien. Dans le contexte de l'époque
soviétique, il désignait un dysfonctionnement du système nerveux
supérieur causé par un stress chronique qui dépasse les capacités
d'adaptation de la personne. Les équivalents modernes incluent le
trouble d'anxiété généralisée, le trouble mixte anxieux-dépressif
(CIM-11), la neurasthénie et le trouble de l'adaptation avec humeur
anxieuse ou dépressive.
Ils en ont déduit :
Le cerveau reçoit normalement un débit sanguin 5 à 7 fois supérieur par gramme de tissu à celui de la plupart des autres organes, en raison de ses besoins énergétiques exceptionnels. Un stress aigu provoque généralement une augmentation transitoire du débit sanguin cérébral, tandis qu'un stress chronique prolongé (entraînant une névrose) induit une diminution durable qui persiste 4 à 6 semaines après la fin de l'événement stressant. Cette réduction provoque une hypoxie circulatoire, une élévation du lactate cérébral, une diminution de l'activité de la caspase-3 et de la Na,K-ATPase, une altération de la respiration mitochondriale (notamment une réduction de l'activité de la succinate déshydrogénase et de la NADH déshydrogénase) et une augmentation de la production d'espèces réactives de l'oxygène (ERO). Chez les animaux incapables de s'adapter en passant de l'oxydation de l'acide succinique à l'oxydation du NADH, la résistance au stress est fortement réduite. L'hypoxie qui en résulte augmente également l'activité de la cytochrome oxydase (de 35 à 40 %) et déclenche la biogenèse mitochondriale, suivie d'une peroxydation lipidique (LPO) induite par les ERO. 1 , 2 , 3 , 4
Remarque : le cerveau est particulièrement vulnérable à cette cascade
en raison de son taux métabolique et de sa demande en oxygène
exceptionnellement élevés, ainsi que de sa teneur élevée en acides gras
polyinsaturés (oxydables) dans les membranes cellulaires.
Aux
premiers stades de la névrose, le stress aigu, une réponse protectrice
non spécifique, inhibe la peroxydation lipidique (LPO), entraîne
l'accumulation de phospholipides facilement oxydables, diminue la teneur
en cholestérol et augmente l'activité de piégeage des superoxydes (en
partie grâce aux hormones du stress agissant comme piégeurs de radicaux
libres). En cas de stress chronique persistant, cette phase protectrice
est dépassée, ce qui conduit à l'activation de l'oxydation lipidique par
les radicaux libres, à une déplétion progressive des phospholipides, à
une accumulation de cholestérol et à une
augmentation des protéines oxydées. Ces modifications membranaires
biphasiques augmentent initialement la résistance à la peroxydation,
mais rendent finalement les membranes plus vulnérables à mesure que le
stress se prolonge.<sup>1,2,3,4 </sup> Remarque : ce profil biphasique a également été observé
chez les femmes souffrant de dysménorrhée (après 12 heures de douleur,
les taux plasmatiques de bases de Schiff étaient réduits de près des
deux tiers, tandis qu'après 12 à 24 heures, ils étaient presque le
double des valeurs témoins).
Les adaptations ultérieures au stress chronique sont plus spécifiques et les modifications membranaires et radicalaires présentent souvent une asymétrie interhémisphérique variable selon le type comportemental. Par exemple, en cas de stress aigu, les animaux à forte réactivité et résonance émotionnelles présentent une orientation vers une dominance droite ou une polarisation latérale gauche (LPO) équilibrée (comme les rats sensibles au stress qui excellent dans les labyrinthes), tandis que les animaux à faible réactivité présentent une LPO plus importante à gauche (comme les rats résistants au stress qui ont des difficultés dans les labyrinthes).
Ces
modifications moléculaires s'accompagnent de perturbations
physiologiques manifestes : élévation et fluctuation de la pression
artérielle systolique, perturbation et réduction du débit sanguin
cérébral local, perte de spécificité fonctionnelle ( égalisation du débit sanguin entre les structures cérébrales )
et évolution comportementale vers une attitude passive-défensive. Le
stress et l'hyperactivité sympathique pouvant induire ces troubles du
système nerveux autonome, les chercheurs ont conclu que la restriction
du débit sanguin cérébral qui en résulte contribue à de nombreux
symptômes observés dans les névroses.
Remarque : l'une de mes modalités thérapeutiques préférées ( la thérapie neurale )
agit en neutralisant les perturbations du système nerveux autonome et
produit fréquemment des réponses rapides et spectaculaires dans les
maladies complexes, ce qui, à mon avis, est lié au processus
pathologique décrit par les chercheurs russes.
Ils ont également constaté que la
libération locale de noradrénaline au sein de l'hypothalamus latéral
participe à un système dépresseur qui contribue à normaliser
l'hypertension artérielle. Lors d'un stress aigu, la vitesse de retour à
la pression artérielle de base dépend de l'intensité de cette réponse
noradrénergique locale dans l'hypothalamus latéral. Ainsi, lorsque ce
mécanisme est altéré, un stress répété peut entraîner une instabilité
hémodynamique prolongée qui, à terme, peut contribuer à une dérégulation
de l'autorégulation cérébrale et à une réduction durable du débit
sanguin cérébral (ce qui endommage l'hypothalamus et engendre un cercle
vicieux de maladie chronique).
Remarque :
la plupart des hypertensions chroniques sont d'origine inconnue. Ce
modèle pourrait expliquer une cause majeure jusqu'alors méconnue (ainsi
qu'une autre raison pour laquelle la restauration du potentiel zêta améliore la pression artérielle ,
car elle rétablit le flux sanguin vers l'hypothalamus). Par ailleurs,
il convient de noter que certains praticiens de médecine holistique ont
rapporté des succès significatifs dans le traitement de l'hyperactivité
sympathique en agissant sur la fonction hypothalamique.
Le débit sanguin cérébral normal est d'environ 50 ml/100 g/min ; en cas de névrose chronique, il chute en dessous de 30 ml/100 g/min . Les vaisseaux cérébraux perdent également leur capacité d'autorégulation : après une occlusion carotidienne bilatérale, les animaux sains présentent une dilatation artérielle généralisée, tandis que les animaux névrosés présentent des réponses artérielles et veineuses mixtes (par exemple, 54 % des artérioles sont dilatées, 21 % sont contractées et 25 % restent inchangées), avec de fréquentes contractions spastiques, des déformations en forme de bouteille, des interruptions du flux sanguin et des réactions vasculaires piales anormales. Il en résulte une relative égalisation du débit sanguin dans toutes les structures étudiées (indiquant une perte de spécificité fonctionnelle, ce qui, à mon sens, revêt une importance clinique considérable, car certaines traditions de guérison associent cette modification circulatoire à la mort imminente).
Remarque : dans de nombreux cas , l'hémodynamique cérébrale ne se rétablit jamais complètement après la période de stress chronique.
Ces modifications hémodynamiques sont parallèles à l'homogénéisation de l'activité EEG observée dans les névroses. La biomicroscopie a confirmé des perturbations microstructurales compatibles avec une hypoxie, notamment un œdème périvasculaire et péricellulaire, des vaisseaux tortueux, des neurones sombres, des cellules acidophiles, une prolifération microgliale et des lésions de l'hippocampe (en particulier un soma rétréci, des noyaux altérés et des dendrites en tire-bouchon dans CA3 ; une perte cellulaire de 2,7 à 7,1 % dans CA1, proche du seuil de déficience cognitive et de démence).
•Le processus endommage sélectivement les récepteurs β-adrénergiques du cerveau (qui, pendant environ une semaine, ont montré une diminution de l'affinité du récepteur compensée par une augmentation du nombre de récepteurs, la densité élevée des récepteurs persistant après trois semaines), le cortex sensorimoteur (couche V) et l'hippocampe (dans la couche pyramidale, en particulier dans le champ CA3 ).
•Trois stades du syndrome général d’adaptation ont été identifiés dans le modèle de stress émotionnel et douloureux chronique : (1) recherche initiale d’un fonctionnement optimal avec des défauts viscéraux résiduels, un comportement dominé par la peur et une pression artérielle labile, durant une semaine ; (2) stabilisation autonome partielle mais déplétion continue des phospholipides (« usure locale ») ; (3) épuisement avec rupture de la régulation autonome, activation de la LPO et perturbation membranaire profonde des neurones, des cellules gliales et des synapses, contribuant à la rupture de l’activité nerveuse supérieure, qu’ils ont décrite comme une « adaptation pathologique à coût structurel élevé ».
Ils ont ensuite :
•Il
a souligné que la réaction interne d'un individu face aux facteurs de
stress, plutôt que le facteur de stress lui-même, est primordiale (« … peu importe les faits qui nous sont rapportés ; ce qui importe, c'est notre réaction ; c'est là la question essentielle »)
et a établi un lien avec l'observation selon laquelle de nombreuses
maladies résultant d'un stress psycho-émotionnel chronique sont
caractérisées par des troubles du système nerveux autonome (vasculaire),
des états hypoxiques et de graves perturbations des processus
métaboliques, se manifestant souvent par une dysrégulation
autonome/vasculaire, une hypoxie et des troubles métaboliques.
Remarque : la personne non anglophone qui a forgé le concept médical de stress a par la suite déclaré avoir utilisé le mauvais terme et voulait parler de « tension » (la façon dont un système se déforme en réponse au stress).
•Il a été noté que, si de nombreuses personnes atteignent le stade de névrose complète, beaucoup plus se trouvent dans un stade pré-névrotique de tension importante sans décompensation complète et bénéficieraient grandement d'interventions thérapeutiques précoces dans leur processus pathologique.
•Ils ont souligné que les effets du stress chronique qu’ils observaient étaient similaires à ceux observés après un accident vasculaire cérébral , une crise cardiaque ou un traumatisme crânien , et dans de nombreux cas, ils ont utilisé avec succès les mêmes thérapies pour les deux (par exemple, le panthénol ⬖ ).
Pour traiter la névrose :
•Les chercheurs ont d’abord utilisé des agents aux propriétés antihypoxiques et antioxydantes (par exemple, la carnosine , la substance P , le phénosan K ou des antioxydants phénoliques synthétiques 1 , 2 ) et ont constaté que ces interventions prévenaient et traitaient efficacement la névrose expérimentale chez les animaux (alors que les animaux non traités développaient systématiquement une névrose et présentaient une faible récupération).
Remarque : d’autres agents comme le panthénol n’ont apporté que des améliorations temporaires. Par ailleurs, l’alcool (un piégeur de radicaux hydroxyles) s’est également révélé efficace, offrant une nouvelle explication au soulagement partiel de la dépression chronique procuré par l’alcool. Notamment, le stress chronique diminue l’activité de la Na,K-ATPase cérébrale (comme détaillé précédemment), et une étude distincte sur cette enzyme a montré que si le DMSO et l’éthanol piègent tous deux les radicaux hydroxyles, l’éthanol déstabilise davantage l’enzyme tandis que le DMSO la stabilise – ce qui pourrait expliquer pourquoi le DMSO procure un bénéfice durable là où l’alcool n’apporte qu’un soulagement temporaire (alors que, parallèlement, Riddick a constaté que l’alcool augmentait la viscosité sanguine).
Après avoir testé plusieurs agents, les chercheurs ont obtenu d'excellents résultats avec l'ionothérapie négative (qui
possède un effet antihypoxique marqué). En présence d'ions négatifs
lors d'un stress aigu (par exemple, une immobilisation), ces ions ont
complètement prévenu les altérations cérébrales pathologiques chez tous
les animaux, quel que soit leur comportement. Ils ont notamment préservé
l'activité des enzymes oxydatives dans le cortex sensorimoteur et
normalisé les paramètres comportementaux et autonomes (fréquence
cardiaque, pression artérielle et respiration). Des effets protecteurs
similaires ont été observés avec l'acide succinique (30 mg/kg par voie orale une fois par jour pendant 8 jours), qui a également permis de
préserver le comportement d'orientation après un infarctus. Il est à
noter que les rats présentant un comportement actif ont montré une plus
grande résistance naturelle à l'hypoxie cérébrale, avec une augmentation
plus rapide du débit sanguin cérébral local et de la pression partielle
d'oxygène dans le cerveau pendant le stress.
Remarque : les ions positifs présents dans l'air sont largement associés à des troubles psychiatriques . Je pense que cela est dû au fait que les ions positifs altèrent le potentiel zêta et réduisent ainsi la microcirculation cérébrale (alors que les ions négatifs la rétablissent).
Leurs meilleurs résultats ont été obtenus en combinant le DMSO oral (un puissant piégeur de radicaux hydroxyles) à la vitamine Eβ (alpha-tocophérol ) . Ils ont constaté que l'efficacité de cette combinaison était supérieure à celle des deux substances administrées séparément (par exemple, pour des troubles du système nerveux autonome ou du comportement ). Ils ont attribué ce succès au fait que le DMSO renforce le pouvoir antioxydant de la vitamine Eβ, car il peut l'acheminer rapidement jusqu'aux membranes cellulaires avant qu'elle ne perde son pouvoir antioxydant en réagissant avec d'autres substances dans l'organisme ( ce qui est corroboré par la réduction des produits d'oxydation des radicaux libres, l'augmentation de l'activité de piégeage des superoxydes dans le cerveau et le sérum sanguin, l'augmentation de la teneur en phospholipides cérébraux et la normalisation du taux de cholestérol cérébral). Enfin, en 1999, ils ont annoncé que ces résultats commençaient à être reproduits dans le cadre d'essais cliniques autorisés par le gouvernement à l'Académie de médecine de Moscou.
Bien que l'on puisse dire beaucoup de choses sur leurs recherches, l'un des principaux enseignements que j'en ai tirés est l'une des explications mécanistiques les plus claires que j'aie rencontrées sur le rôle réel des adaptogènes (un terme appliqué à de nombreux produits naturels), car les agents qui ont efficacement contrecarré l'ensemble du processus de stress ont été explicitement qualifiés d'« adaptogènes » par les chercheurs.
Remarque : pour compiler le résumé ci-dessus et représenter fidèlement leurs conclusions, j'ai lu plus de 50 articles (dont beaucoup omettaient des détails clés) et j'ai fait de mon mieux pour intégrer leurs conclusions à la science physiologique actuelle.
Forts de cette compréhension (et d'une exploration plus approfondie de l'importance du drainage circulatoire qui sera abordée dans la section consacrée à la sclérose en plaques), examinons maintenant comment ces propriétés permettent au DMSO d'agir sur un large éventail de troubles neurologiques et psychiatriques.
maladie de Parkinson
La
maladie de Parkinson résulte de la perte progressive des neurones
dopaminergiques de la substance noire. La recherche dans ce domaine a
été révolutionnée au début des années 1980 lorsque des consommateurs de
drogues récréatives, ayant consommé une héroïne synthétique de mauvaise
qualité, ont rapidement développé de graves symptômes parkinsoniens.
Cette héroïne était contaminée par du MPTP, un agent dont le métabolite
actif (MPP+) ciblait spécifiquement ces neurones, permettant ainsi de
modéliser la maladie de Parkinson de manière fiable chez les animaux de
laboratoire. On a ensuite constaté qu'un herbicide (le paraquat) était
très similaire au MPP+, qu'un autre pesticide (la roténone) provoquait
également des dommages neuronaux similaires, que divers pesticides
étaient associés à un risque accru de maladie de Parkinson (comme les
organophosphorés) et que le 6-OHDA pouvait également induire la maladie
de Parkinson de manière fiable.
À
noter : l'un des principaux problèmes posés par le glyphosate (Roundup)
est que, bien qu'il soit toxique, les herbicides qu'il a largement
remplacés, comme le paraquat, sont encore plus toxiques.
De
nombreuses études ont démontré que le DMSO contrecarre directement la
neurotoxicité des agents induisant la maladie de Parkinson (par exemple,
dans les études sur les organophosphorés mentionnées précédemment, le
DMSO a réduit la mortalité à plusieurs reprises, accéléré la
détoxification des organophosphorés et protégé la fonction
neuromusculaire). Plus remarquable encore, une étude cas-témoins sur
la maladie de Parkinson à début précoce (63 cas, 68 témoins) a révélé
que les personnes atteintes de la maladie avaient dix fois moins de
risques d'avoir été exposées au DMSO que les témoins sains, ce qui
suggère que l'exposition au DMSO est associée à une réduction d'environ
10 fois du risque de développer la maladie (et pourrait donc avoir un
effet protecteur). En revanche, la même étude a constaté que
l'exposition aux insecticides multipliait le risque par près de 6, la
fumigation des logements par plus de 5 et l'exposition aux herbicides
par plus de 3 – des résultats concordants avec la littérature
épidémiologique abondante établissant un lien entre l'exposition aux
pesticides et la maladie de Parkinson.
Remarque :
cette étude a également révélé que le tabagisme était associé à un
risque réduit de maladie de Parkinson, une conclusion qui concorde avec
des décennies de données épidémiologiques établissant un lien entre
l’exposition à la nicotine et une incidence plus faible de la maladie de
Parkinson, ce qui confère une crédibilité à la méthodologie de l’étude.
Le DMSO a démontré directement des effets neuroprotecteurs dans plusieurs modèles de la maladie de Parkinson. Chez l'animal, il a supprimé les lésions nigrostriatales induites par les radicaux hydroxyles suite à l'administration de MPTP 1,2,3,4. Chez le rat atteint de la maladie de Parkinson induite par la roténone, le DMSO a amélioré la morphologie des neurones CA1 et CA3 de l'hippocampe , restaurant les cellules pyramidales et les corps de Nissl endommagés par la roténone et normalisant leur activité électrique. Le DMSO a également protégé les astrocytes de la toxicité induite par le MPP+en réduisant la peroxydation lipidique et les troubles métaboliques, a protégé la glutamine synthétase gliale des dommages causés par les radicaux hydroxyles induits par le MPP<sup>+</sup>, a protégé les cellules de neuroblastome humain SH-SY5Y de la cytotoxicité induite par le 6-OHDA et a réduit la peroxydation lipidique et la formation de protéines carbonylées dans les homogénats de cerveau de rat traités au chlorure ferreux ou au peroxyde d'hydrogène. Il a également réduit la production de radicaux hydroxyles lors de l'auto-oxydation du 6-OHDA et la formation de produits dopaminergiques hydroxylés. 1 , 2
Remarque : dans une étude sur des souris ,
le DMSO intrapéritonéal n'a pas protégé contre l'épuisement de dopamine
induit par le MPTP, ce qui indique que ses effets neuroprotecteurs
peuvent dépendre de la voie, du moment ou de la dose d'administration.
Il est intéressant de noter que le DMS (métabolite odorant naturel du DMSO) à des concentrations proches des concentrations physiologiques protège également les neurones contre l'apoptose induite par le 6-OHDA et le MPP+, cet effet étant dépendant de la MsrA (l'enzyme qui convertit le DMS en DMSO). Ceci suggère que le cycle endogène DMS-DMSO participe à la défense antioxydante naturelle de l'organisme contre la neurodégénérescence dopaminergique. 1,2 Cela soulève une question intéressante : j'ai reçu des témoignages de patients atteints de la maladie de Parkinson ayant présenté des réponses spectaculaires au DMSO, mais ayant ensuite interrompu le traitement en raison de l'odeur gênante pour leurs relations sexuelles avec leur conjoint. Ma première idée a été de recommander une formulation de DMSO à faible odeur (voir ici ) , mais si le DMSO joue un rôle thérapeutique clé dans la maladie de Parkinson, cette approche pourrait ne pas être viable.
À noter : cette étude a
également montré que le DMSO protégeait contre la peroxydation lipidique
induite par le H₂O₂ et la production de superoxyde générée par
l'antimycine A.
De plus, le DMSO a inversé le blocage complet de l'assemblage des microtubules à partir de tubuline purifiée in vitro par la roténone – une découverte directement pertinente pour la maladie de Parkinson, car la désorganisation des microtubules altère le transport axonal et contribue à la mort des neurones dopaminergiques. De même, une monographie russe de physiothérapie recommandait l'application topique de compresses de DMSO-novocaïne pour les affections neurologiques, notamment la maladie de Parkinson, et un brevet proposait le DMSO comme potentialisateur transdermique d'un patch de toxine botulique pour traiter la spasticité associée à la maladie de Parkinson, à la paralysie cérébrale, à la dystonie et à la sclérose en plaques.
Remarque :
de nombreuses études (qui seront abordées plus loin dans cette série)
montrent que le DMSO stabilise les microtubules et explique probablement
certaines de ses propriétés neuroprotectrices.
Un
grand nombre d'agents, en association avec le DMSO, ont également
démontré un bénéfice thérapeutique dans des modèles de la maladie de
Parkinson.
La curcumine ⬖ a protégé les neurones dopaminergiques de la substance noire, réduit l'activation de l'iNOS et des cellules gliales, et stimulé les voies neuroprotectrices (IGF-1/Akt/FoxO3a). 1 , 2
La paeoniflorine ⬖ a réduit de façon répétée l'expression de l'α-synucléine, diminué la formation de corps de Lewy et protégé les neurones dopaminergiques dans de multiples études. 1,2 Elle a également inhibé l'hyperactivation microgliale, augmenté la sécrétion de BDNF et de GDNF et favorisé la différenciation des cellules souches neurales en neurones dopaminergiques . 1
L'icariside II ⬖ a induit la différenciation de cellules souches mésenchymateuses amniotiques humaines en cellules de type neuronal dopaminergique (concentration optimale : 3–10 µmol/L via la voie de signalisation PI3K). Dans un autre protocole, le DMSO a permis la différenciation de cellules iPS en progéniteurs dopaminergiques pour la thérapie cellulaire de la maladie de Parkinson.
Les ginsénosides Rg1 ⬖ et Rg3 ⬖ ont tous deux atténué de manière significative la perte de neurones dopaminergiques, la neuroinflammation et l'accumulation d'α-synucléine. 1 , 2 , 3 , 4
Le géniposide ⬖ a réduit les taux d'α-synucléine et prévenu la perte de neurones dopaminergiques en modulant l'axe miR-21/LAMP2A, tandis que le ginkgolide B ⬖ a réduit de la même manière l'expression de l'α-synucléine via la voie miR-207/LAMP2A.<sup> 1,2 l' ambroxol a augmenté l'activité de la β-glucocérébrosidase et réduit les taux d'oligomères d'α-synucléine, restaurant la viabilité cellulaire et la fonction mitochondriale dans les neurones dopaminergiques. Les polyphénols ⬖ ont réduit l'agrégation de l'α-synucléine induite par des réponses antioxydantes médiées par NRF2. L'acide carnosique ⬖ a atténué la neurotoxicité du 6-OHDA en régulant positivement la parkine et en restaurant la clairance protéasomale des protéines ubiquitinisées dans des modèles cellulaires et animaux de la maladie de Parkinson.
Le L-sulforaphane ⬖ dissous dans du DMSO a activé la voie NRF2 dans des cellules dérivées de patients atteints de la maladie de Parkinson, restaurant leurs niveaux déficients de glutathion — l'une des seules études utilisant de véritables cellules de patients.
Plus particulièrement , le NAMI-A — un complexe ruthénium-DMSO à faible toxicité — a inhibé l'agrégation de l'α-synucléine et les interactions membranaires avec une affinité submicromolaire, a désassemblé les fibrilles préformées, aboli la cytotoxicité de l'α-synucléine envers les cellules neuronales et atténué la neurodégénérescence et les troubles moteurs dans un modèle de rat atteint de la maladie de Parkinson, fournissant ainsi une nouvelle base pour la conception de complexes ruthénium-DMSO ciblant la pathologie induite par l'α-synucléine par un mécanisme distinct de celui des agents organiques.
Dans les modèles MPTP, la tanshinone IIA a préservé environ 75 % des neurones dopaminergiques tout en réduisant l'activation microgliale ; la tétraméthylpyrazine a prévenu les déficits moteurs et la perte neuronale via la voie Nrf2 ; le 6-hydroxy-1H-indazole a protégé 90 à 93 % des neurones dopaminergiques de la mort ; la baicaléine a réduit de manière dose-dépendante le comportement de rotation (un indicateur clé de l'atteinte motrice), la neuroinflammation et l'apoptose des neurones dopaminergiques via Wnt/β-caténine ; la néférine a amélioré les troubles moteurs chez la souris et réduit la neuroinflammation et l'α-synucléine dans la substance noire ; le SB239063 (un inhibiteur de la p38 MAPK) a protégé les neurones TH-positifs ; le NESS 0327 (un antagoniste du récepteur CB1) a amélioré les déficits moteurs ; de nouveaux inhibiteurs de la kinase c-Abl ont été plus efficaces que le nilotinib pour bloquer l'apoptose induite par le MPP+. Le GW5074 a prévenu la perte de neurones TH-positifs chez des souris génétiquement modifiées pour développer la maladie de Parkinson. Chez des souris présentant une lésion de la voie nigrostriée, l'inhibition d'ERK ( U0126 ) et l'inhibition de PDGFRα ( AG1296 ) ont réduit l'activation gliale et la cicatrisation, l'U0126 améliorant également les résultats neurocomportementaux à long terme.
Chez les souris atteintes de la maladie de Parkinson induite par le LPS , le pazopanib a protégé les neurones dopaminergiques en supprimant le TNF-α, le PGE2 et l'IL-6 via la signalisation MEK4-JNK-AP-1, tandis que la rapamycine a réduit la neuroinflammation en améliorant le métabolisme lipidique microglial.
Le NBP (un médicament chinois contre les AVC) a permis de préserver 30 % des neurones dopaminergiques et 49 % des terminaisons dopaminergiques striatales. Le carvacrol (présent dans les huiles d'origan et de thym) a exercé un effet neuroprotecteur via l'inhibition de TRPC1 dans les neurones dopaminergiques et l'activation de TRPA1 dans les astrocytes. L'association de dasatinib et de resvératrol a amélioré l'apprentissage , la mémoire et la coordination motrice, tout en réduisant l'anxiété . Le MOTS-c a amélioré la fonction motrice , inversé la perte de neurones TH-positifs et activé la voie antioxydante Nrf2/Keap1 chez les rats atteints de la maladie de Parkinson induite par la roténone. La puérarine a atténué les comportements de rotation et augmenté l'expression de DAT, VMAT2 et TH chez ces mêmes rats. Un inhibiteur de caspase a réduit la perte neuronale et amélioré les comportements de rotation chez les rats traités à la 6-OHDA, bien que le blocage de l'apoptose ait induit une nécroptose gliale compensatoire.
Shuimuheningfang ⬖ a amélioré les symptômes moteurs et non moteurs chez 80 patients atteints de la maladie de Parkinson et a réduit l'α-synucléine chez des souris modèles, 1 , 2 tandis que les granules composés Dihuang ⬖ (avec un inhibiteur de JNK) ont réduit le comportement de rotation et protégé les neurones dopaminergiques chez les rats 6-OHDA.
Dans les modèles de maladie de Parkinson de C. elegans , l'extrait de feuille d'olivier ⬖ a fortement protégé les neurones dopaminergiques de la toxicité du 6-OHDA (jusqu'à ~56 % de dégénérescence en moins), tandis que l'oleuropéine ⬖ , l'acide oléanolique ⬖ , le tyrosol ⬖ , le 3-hydroxytyrosol ⬖ , le safran ⬖ , le Polygonum multiflorum ⬖ et le Ziziphus jujuba ⬖ ont également fourni une protection significative.
Parmi les autres agents présentant des effets neuroprotecteurs dans les modèles de la maladie de Parkinson, on peut citer le guarana ⬖ (contre la roténone dans les cellules SH-SY5Y), l'huile de krill antarctique ⬖ (amélioration de l'activité locomotrice et des neurones dopaminergiques chez le poisson-zèbre), la lutéine ⬖ (amélioration dose-dépendante des fonctions cognitives et motrices chez le rat), les composés de cytochalasine issus de champignons endophytes (contre le MPP+), l'extrait d' Erythrina velutina ⬖ , l'acide rhizonique ⬖ et les dérivés de xylokétal ⬖ (contre les dommages induits par la 6-OHDA ou les ROS), le butyrate de sodium ⬖ (un inhibiteur d'HDAC qui restaure épigénétiquement l'expression du transporteur de dopamine et de VMAT2 contre la roténone et le MPP+), l'alloprégnanolone (qui favorise la régénération des cellules TH-positives via le BDNF et la CaMKIIδ3 contre la 6-OHDA) et la wedélolactone ⬖ (qui augmente l'activité neuroprotectrice dans la maladie de Parkinson). protéine DJ-1/PARK7), dexmédétomidine (neuroprotectrice via l'acétylation des histones médiée par ERK1/2), ainsi que 7,8-dihydroxyflavone , ⬖ cordycépine ⬖ (contre la roténone dans les cellules PC12), AMG9810 (un antagoniste de TRPV1 qui réduit les déficits moteurs mais altère la cognition en cas d'utilisation chronique), insuline avec l'inhibiteur de TLR4 TAK242 (améliore les performances motrices et normalise l'α-synucléine chez les rats 6-OHDA), catalpol ⬖ (réduit l'α-synucléine et améliore la fonction mitochondriale contre la roténone), génistéine , ⬖ décoction de Taohe Siwu , ⬖ composés de Ligusticum chuanxiong , ⬖ et acides gras de Nigella sativa . ⬖
Étant donné que le paraquat et d'autres herbicides figurent parmi les principaux facteurs de risque environnementaux de la maladie de Parkinson, il est également important de noter que le DMSO s'est avéré, dans de nombreuses études, capable de piéger les radicaux hydroxyles générés par le paraquat 1,2,3,4 . Des preuves directes chez le rat ont notamment démontré que le DMSO intercepte ces radicaux via une réaction de type Fenton, et des tests de biocapteurs bactériens ont montré que le DMSO piège jusqu'à 96 % des radicaux superoxydes générés par le paraquat. Il a également été démontré que le DMSO exerce un effet neuroprotecteur direct contre le paraquat dans des cultures de cellules striatales , qu'il supprime la signalisation inflammatoire induite par le paraquat (par exemple, l'IL-8 et l'activité chimiotactique des neutrophiles) et qu'il protège l'ADN de la mutagénèse induite par le paraquat . Ces résultats pourraient expliquer le constat épidémiologique d'une association inverse entre l'exposition au DMSO et le risque de développer la maladie de Parkinson. De plus, le myrténol , l' andrographolide (via Nrf2/HO-1), le VPA (un inhibiteur de l'HDAC), la chymostatine , le propofol et le resvératrol ont été combinés avec du DMSO pour contrer la toxicité et le stress oxydatif induits par le paraquat dans différents modèles de tissus.
Remarque : L’agrégation de l’α-synucléine en fibrilles toxiques est un facteur clé de la neurodégénérescence de la maladie de Parkinson. Une étude a montré que le DMSO, à des concentrations de 0,75 à 1,0 %, notamment en association avec du fer ferrique, favorisait la formation d’oligomères d’α-synucléine et sa cytotoxicité. Cependant, lors de tests réalisés chez des souris vivantes (normales et transgéniques surexprimant l’α-synucléine humaine) ayant reçu du DMSO par voie orale, aucune augmentation de l’agrégation de l’α-synucléine, aucune perte neuronale ni aucune pathologie de type Parkinson n’ont été observées. De même, l’injection de DMSO directement dans la substance noire n’a pas entraîné de perte de neurones dopaminergiques, d’accumulation de protéines ubiquitinisées ni de déficits comportementaux 1,2 , ce qui suggère que l’effet pro-agrégant du DMSO sur l’α-synucléine dans des cultures cellulaires isolées (à des concentrations bien supérieures à celles atteintes en clinique) ne se traduit pas dans l’organisme vivant.
Outre les données expérimentales, j'ai reçu quelques témoignages de lecteurs et de médecins ayant obtenu des résultats positifs avec le DMSO. Mon expérience portant principalement sur le DMSO administré par voie intraveineuse (qui, à mon avis, offre les meilleurs résultats), je souhaitais partager cet échantillon complet, incluant des approches non intraveineuses, afin d'illustrer la différence entre elles.
Une femme a décrit ce qui s'est passé lorsque son mari, atteint de la maladie de Parkinson, a reçu une perfusion intraveineuse de mannitol et de DMSO lors d'une thérapie par cellules souches à Amsterdam : « Il a descendu un escalier sans s'appuyer sur la rampe, a coupé ses aliments lui-même pendant une semaine, parlait distinctement et ouvrait les portières des taxis. » Ils savaient que ce n'était pas grâce aux cellules souches, dont les effets se feraient sentir dans plusieurs mois.
Le rapport le plus détaillé provient d'un chercheur diagnostiqué avec la maladie de Parkinson en 2018. Ce dernier, qui contrôlait déjà ses symptômes non moteurs grâce au sulforaphane (un activateur de Nrf2), présentait encore toute la gamme des symptômes moteurs. Après avoir testé systématiquement le DMSO par voie orale pendant plusieurs mois, il a constaté qu'à une dose optimale, la bradykinésie disparaissait, la douleur et la dystonie étaient réduites de 80 %, la rigidité de 50 % et le niveau d'énergie était nettement supérieur. Il a observé que le DMSO agissait sur les symptômes moteurs là où le sulforaphane était inefficace, ce qui suggère que le DMSO atteint le cerveau par des voies inaccessibles au sulforaphane – ce qui concorde avec sa capacité connue à traverser la barrière hémato-encéphalique. Il est à noter que des doses supérieures à son seuil de tolérance aggravaient systématiquement les tremblements, la rigidité et les troubles du sommeil, mais ces effets disparaissaient complètement dans les deux jours suivant l'arrêt du traitement.
Une troisième personne a indiqué que le DMSO topique et oral avait initialement aidé son mari atteint de la maladie de Parkinson à marcher sur de courtes distances, mais que l'effet n'avait pas persisté.
De plus, j'ai également reçu quelques témoignages selon lesquels la prise orale de DMSO aiderait des lecteurs atteints de la maladie de Parkinson, mais comme ces témoignages étaient informels (verbaux), je ne peux pas fournir de détails à ce sujet.
Compte tenu de tout cela (et de notre propre expérience avec la maladie de Parkinson), je pense que le DMSO présente un grand potentiel pour le traitement de cette maladie. L'administration orale est susceptible d'être bénéfique aux patients, et l'administration intraveineuse encore davantage. Les meilleurs résultats seront obtenus en associant le DMSO à un agent neurotrophique complémentaire. J'ai actuellement identifié un candidat très prometteur à cet effet (ainsi que quelques autres pistes), mais comme le démontrent les études d'association mentionnées précédemment, il en existe probablement beaucoup d'autres qui restent à découvrir.
Sclérose latérale amyotrophique (SLA)
La sclérose latérale amyotrophique (SLA) est une maladie neurodégénérative progressive caractérisée par la mort graduelle des motoneurones contrôlant les mouvements volontaires. Il en résulte une faiblesse musculaire croissante, une paralysie et, généralement, le décès dans les 2 à 5 ans suivant le diagnostic. Il n'existe aucun traitement curatif, et les quelques médicaments approuvés par la FDA n'offrent qu'un gain de survie modeste. Cependant, comme le montre l'histoire de Todd ( dont la volonté de prouver l'efficacité du DMSO en l'interrompant à plusieurs reprises, puis en documentant l'aggravation rapide des symptômes qui s'en est suivie) : il y a de l'espoir pour la SLA. Par ailleurs, certaines recherches viennent corroborer cette hypothèse.
• Chez des souris modèles de SLA, l’administration orale à long terme de 5 % de DMSO a significativement augmenté la durée de survie moyenne, réduit les scores neurologiques et amélioré les performances motrices (ces améliorations étant principalement fonctionnelles plutôt qu’histologiques). 1 , 2
• De faibles concentrations de DMSO ont permis de stabiliser la conformation de la protéine SOD1 (un mauvais repliement de la SOD1 étant une cause majeure de la SLA). De plus, la 5-fluorouridine et l'épigallocatéchine gallate ( souvent associée au DMSO) ont également stabilisé la SOD1.
Divers agents, en association avec le DMSO, ont également démontré un bénéfice thérapeutique chez des souris atteintes de SLA. L'administration intrapéritonéale chronique de resvératrol a retardé l'apparition de la maladie, prolongé la survie et préservé près de deux fois plus de motoneurones. Un inhibiteur de GSK-3β a retardé l'apparition de la maladie et le décès, et a partiellement préservé les motoneurones lombaires. Les inhibiteurs d'ASK1 ont protégé les motoneurones contre la mort et réduit l'activation gliale. La rapamycine a amélioré l'équilibre neuroprotecteur entre fission et fusion mitochondriales. Le lycopène a réduit , de manière dose-dépendante, le stress oxydatif et l'apoptose des motoneurones. Notamment, le carboxyamidotriazole a inhibé fortement les cytokines inflammatoires in vitro, mais n'a pas amélioré significativement l'apparition de la maladie ni la survie par rapport au groupe témoin (DMSO) in vivo, ce qui suggère que le DMSO seul procure déjà un bénéfice comparable.
Remarque : Le DMSO a également été associé au riluzole (l’un des rares médicaments contre la SLA) pour traiter diverses autres affections neurologiques, notamment les douleurs neuropathiques 1,2 , la dégénérescence rétinienne photo-induite 1,2 ,la perte auditive (pour laquelle le DMSO seul s’est également révélé protecteur de l’audition et préservant les neurones cochléaires) et l’état de mal épileptique – autant d’affections pour lesquelles le DMSO est efficace. De plus, il a été utilisé comme solvant pour le criblage d’un grand nombre de composés en vue de leur utilisation dans le traitement de la SLA.
Outre la remarquable réponse de Todd au DMSO topique et surtout intraveineux, quelques autres témoignages suggèrent que le DMSO pourrait être bénéfique pour la SLA et les affections apparentées. Un ouvrage relate le cas de Stanley Jacob traitant un patient atteint de SLA avec du DMSO, obtenant des « miracles thérapeutiques instantanés, immédiats et légèrement différés » (après quoi le médecin a interdit tout traitement ultérieur).
Remarque : Je soupçonne que ce cas ait initialement incité un mentor à essayer le DMSO intraveineux pour la SLA.
Une autre lectrice a rapporté qu'une collègue avait administré du DMSO à son père atteint de SLA et avait été « surprise de constater une nette amélioration de son état ». Enfin, un lecteur souffrant du syndrome de fasciculations spasmodiques (une affection dont les symptômes ressemblent à ceux de la SLA à un stade précoce, mais qui n'évolue pas vers cette maladie) a décrit comment, poussé par la combinaison de douleurs chroniques et d'insomnies sévères, il avait envisagé le suicide avant de découvrir que le DMSO par voie orale améliorait considérablement l'efficacité de ses autres médicaments, lui permettant de dormir toute la nuit, éliminant en grande partie ses crampes et ses douleurs nerveuses, et lui redonnant la capacité de travailler et de voir grandir ses enfants.
Remarque : notre expérience (limitée) montre que le DMSO administré par voie intraveineuse ralentit la progression de la SLA sans toutefois l’inverser. Cependant, les témoignages recueillis suggèrent que certaines personnes présentent une réponse beaucoup plus marquée, que ce soit en raison d’une prédisposition génétique ou de doses intraveineuses plus élevées. Une de mes principales interrogations demeure : les cas de SLA « atypiques » apparus après la vaccination contre la COVID-19 réagissent-ils différemment au DMSO par rapport aux cas de SLA survenus avant la vaccination (dont est issue toute notre expérience) ?
maladie de Huntington
La
maladie de Huntington est une affection génétique fatale caractérisée
par une perte progressive de la motricité, un déclin cognitif et des
troubles psychiatriques. Elle appartient à une famille de neuf maladies
neurodégénératives (maladies à polyglutamine) causées par des protéines
mal repliées présentant des répétitions de glutamine anormalement
longues. Une revue des chaperons chimiques utilisés dans ces maladies a
révélé que le DMSO inhibait la toxicité induite par les polyglutamines
de manière similaire, voire supérieure, à celle des autres chaperons
chimiques testés (glycérol, TMAO). De même, dans des modèles cellulaires de la maladie de Machado-Joseph (une
autre maladie de cette famille), le DMSO a stabilisé le repliement de
la protéine ataxine-3 mutante, réduisant ainsi son agrégation, sa
cytotoxicité et la mort cellulaire.
Dans la seule étude ayant
testé directement l'effet du DMSO sur la maladie de Huntington, le DMSO
(à une concentration d'environ 1 à 4 %) a partiellement prévenu la mort
cellulaire, augmenté la viabilité cellulaire, diminué l'agrégation de
la protéine huntingtine et augmenté sa forme soluble (non toxique).
Divers agents, en association avec le DMSO, ont également démontré un bénéfice thérapeutique dans des modèles de la maladie de Huntington. Chez le rat,l' inosine a protégé contre les symptômes de type Huntington en améliorant la fonction motrice, en activant la voie neurotrophique BDNF/TrkB/ERK/CREB, en augmentant le BDNF striatal et en réduisant le stress oxydatif, la neuroinflammation et les lésions neuronales striatales. L'inhibition de FKBP5 a réduit les taux de huntingtine mutante et augmenté la clairance autophagique dans les cellules souches de patients atteints de la maladie de Huntington et dans des modèles murins. Dans des modèles de la maladie de Huntington chez C. elegans , l'extrait de feuille d'olivier a fortement protégé les neurones de la dégénérescence induite par la polyglutamine (jusqu'à quatre fois plus de neurones intacts) et a amélioré la réponse mécanosensorielle, tandis que le 3-hydroxytyrosol et le tyrosol ont réduit le nombre de plaques de polyglutamine, protégé les neurones et amélioré la réponse mécanosensorielle. Les extraits d'espèces d'Hyptis ⬖ ont également amélioré de manière significative la locomotion et augmenté la résistance au stress oxydatif dans les modèles de polyglutamine.
Remarque : le DMSO a également été utilisé pour cribler un grand nombre de traitements potentiels contre la maladie de Huntington et pour étudier ses mécanismes pathogènes sous-jacents .
maladie d'Alzheimer
La maladie d'Alzheimer (MA), la forme la plus courante de démence, est caractérisée par l'accumulation extracellulaire de plaques amyloïdes β (Aβ) (notamment dans l'hippocampe et le cortex) et d'enchevêtrements neurofibrillaires intracellulaires issus de la protéine tau hyperphosphorylée. On pense qu'elle résulte des lésions que ces protéines causent au tissu cérébral ; de ce fait, la quasi-totalité des recherches sur la maladie s'est concentrée sur l'élimination des plaques amyloïdes.
Remarque : il est possible de démontrer que les protéines amyloïdes protègent initialement les cellules cérébrales des facteurs de stress (par exemple, les toxines), ce qui est étayé par le fait que tous les médicaments éliminant l'amyloïde ont échoué (et ont souvent des effets secondaires importants car ils préparent le système immunitaire à attaquer l'amyloïde et donc à créer une inflammation dans le cerveau), ainsi que par le fait que les thérapies naturelles qui ciblent directement les facteurs endommageant le tissu cérébral sont actuellement le seul traitement de la maladie d'Alzheimer avec des données probantes (discutées plus en détail ici ).
Le DMSO présente une utilité unique dans le traitement de cette maladie, car le DMSO :
•
Stabilise les protéines et élimine les agrégats amyloïdes mal repliés
(permettant ainsi d'éliminer les accumulations amyloïdes dangereuses de
manière non invasive). Par exemple, une étude de modélisation informatique a indiqué que le DMSO inhibe l'agrégation d'Aβ en modulant la stabilité du pont salin Lys28-Ala42, tandis que des simulations de dynamique moléculaire ont
montré que le DMSO favorise la structure en hélice α et stabilise Aβ42
(empêchant la formation de feuillets β à l'origine de l'agrégation
toxique).
• Inhibiteur de l'acétylcholinestérase 1,2
(la même stratégie thérapeutique que celle utilisée par le donépézil et la galantamine, médicaments contre la maladie d'Alzheimer approuvés par la FDA).
• Il a été démontré qu'il
augmente l'activité de la phosphatase alcaline lysosomale (ALP) de 20
%, ce qui favorise probablement l'élimination des agrégats protéiques
toxiques contribuant à la neurodégénérescence.
Remarque : un spray nasal d’insuline à base de DMSO, développé pour le traitement de la maladie d’Alzheimer, a permis , chez le rat, de délivrer l’insuline dans tout le cerveau en une heure sans aucun signe de toxicité. 1,2,3
De plus, les propriétés fondamentales du DMSO (par exemple, l'amélioration de la circulation, la réduction de l'inflammation et la réactivation des cellules « choquées » et dormantes) contrecarrent directement les processus pathologiques à l'origine de la maladie d'Alzheimer. Par exemple, il a été démontré que le DMSO inhibe l'activation des inflammasomes NLRP3 et de la caspase-1, qui sont impliqués dans la neuroinflammation chronique accélérant la progression de la maladie d' Alzheimer . 1,2,3
Remarque : Le DMSO est couramment utilisé en laboratoire pour solubiliser les peptides amyloïdes à des fins expérimentales 1,2,3,4 . Les conditions initiales de solubilisation (notamment l’exposition au DMSO) influencent fortement la reproductibilité de la cinétique d’agrégation d’Aβ . Des études caractérisant la toxicité de différentes espèces d’Aβ (oligomères, protofibrilles, fibrilles) et fractions de poids moléculaire ont utilisé le DMSO pour la préparation des peptides<sup>1,2</sup>. Le DMSO a également servi de solvant pour le criblage de cocktails de médicaments anti-âge contre la neurotoxicité d’Aβ et de la protéine tau dans des lignées cellulaires neuronales.
Dans les études animales, le DMSO a démontré à plusieurs reprises des bénéfices cognitifs directs dans les modèles de la maladie d'Alzheimer :
Chez des rats ayant reçu des perfusions intracérébroventriculaires de streptozotocine (STZ) pour modéliser la maladie d'Alzheimer sporadique, l'administration quotidienne de DMSO par voie intraveineuse pendant deux semaines a permis de contrer les troubles de la mémoire, améliorant ainsi les performances aux tests comportementaux et mnésiques. Ces résultats ont été corroborés par une étude montrant qu'une administration intracérébroventriculaire chronique de DMSO à 10 % (mais pas à 2,5 % ni à 5 %) atténuait significativement les déficits de mémoire spatiale induits par la STZ dans le labyrinthe aquatique de Morris. Les auteurs attribuent ce bénéfice aux propriétés antioxydantes, anti-inflammatoires et d'amélioration de la perfusion cérébrale du DMSO.<sup> 1,2 </sup> Dans une autre étude sur la STZ , une équipe distincte a observé des tendances similaires : diminution de la neuroinflammation (IL-1β, TNFα), améliorations comportementales et augmentation du BDNF suite au traitement par DMSO.
Chez des rats modèles de la maladie d'Alzheimer ayant reçu une injection d'Aβ25-35 dans l'hippocampe, le DMSO a amélioré l'apprentissage et la mémoire, réduisant le temps de latence pour s'échapper et la distance de recherche dans le labyrinthe aquatique de Morris. Notamment, aucun effet synergique significatif n'a été observé lorsque le DMSO était combiné à un extrait de Ginkgo biloba, ⬖ suggérant que le DMSO seul exerçait déjà un effet substantiel. Dans une étude similaire , le DMSO et l'extrait de Ginkgo biloba ⬖ ont chacun amélioré l'apprentissage et la mémoire chez des rats modèles de la maladie d'Alzheimer avec injection d'Aβ25-35, avec des effets associés à la modulation de l'expression de l'APP hippocampique.
De plus, chez des souris génétiquement modifiées pour développer la maladie d'Alzheimer , le DMSO a augmenté la densité des épines dendritiques de manière spécifique à certaines régions de l'hippocampe, amélioré la précision de la mémoire spatiale, modulé l'habituation olfactive et présenté un effet anxiolytique. Malgré ces améliorations observées chez des animaux présentant des taux élevés d'Aβ, le DMSO n'a pas réduit les espèces oligomériques d'Aβ et semble plutôt agir par modulation de la signalisation des récepteurs NMDA (l'antagoniste NMDA MK-801 reproduisant l'effet du DMSO sur la densité des épines dendritiques). Les auteurs en concluent : « Le DMSO doit être considéré comme un véritable composé bioactif, susceptible d'être un adjuvant bénéfique pour contrer la synaptotoxicité et les troubles comportementaux induits par l'Aβ. »
Dans une étude distincte sur la maladie d'Alzheimer chez la souris, le DMSO a traversé indépendamment la barrière hémato-encéphalique, amélioré la cognition et réduit la neuroinflammation — des effets observés même si l'étude était conçue pour tester la serpina3n, et non le DMSO lui-même.
Chez de jeunes souris (3 à 4 mois) génétiquement modifiées pour développer une MA précoce, 0,01 % de DMSO mélangé à de l'eau de boisson a atténué les baisses de vision et l'épaississement rétinien observés dans la phase prodromique de la MA (avec des avantages comparables au R-carvédilol), indiquant que le DMSO améliorait le transport de l'eau hors des yeux, dépendant de l'énergie.
Chez C. elegans, le DMSO a considérablement retardé (de 48 à 98 %) la paralysie induite par Aβ42 et a prolongé la durée de vie de 23,0 à 24,4 %. <sup>1,2 </sup> Les chercheurs ont attribué ce retard de la paralysie à la modulation de la neurotransmission par le DMSO , notant que ce dernier réduisait la paralysie induite par des agents liés à l'acétylcholine d'environ 70 % et que cette protection dépendait de la voie de longévité daf-16/FOXO.
En culture cellulaire, de faibles concentrations de DMSO ( 0,015625–0,0625 %)
ont augmenté la viabilité des cellules cérébrales et masqué la toxicité
de l'Aβ (concentrations facilement atteignables dans le tissu cérébral
suite à la prise de DMSO à domicile ou à son utilisation courante dans
les expériences cellulaires).
Remarque :
étant donné l'utilisation fréquente du DMSO dans la recherche sur la
maladie d'Alzheimer, il a été suggéré à plusieurs reprises que cet effet
protecteur a probablement contribué à surestimer l'efficacité des
thérapies qui y sont associées et à sous-estimer la neurotoxicité des
particules amyloïdes. <sup> 1,2 </sup>
De plus, le DMSO a modifié l'épissage de la protéine précurseur de l'amyloïde (APP) dans l'hippocampe du rat adulte, favorisant l'isoforme neurotrophique APP-695 (dont la proportion est passée de 89 % à 94 %), tout en réduisant les isoformes pathologiques contenant le motif KPI (APP-751/770), généralement élevées dans la maladie d'Alzheimer (soulignant une fois de plus son utilité dans cette pathologie). Dans un modèle murin de traumatisme crânien par impact cortical contrôlé, le DMSO (utilisé comme excipient du glibenclamide) a démontré des effets bénéfiques indépendants et inattendus chez les souris femelles, en diminuant significativement l'expression des protéines pathologiques TAU et TDP43 dans plusieurs régions cérébrales et en contribuant à la restauration du débit sanguin cérébral (effets que les auteurs de l'étude ont qualifiés de novateurs).
Une étude japonaise des années 1980 notait que le DMSO avait été exploré pour dissoudre les dépôts amyloïdes dans la maladie d'Alzheimer, un rapport faisant état d'une amélioration partielle de la fonction motrice.
Études humaines
Dix-huit patients présentant des symptômes probables de la maladie d'Alzheimer ont été traités en Moldavie avec du DMSO et suivis régulièrement pendant neuf mois. Des améliorations significatives ont été observées dès le troisième mois de traitement, et sont devenues particulièrement marquées après six mois. Ces améliorations concernaient la mémoire, la concentration et la communication, ainsi qu'une diminution significative de la désorientation spatio-temporelle.
De même, selon Jack De La Torre ,
chercheur de premier plan sur les applications neurologiques du DMSO :
« Le diméthylsulfoxyde, un puissant piégeur de radicaux libres connu
pour augmenter le débit sanguin cérébral, tant cliniquement
qu’expérimentalement, dans divers états pathologiques cérébraux, a
démontré améliorer les fonctions cognitives tout en stabilisant les
enzymes protéiques chez les patients atteints de la maladie d’Alzheimer
traités avec ce médicament pendant six mois. »
Remarque : Je n’ai pas pu déterminer si De La Torre faisait référence à l’étude moldave ou à une autre étude.
Études combinées dans les modèles de la maladie d'Alzheimer
De nombreuses recherches ont évalué des agents thérapeutiques dissous dans du DMSO dans différents modèles de la maladie d'Alzheimer.
Traitement de l'APP et modulation de la sécrétase
Divers agents dissous dans du DMSO ont démontré leur capacité à orienter le traitement de l'APP vers une production réduite d'Aβ toxique. L'extrait d'écorce de cannelle ⬖ a réduit la production d'Aβ40 de 50 à 60 % grâce à ses composés actifs, le médiorésinol et la cryptamygine A, qui ont diminué les niveaux de β-sécrétase. Le lévistolide A ⬖ (issu de Danggui-Shaoyao-San) a réduit l'Aβ1-42 extracellulaire dans les cellules de patients atteints de la maladie d'Alzheimer et a démontré sa capacité à traverser la barrière hémato-encéphalique, atteignant des concentrations cérébrales maximales en 30 minutes. L'apicidine (un inhibiteur d'HDAC) a augmenté l'expression d'ADAM10 (α-sécrétase) via la signalisation USF1 et ERK, orientant ainsi le clivage de l'APP vers une voie moins amyloïdogène. L'acide rétinoïque inhibe l'activité de la γ-sécrétase par l'activation d'ERK, tandis que les modulateurs de la γ-sécrétase à base de sulfamides modifient les ratios Aβ40/42 sans les effets secondaires liés à Notch associés à une inhibition complète de la γ-sécrétase. De plus, plusieurs inhibiteurs de la BACE1 dissous dans du DMSO réduisent la production d'Aβ1-40 et d'Aβ1-42 dans les cellules neuronales (mais, comme d'autres médicaments anti-amyloïdes, ils échouent lors des essais cliniques ultérieurs). Le DMSO est également utilisé pour dissoudre l'acide ursolique , identifié par criblage à haut débit comme un puissant inhibiteur de la liaison d'Aβ au récepteur CD36, bloquant ainsi la production d'espèces réactives de l'oxygène par la microglie.
Souris transgéniques AD
Les combinaisons de DMSO ont été largement étudiées chez des souris transgéniques atteintes de la maladie d'Alzheimer. La dihydromyricétine a amélioré les performances dans le labyrinthe aquatique de Morris, diminué l'accumulation d'Aβ et les plaques séniles, et restauré le flux autophagique en augmentant la Becline 1 et le rapport LC3-II/LC3-I, et en réduisant la P62. De nombreux inhibiteurs de l'HDAC6 ont atténué le déclin cognitif, réduit les taux d'Aβ et le dépôt de plaques, diminué la protéine tau hyperphosphorylée, stimulé l'expression des protéines d'autophagie et protégé les neurones corticaux des dommages oxydatifs. Un inhibiteur de la p38 MAPK a amélioré la cognition en réduisant l'Aβ, la phosphorylation de la protéine tau, la BACE1 et la préséniline , tout en augmentant les protéines synaptiques et les protéines dégradant l'amyloïde. L'astragaline a amélioré l'apprentissage spatial et la mémoire chez la souris en réduisant le dépôt de plaques d'Aβ et en stimulant le flux autophagique via la voie PI3K/Akt-mTOR. Le ligustilide a amélioré l'apprentissage et la mémoire, favorisé le transport et l'élimination de l'Aβ et réduit la neuroinflammation. Le blocage chronique du canal TRPA1 a normalisé l'activité astrocytaire, prévenu le dysfonctionnement neuronal, préservé l'intégrité synaptique et empêché le déclin de la mémoire de travail spatiale. La kenpaullone a amélioré les performances cognitives et réduit les plaques Aβ, la neurodégénérescence et les cytokines pro-inflammatoires, tandis que l'erlotinib a amélioré la mémoire spatiale à court terme, augmenté la formation d'épines dendritiques et réduit la phosphorylation et l'agrégation de la protéine tau.
Parmi les agents ciblant l'élimination ou la réduction de l'Aβ, de nouveaux inhibiteurs de c-KIT ont amélioré l'élimination autophagique de l'Aβ et de la protéine tau, l'ériodictyol a favorisé l'élimination de l'Aβ par la microglie, le menthol a inhibé la polymérisation de l'Aβ et réduit les plaques séniles, et la picropodophylline a réduit l'Aβ et la microgliose hippocampique, tandis que l'acide ellagique a réduit à la fois l'Aβ et la caspase-3. Le GTM-1, la rapamycine et la carbamazépine ont chacun amélioré la mémoire spatiale et réduit l'Aβ42 (le GTM-1 activant l'autophagie via mTOR).
Parmi les agents améliorant la fonction synaptique et la cognition, un inhibiteur de JNK a réduit l'inflammation, restauré les protéines synaptiques et amélioré la cognition ; un inhibiteur de PDE4 a amélioré la mémoire, la plasticité synaptique et la signalisation hippocampique ; le CA140 a restauré la mémoire et la fonction synaptique via la signalisation dopaminergique D1 ; la puérarine a restauré l'activité des récepteurs NMDA ; et l' isoliquiritigénine a rétabli l'équilibre synaptique excitation/inhibition. Un activateur de SERCA a amélioré la mémoire et la coordination motrice, tandis que le clenbutérol a augmenté l'expression de PSA-NCAM et amélioré la cognition.
D'autres agents agissant par neuroprotection, neurogenèse ou modulation immunitaire comprennent un agoniste LXR (qui a favorisé la neurogenèse et augmenté l'apoE), un agoniste CB2R (qui a fait passer la microglie de M1 à M2 anti-inflammatoire), l'idébénone (qui a amélioré la mémoire spatiale et la fonction mitochondriale), un agoniste du récepteur bêta des œstrogènes et la berbérine ⬖ (qui a réduit l'apoptose de manière dose-dépendante et augmenté l'expression de Bcl-2 dans les neurones de l'hippocampe).
Modèles AD sporadiques
Les modèles de maladie d'Alzheimer sporadique (utilisant la streptozotocine intracérébroventriculaire) ont également répondu aux thérapies combinées. Un dérivé de triazine a amélioré l'apprentissage spatial et augmenté l'épaisseur de la couche pyramidale de l'hippocampe ; la canagliflozine a amélioré la morphologie dendritique ; l' extrait de Croton hirtus ( MECH) a inversé les troubles de l'apprentissage et de la mémoire tout en réduisant les taux d'Aβ et d'AChE ; et la rapamycine a réduit la protéine tau hyperphosphorylée et la signalisation mTOR. L' inhibiteur de MIF, l'ISO-1, a amélioré la mémoire contextuelle dépendante de l'hippocampe et réduit la production de cytokines, les taux de MIF étant élevés dans le liquide céphalo-rachidien de patients atteints de la maladie d'Alzheimer à un stade précoce. L' inhibiteur de GSK-3β, le SB216763, a atténué la réponse au stress du réticulum endoplasmique (UPR) induite par la tunicamycine, les altérations synaptiques et les déficits de mémoire.
Modèles d'injection aiguë d'Aβ
Des modèles d'injection aiguë d'Aβ ont été utilisés pour tester un large éventail d'agents. L'extrait de Piper kadsura ohwi a significativement amélioré les déficits éthologiques induits par les oligomères et les fibrilles d'Aβ, tout en réduisant la neuroinflammation via la voie TLR4/NF-κB/TNF-α. <sup> 1,2 </sup> La rapamycine a amélioré les fonctions cognitives, réduit les dépôts d'Aβ dans l'hippocampe et augmenté l'expression d'Homer3. La testostérone a inversé les déficits d'apprentissage spatial et la perte neuronale via la voie de signalisation BDNF/CaMKII/CREB (un effet totalement bloqué par le flutamide, un antagoniste des récepteurs aux androgènes). La curcumine dissoute dans du DMSO a partiellement amélioré l'apprentissage spatial chez des rats modèles de la maladie d'Alzheimer et a également inversé les dommages induits par l'Aβ sur les cellules souches neurales, améliorant ainsi leur viabilité et les marqueurs de différenciation (Nestin, Tuj-1, GFAP). 1 , 2 , 3 La pioglitazone a inversé de manière dose-dépendante l'activation de MKK4, JNK1 et c-Jun induite par Aβ1-42 dans l'hippocampe du rat, la plupart des immunoréactivités p-JNK étant colocalisées avec la microglie.
D'autres agents qui ont amélioré la cognition ou réduit la pathologie de la maladie d'Alzheimer dans les modèles injectés avec Aβ comprennent l'extrait d'Angelica keiskei ⬖ (qui a amélioré la mémoire de manière dose-dépendante), la génistéine à faible dose ⬖ (qui a régulé positivement STAT3 et supprimé la caspase-3), l'acide bétulinique ⬖ (qui a amélioré la mémoire, l'anxiété et la LTP), le DL0410 (un inhibiteur double de l'AChE/BChE qui a amélioré l'apprentissage via CREB/BDNF), l'extrait de feuille de B. pendula ⬖ (qui a réduit le stress oxydatif et la signalisation NF-κB), la décoction Huanglian Jiedu ⬖ (qui a réduit l'activation microgliale), un inhibiteur de DAPK1 (qui a réduit l'activation de l'inflammasome NLRP3 et amélioré les déficits de mémoire) et l'atorvastatine (qui a prévenu la synaptotoxicité et la neuroinflammation via l'inhibition de la p38 MAPK). La biochanine A ⬖ a atténué la mort neuronale induite par Aβ et amélioré l'apprentissage spatial via l'inhibition de la p38 MAPK dépendante du récepteur des œstrogènes, tandis que la fraction hexane de Perilla frutescens ⬖ a inhibé l'agrégation d'Aβ et protégé les cellules de la toxicité d'Aβ, tout comme un peptide briseur de feuillet bêta conçu à cet effet .
D'autres agents présentant des effets neuroprotecteurs dans des modèles cellulaires Aβ incluent les alcaloïdes de Dendrobium nobile ⬖ (qui augmentent la survie cellulaire), la neuroprotectine D1 (qui réduit l'Aβ42, la phosphorylation de la protéine tau et l'apoptose tout en stimulant l'autophagie), la curcumine ⬖ (qui réduit les ROS mitochondriales, stimule l'autophagie via les protéines Rab et augmente le transport axonal), 1 , 2 , 3 l'icariine ⬖ (qui inhibe l'autophagie et réduit la production d'Aβ via p70 S6K), un inhibiteur de la DPP-4 (qui active la voie PI3K/Akt/GSK-3β et réduit la phosphorylation de la protéine tau), le férulate de sodium ⬖ (qui protège les neurones de l'hippocampe via la modulation de la voie Notch), le butylphtalide (qui protège les cellules endothéliales de l'apoptose induite par l'Aβ via TLR4/COX-2), 1 , 2 et le ZL006 (qui active la voie PI3K/Akt/GSK-3β). Akt/Nrf2/HO-1), MS-275 et JQ1 (qui ont amélioré la mémoire via CREB et réduit le TNF-α), la pioglitazone (qui a réduit l'Aβ et la protéine tau via l'activation de PPARγ), le glucoside de tétrahydroxystilbène ⬖ (qui a réduit l'inflammation microgliale et l'expression d'APOE/TREM2), la berbérine ⬖ (qui a favorisé la polarisation M2 microgliale via la signalisation PI3K-AKT, protégeant les neurones des lésions induites par l'Aβ), et l'inhibition du récepteur 5-HT1B (qui a restauré la phosphorylation de l'eNOS et de l'Akt perturbée par l'Aβ1-42 dans les cellules endothéliales humaines, suggérant que ce récepteur est impliqué dans le dysfonctionnement vasculaire induit par l'Aβ pertinent pour la MA).
Modèles d'acide okadaïque (OA)
Les modèles d'acide okadaïque (qui induisent une hyperphosphorylation de la protéine tau en inhibant la protéine phosphatase 2A) ont également répondu aux thérapies administrées par DMSO. La décoction de Trillium tschonoskii a amélioré l'apprentissage spatial, augmenté l'activité de la PP2A et réduit la phosphorylation de la protéine tau tout en préservant les neurones de l'hippocampe. La décoction de Banqiao Codonopsis pilosula a amélioré la cognition de manière dose-dépendante, réduit l'hyperphosphorylation de la protéine tau et augmenté les protéines synaptiques et le nombre d'épines dendritiques. <sup> 1,2 </sup> Chez le poisson-zèbre, la mansonone G a inversé les déficits cognitifs induits par l'acide okadaïque, améliorant la mémoire spatiale et de reconnaissance et restaurant la fonction cholinergique. Les agents supplémentaires comprennent le ginsénoside Rb1 ⬖ (qui atténue l'hyperphosphorylation de la protéine tau), le ginkgolide ⬖ combiné à l'insuline (qui améliore de manière synergique l'apprentissage et réduit les enchevêtrements neurofibrillaires), le polypeptide de bois de cerf pilose ⬖ (qui active PI3K/AKT et réduit l'apoptose) et la sarsasapogénine ⬖ (qui atténue l'hyperphosphorylation de la protéine tau via Akt/GSK-3β).
Pathologie Tau
Plusieurs découvertes concernent directement la protéine tau, un facteur clé de la neurodégénérescence dans la maladie d'Alzheimer :
Chez des souris femelles ayant subi un traumatisme crânien, le DMSO a réduit indépendamment les protéines TAU et TDP43 pathologiques dans plusieurs régions cérébrales, un effet comparable à celui du glibenclamide. L'EGTA (un chélateur de calcium) a diminué la phosphorylation de la protéine tau en Ser396 chez des souris atteintes de la maladie d'Alzheimer en réduisant l'expression de la calpaïne 2 et de CDK5. Le resvératrol a réduit l'hyperphosphorylation de la protéine tau induite par le cadmium via l'activation de la voie AMPK/PI3K/Akt, et a également réduit l'acétylation et la phosphorylation de la protéine tau chez des rats âgés présentant un dysfonctionnement cognitif postopératoire en activant SIRT1 et en induisant une transition du phénotype microglial de M1 à M2a. L' acide docosahexaénoïque administré après un traumatisme crânien a réduit l'accumulation de protéine tau phosphorylée et d'APP. L'inhibition de l'UCH-L1 a bloqué la formation d'agrégats de protéine tau en réduisant les chaînes d'ubiquitine liées à K63 et en altérant la liaison HDAC6-tau.
Chez C. elegans (souches AD), l'extrait de chanvre ⬖ (contenant à la fois des cannabinoïdes et des terpènes, dispersés dans du DMSO) a augmenté de manière significative la durée de vie des nématodes modèles tau, le CBD ⬖ empêchant directement la formation d'agrégats protéiques.
Stress oxydatif
L'ester éthylique de l'acide férulique , administré par voie intrapéritonéale dans du DMSO, a protégé les synaptosomes du cerveau de gerbille des dommages oxydatifs induits par Aβ, en réduisant les espèces réactives de l'oxygène, l'oxydation des protéines et la peroxydation lipidique, tout en stimulant les défenses antioxydantes (HO-1, HSP72) et en réduisant l'iNOS. L' astaxanthine a amélioré les performances cognitives de manière dose-dépendante, réduit l'accumulation d'Aβ42 et de malondialdéhyde, inhibé les activités de l'AChE et de la MAO et augmenté l'expression de Nrf2 et de miR-124. Chez la souris , le DMSO a réduit les ROS cérébrales de 9,8 à 79 % (effet maximal chez les jeunes souris) et les dommages oxydatifs irréversibles aux protéines de 30,7 à 69 % (effet maximal chez les souris âgées) ; ces effets bénéfiques ont été potentialisés par la curcumine. ⬖ Chez les rats, l'inhibition de SIRT2 a réduit le stress oxydatif, augmenté l'activité anti-apoptotique de bcl-2 et élevé le régulateur de l'autophagie beclin-1 dans le cortex et l'hippocampe, tandis que la mélatonine ⬖ et la curcumine ⬖ ont chacune réduit la peroxydation lipidique et l'expression de SIRT2 et augmenté Nrf2 et les défenses antioxydantes dans le cortex cérébral (bien que sans effet synergique lorsqu'elles sont combinées).
Le MSM ⬖ (métabolite oxydé du DMSO) a amélioré la neurodégénérescence induite par la co-exposition au BPA et aux radiations, réduisant les marqueurs de la MA (Aβ42 de 71,6 %, AChE d'environ 50 %, phosphorylation de tau de 57 %), stimulant le BDNF (132–160 %), supprimant la voie TREM-2/DAP12 et réduisant les plaques Aβ d'environ 75 %.
Remarque : Le MSM traverse rapidement la barrière hémato-encéphalique (détectable en ~10 minutes après ingestion orale), atteignant des concentrations cérébrales d’environ 2,36 mM après supplémentation orale, avec une demi-vie d’environ 7,5 jours. <sup> 1,2 </sup>
Inhibition de l'AChE et criblage de médicaments
Outre le fait que le DMSO soit lui-même un inhibiteur de l'AChE, divers inhibiteurs de l'AChE ont été testés dans le DMSO pour leur pertinence dans le contexte de la maladie d'Alzheimer. De nouveaux dérivés de tacrine-acide hydroxamique ont montré une puissante double inhibition de l'AChE et de l'HDAC, associée à une inhibition de l'Aβ, tandis que les inhibiteurs à base de thiazole se sont révélés plus performants que la rivastigmine et l'huperzine A. Parmi 21 flavonoïdes testés, la galangine a présenté la plus forte inhibition de l'AChE cérébrale (IC50 ~120 μM). Un autre criblage a permis d'identifier une sonde multifonctionnelle qui, en présence de DMSO, se liait aux agrégats d'Aβ, inhibait la cholinestérase et améliorait la mémoire cognitive et spatiale.
Composés naturels et organismes modèles
De nombreux composés naturels dissous dans du DMSO ont démontré des effets neuroprotecteurs dans des modèles de la maladie d'Alzheimer. Chez C. elegans, l'extrait de feuille d'olivier a fortement protégé les neurones de la dégénérescence induite par Aβ, tandis que le 3-hydroxytyrosol, le tyrosol, le safran, Polygonum multiflorum et Ziziphus jujuba ont également procuré une protection significative. Le cannabidiol a prolongé la durée de vie et ralenti la détérioration neuronale liée à l'âge chez C. elegans, et a amélioré la croissance des neurites et la densité des épines dendritiques dans les neurones de mammifères via la même voie SIRT1. La quercétine et la rifampicine ont réduit individuellement les plaques Aβ, leur combinaison permettant l'élimination la plus importante. La quercétine et le kaempférol ( polyphénols isolés de cultures cellulaires de Ginkgo biloba) ont réduit, de manière dose-dépendante, la carbonylation des protéines chez C. elegans, un marqueur clé des dommages protéiques liés au vieillissement et associés aux maladies neurodégénératives. Des hybrides d'oxoisoaporphine et d'acide lipoïque ont amélioré l'apprentissage, la mémoire, la durée de vie et l'inhibition de l'AChE chez la drosophile transgénique Aβ42. Chez le poisson-zèbre, des antagonistes des récepteurs purinergiques (caféine, ZM241385, DPCPX) ont prévenu les troubles de la mémoire induits par la scopolamine.
Dans des modèles cellulaires et animaux, le carvacrol a protégé les neurones de la neurotoxicité induite par Aβ et amélioré la mémoire chez les rats atteints de la maladie d'Alzheimer (MA)<sup> 1,2 </sup> . Les withanolides dérivés de l'ashwagandha ont restauré la longueur des axones et des dendrites ainsi que les marqueurs synaptiques dans les neurones lésés par Aβ et ont inversé les déficits de mémoire après administration orale. Les extraits de <i>Cynarae folium </i> ont présenté des effets neuroprotecteurs contre Aβ dans les cellules et chez les rats, tandis que chez les mouches résistantes aux médicaments, l'anle138b a significativement prolongé la survie. L'extrait de <i>Ptychopetalum olacoides</i> a inversé l'amnésie induite par le MK-801, suggérant l'implication du système glutamatergique dans ses propriétés d'amélioration cognitive.
D'autres composés naturels présentant des effets anti-Aβ incluent la curcumine ⬖ 1 , 2 (qui supprime la signalisation HMGB1/RAGE/NF-κB microgliale), la bisdéméthoxycurcumine ⬖ , les polyphénols de Ginkgo biloba ⬖ (qui protègent les cellules dPC12 des dommages causés par Aβ), Perilla frutescens ⬖ (qui désagrège les agrégats Aβ préformés), l'icariine ⬖ (qui réduit l'iNOS et le TNF-α et améliore la cognition chez les souris AD induites par LPS), divers extraits de germes comestibles ⬖ 1 , 2 , 3 (les germes de sarrasin ⬖ présentant la plus forte suppression des ROS et la plus forte réduction d'Aβ), et la curcumine ⬖ (qui, en se liant à l'amyloïde, a permis la détection in vivo de l'amyloïde rétinienne chez des souris AD transgéniques vivantes par ophtalmoscopie confocale, démontrant ainsi le potentiel de Le diagnostic non invasif de la maladie d'Alzheimer), ainsi que les polyphénols acide nordihydroguaïarétique, ⬖ baicaléine, ⬖ et extrait de Padina ⬖ (qui protègent les cellules des dommages induits par Aβ42). La curcumine ⬖ dissoute dans du DMSO a également atteint une solubilité sérique élevée (au moins 3 mM), inhibant efficacement la formation de plaques Aβ.
Modèles de la maladie d'Alzheimer liés au vieillissement
L'injection de D-galactose induit un vieillissement accéléré chez les rongeurs, modélisant ainsi le déclin cognitif lié à l'âge. Le Guilingji ⬖ (une formule traditionnelle) a significativement amélioré les performances au labyrinthe aquatique de Morris chez les rats vieillis par le D-galactose, restaurant l'activité antioxydante et normalisant les neurotransmetteurs. L'extrait de Ganoderma tsugae ⬖ a amélioré la locomotion, l'apprentissage et la mémoire en augmentant les enzymes antioxydantes cérébrales et le BDNF, tout en réduisant l'activation de l'inflammasome. La Kurarinone ⬖, combinée à des exercices de rééducation, a amélioré de façon synergique l'apprentissage spatial et la mémoire, a régulé à la hausse les marqueurs de plasticité synaptique (PSD-95, synaptophysine) et a réduit le dépôt d'Aβ1-42 via la voie BACE1/Aβ. Le resvératrol ⬖ a significativement augmenté la SOD et diminué les dommages oxydatifs dans les neurones de l'hippocampe de souris présentant un vieillissement induit par le D-galactose. La curcumine ⬖ a réduit l'expression de l'APP et de la protéine tau et a supprimé l'activité de la HAT chez les rats atteints de la maladie d'Alzheimer. L’artémisinine ⬖ a également démontré des effets neuroprotecteurs dans un modèle animal de prévention de la MA.
Le chlorure d'aluminium, qui induit l'accumulation de plaques Aβ et la phosphorylation de la protéine tau, a été neutralisé par un dérivé du bithiophene qui a restauré les défenses antioxydantes, prévenu la perte neuronale et synaptique et atténué la pathologie liée à la maladie d'Alzheimer. <sup> 1,2 </sup>
Démence vasculaire
La démence vasculaire (VaD) résulte d'une hypoperfusion cérébrale chronique qui provoque des lésions neuronales progressives et un déclin cognitif, ce qui rend le DMSO bien adapté à cette affection.
Deux inhibiteurs de la p38 MAPK dissous dans du DMSO ont amélioré de façon répétée l'apprentissage spatial et la mémoire chez des rats atteints de démence vasculaire induite par occlusion bilatérale des artères carotides, en réduisant l'apoptose hippocampique, en prolongeant la survie et en diminuant la phosphorylation de la p38 MAPK. <sup> 1,2,3 </sup> La curcumine dissoute dans du DMSO a amélioré de façon dose-dépendante l'apprentissage et la mémoire chez ces mêmes rats, en réduisant la pathologie hippocampique et en favorisant l'efflux de cholestérol cérébral via la voie LXR/RXR-ABCA1-apoA1. 1 , 2 , 3 La paeoniflorine ⬖ a amélioré l'apprentissage et la mémoire chez les rats VaD en réduisant les cytokines pro-inflammatoires et en induisant une polarisation microgliale de M1 à M2 via le récepteur cannabinoïde de type 2. L'inhibition de la cathepsine B a réduit les anomalies mitochondriales, l'apoptose neuronale, la neuroinflammation et le dysfonctionnement cognitif après une occlusion transitoire de l'artère cérébrale moyenne.
Parmi les agents supplémentaires améliorant la cognition dans les modèles de démence vasculaire, on retrouve l'andrographolide ⬖ (qui réduit l'apoptose hippocampique et augmente l'expression de Bcl-2), la PGE1 (qui améliore l'apprentissage et la mémoire via la voie BDNF/TrkB), l'eskétamine (qui augmente l'expression de BDNF, ERK et Nrf2), le tripchlorolide ⬖ (qui réduit l'expression d'Aβ, NF-κB et COX-2), l'IGF-1 (qui améliore la cognition via Akt/mTOR), l'érythropoïétine recombinante par voie intranasale (qui améliore le temps de latence d'échappement et préserve les neurones hippocampiques), la formule Shenmayizhi ⬖ (qui augmente l'expression des protéines synaptiques et du VEGF), le resvératrol avec activation de SIRT1 (qui améliore la cognition et renforce la capacité antioxydante dans l'ischémie cérébrale chronique), l'inhibiteur d'HDAC composé 13 (qui active les isoformes de BDNF et module la signalisation du récepteur AMPA), et la rapamycine (qui inverse la suppression de l'autophagie médiée par mTOR, réduisant ainsi l'expression de BDNF et d' ERK, et la VEGF). L’accumulation d’Aβ et l’hyperphosphorylation de la protéine tau chez les rats diabétiques après une chirurgie orthopédique ont été observées, de même que l’ émodine (qui a réduit la production d’espèces réactives de l’oxygène et inhibé la prolifération néointimale dans la sténose de l’artère carotide). La quercétine a également atténué la démyélinisation de l’hippocampe dans un modèle de sténose bilatérale des artères carotides.
Remarque : la perte de molaires (extraction de dents) chez les rats atteints de démence vasculaire a aggravé les troubles cognitifs et augmenté l'apoptose de l'hippocampe et l'expression d'iNOS/p38 MAPK/NF-κB ; un inhibiteur de p38 MAPK dans du DMSO a réduit ces effets, illustrant que la santé dentaire a un impact sur le déclin cognitif cérébrovasculaire.
Le DMSO a également été utilisé pour différencier les cellules souches mésenchymateuses de la moelle osseuse (BMSC) en cellules de type neuronal exprimant des marqueurs neuronaux (en utilisant un milieu DMSO/BHA à 2 %), qui ont ensuite été transplantées dans le cerveau de rats atteints de VaD, et les BMSC ont favorisé la récupération d'un modèle cellulaire de la maladie d'Alzheimer en régulant à la hausse le PDGF-BB via la voie PI3K/AKT.
Rapports des lecteurs
L'épouse de mon oncle souffre de démence et est aphasique depuis plus d'un an. Ma mère leur a récemment rendu visite et leur a parlé du DMSO. Mon oncle a commencé à lui en administrer par voie orale. Au bout de deux semaines, elle a recommencé à parler.
J'ai lu l'article et j'ai commencé à en donner à ma mère de 93 ans, mélangée à son jus, tous les matins fin novembre. Elle souffre d'une forme de démence depuis plus de 15 ans. Ces derniers temps, elle souffrait beaucoup du syndrome crépusculaire et avait du mal à suivre les instructions. Depuis qu'elle prend du DMSO, ce syndrome a disparu. Elle est plus alerte, elle peut communiquer et rire avec nous. Sa personnalité est revenue. Elle comprend quand je lui demande d'aller aux toilettes. Ses capacités cognitives se sont améliorées et elle a recommencé à colorier dans ses livres.
J'apprécie énormément vos publications sur le DMSO . Vous avez contribué à rétablir les interactions spontanées dans la vie de mon père atteint d'Alzheimer, ainsi que de nombreuses autres personnes à qui j'ai fait part de ses bienfaits. Que Dieu vous bénisse.
Entre-temps, vos informations sur le DMSO semblent avoir été déterminantes pour lui [le patient victime d'un AVC]. Nous sommes maintenant à environ huit semaines de traitement et j'ai constaté : sa voix est plus forte, son élocution s'est nettement améliorée, son appétit a augmenté et sa dysphagie a considérablement diminué – il est maintenant capable de manger des repas normaux. Il se nourrit désormais presque exclusivement lui-même, en utilisant sa main affectée. Son goût commence à revenir.
Nous avons mis en pratique plusieurs des thérapies que vous nous avez indiquées. J'ai commencé par ajouter 2/3 de cuillère à café de DMSO avec une cuillère à café de galactose dans son café chaque matin. Je lui en ai également donné 2 cuillères à café après le petit-déjeuner, diluées dans du jus, et 2 cuillères à café l'après-midi, avec de bons résultats. Est-il guéri ? Non, mais il va beaucoup mieux.
Enfin, un lecteur a partagé le témoignage de son conjoint (75 ans) atteint d'un glioblastome inopérable de 8 cm, à l'origine d'une hémorragie cérébrale lente, d'une perte de la parole et d'une paralysie du côté droit, avec un pronostic vital de trois semaines. Après l'application locale abondante de DMSO à 99 %, sa fonction motrice a commencé à se rétablir en 24 heures. À la troisième semaine, il prenait ses repas à table. À la quatrième semaine, il pouvait marcher avec un déambulateur. Un nouveau scanner réalisé au 55e jour n'a révélé aucune hémorragie cérébrale et une diminution de la taille de la tumeur.
Sclérose en plaques
La sclérose en plaques (SEP) est une maladie auto-immune dans laquelle le système immunitaire attaque la myéline, la gaine isolante qui entoure les nerfs du cerveau et de la moelle épinière. À mesure que les nerfs démyélinisés perdent progressivement leur capacité à transmettre les signaux, les patients développent des déficits neurologiques de plus en plus importants, notamment une mobilité réduite, une perte de vision, des douleurs et un déclin cognitif. Malgré des décennies de recherche, les traitements actuels visent principalement à freiner l'attaque immunitaire sans restaurer la myéline perdue, ce qui entraîne une aggravation progressive du handicap chez les patients.
Le DMSO possède plusieurs propriétés qui le rendent particulièrement adapté au traitement de la SEP : il traverse la barrière hémato-encéphalique, réduit l’activité immunitaire nocive, diminue l’inflammation, améliore la circulation (y compris au niveau des faisceaux de substance blanche vulnérables) et, comme évoqué dans la section sur le repliement des protéines, agit comme un chaperon chimique qui stabilise les protéines. De plus, le DMSO inhibe la coagulation sanguine déclenchée par les débris de myéline de manière dose-dépendante – un point important car, lorsque la myéline est dégradée par le système immunitaire, les phospholipides exposés activent des voies de coagulation qui compromettent l’apport sanguin aux nerfs, constituant ainsi un mécanisme secondaire de neurodégénérescence dans la SEP que les anticoagulants existants ne ciblent pas. Le DMSO prévient également la toxicité induite par la bilirubine dans les axones myélinisés, ce qui suggère qu’il protège directement la myéline des produits de dégradation sanguine libérés lors d’une hémorragie ou d’une démyélinisation inflammatoire (de même, un inhibiteur de la caspase-1 – présent dans le DMSO – a inversé les dommages induits par la bilirubine sur les neurones de l’hippocampe via NLRP3).
Cette
perspective circulatoire sur la SEP s'inscrit également dans une
théorie plus large selon laquelle, outre l'insuffisance d'irrigation
sanguine du cerveau, l'altération du drainage veineux et lymphatique
cérébral contribue également à la neurodégénérescence, à la fois en
retenant les toxines et en perturbant le système glymphatique (voie
d'élimination des déchets du cerveau), ce qui entraîne une accumulation
de protéines pathologiques comme le β-amyloïde et l'α-synucléine. En
2009, il a été suggéré que
la SEP était liée à une insuffisance veineuse cérébrospinale chronique
(IVCC) – un mauvais drainage du cerveau par les veines jugulaires – et
des améliorations cliniques significatives ont été observées après la
pose d'endoprothèses dans les veines jugulaires (une technique également
utilisée pour d'autres affections neurologiques complexes avant d'être
restreinte en raison du lobbying pharmaceutique et de préoccupations légitimes concernant la sécurité ).
Plus récemment, en Chine, l'anastomose lymphatico-veineuse (ALV) — une
microchirurgie qui crée des connexions directes entre les vaisseaux
lymphatiques cervicaux profonds et les veines adjacentes afin de
contourner les obstructions de drainage — a déjà permis d'obtenir des
améliorations spectaculaires à court terme chez les patients atteints de
démence et est désormais proposée dans plus de 30 centres chirurgicaux.
<sup> 1,2,3 </sup> Remarque : cet article présente une excellente synthèse des données probantes concernant l' insuffisance veineuse cérébro- spinale chronique
(IVCC) et les affections neurologiques qu'elle provoque (bien que notre
approche thérapeutique diffère de celle des auteurs). <sup> 1,2 </sup>
Je suis enclin à croire que cette théorie est correcte, car nous avons observé de nombreuses améliorations spectaculaires chez des patients atteints de maladies neuro-immunes après la pose d'un stent dans la veine jugulaire, lorsque cette technique était encore disponible. De même, des cliniciens pionniers ont récemment découvert que les lésions induites par le vaccin contre la COVID-19 résultaient fréquemment d'une compression soudaine et persistante de la veine iliaque ( qu'ils ont traitée avec succès par la pose d'un stent ). Je pense personnellement que les obstructions du drainage résultent souvent d'un faible potentiel zêta – qui influence à la fois le flux sanguin et crée la force d'expansion maintenant les vaisseaux ouverts – ou de vaisseaux sanguins intrinsèquement fragiles, susceptibles de se collaber facilement. Ceci explique pourquoi les patients hypermobiles sont généralement beaucoup plus sensibles aux effets indésirables des médicaments (en particulier les vaccins qui altèrent le potentiel zêta ou qui, via la protéine Spike, fragilisent directement les vaisseaux sanguins), et pourquoi la sclérose en plaques est 10 à 11 fois plus fréquente chez les patients atteints du syndrome d'Ehlers-Danlos hypermobile .
Compte tenu des risques liés à la pose d'endoprothèses, j'ai exploré d'autres pistes pour traiter les troubles du drainage (avec succès). Le DMSO, en stimulant la circulation lymphatique et en améliorant le drainage veineux, et en éliminant les agrégats protéiques pathologiques qui s'accumulent en cas d'insuffisance de drainage (comme expliqué précédemment dans cet article), pourrait permettre de corriger ce trouble sous-jacent par voie pharmacologique plutôt que chirurgicale.
Note : le médecin pionnier Dietrich Klinghardt a étudié en profondeur le CCSVI dans diverses affections neurologiques et a rapporté sa présence chez 100 % des patients testés atteints de SEP, d'autisme, de Parkinson, de SLA et de la maladie de Lyme — les patients souffrant de fibromyalgie et de fatigue chronique en présentant également fréquemment — et les patients atteints de la maladie de Lyme obtenant généralement des résultats plus mauvais que les patients atteints de SEP (4 des 5 paramètres diagnostiques positifs contre 2 sur 5 dans la SEP). 1 , 2 , 3 , 4 Il a conclu que le CCSVI était provoqué par des infections endothéliales chroniques (Borrelia, Rickettsia, Chlamydia pneumoniae, Babesia) qui causaient une inflammation, une cicatrisation et une vasoconstriction permanente des veines jugulaires 1 , 2 , 3 (et je dirais une altération du potentiel zêta - comme Knisely l'a observé dans le cas du paludisme [qui est similaire à la babésiose], finalement tué par une accumulation de boues sanguines potentiellement mortelle qui commençait par la formation de petites boues le long des vaisseaux dans lesquels elle se cachait du système immunitaire 1 , 2 , 3 ). Bien que la dilatation par ballonnet ait produit une amélioration significative chez environ un tiers des patients, une amélioration modeste chez un tiers et aucun bénéfice durable chez un tiers, Klinghardt la préférait à la pose d'endoprothèses car ces dernières entraînaient des cicatrices et une occlusion veineuse <sup> 1,2 </sup>. Il avait également constaté que les résultats étaient inconstants, quelle que soit la méthode, si les infections sous- jacentes , les compressions tissulaires existantes et l'élévation des marqueurs inflammatoires (TGF-β1 , C4a, MMP- 9 ) n'étaient pas traitées au préalable, les veines se resténosant alors<sup>1,2,3,4,5,6</sup>. De même , d' autres cliniciens lors d'un sommet sur l' insuffisance veineuse cérébro - spinale chronique (ICCC ) ont confirmé son rôle dans la neurodégénérescence associée à de multiples pathologies <sup> 1,2 </sup> . Un protocole diagnostique auquel Klinghardt a contribué a utilisé les ultrasons thérapeutiques pour mobiliser les agents pathogènes compartimentés de l'endothélium veineux (ou éventuellement des dépôts tapissant l'endothélium) dans l'urine, où ils pouvaient être identifiés par des tests ADN (ce qui était souvent le cas)<sup> 1 </sup>.
DMSO chez les patients atteints de SEP
Dans un cas célèbre rapporté dans la littérature sur le DMSO , Stanley Jacob a pris le risque d'administrer du DMSO par voie orale à une femme de 29 ans paralysée par la sclérose en plaques et souffrant également d'insuffisance rénale. « Son amélioration a été spectaculaire, aussi spectaculaire que tout autre bénéfice que j'aie jamais constaté », a rapporté Jacob. Ses problèmes rénaux ont été stabilisés et, quelques semaines plus tard, elle a remarché. Six ans plus tard, elle marchait encore, conduisait et s'occupait de sa famille, malgré un déclin progressif de son état (indiquant que le DMSO ne suffisait pas à guérir complètement sa maladie).
Un autre cas plus récent concerne une Californienne alitée en position fœtale dans un centre de convalescence, dont l'espérance de vie était estimée à quelques mois. Après avoir commencé un traitement au DMSO par différentes voies (injection, voie orale et application topique), elle a commencé à recouvrer la sensibilité de ses jambes, éprouvant d'abord des douleurs, ce qui était considéré comme un signe positif compte tenu de son insensibilité antérieure. Au cours de l'année suivante, elle a retrouvé la mobilité de ses jambes et la capacité de s'alimenter seule, son état continuant de s'améliorer jusqu'à son transfert dans un autre État où le traitement n'était pas disponible.
La seule étude formelle connue à ce jour a évalué 34 patients atteints de SEP en Russie en 1984. Globalement, les chercheurs ont constaté que le DMSO avait un effet très positif, avec les meilleurs résultats chez les patients atteints de SEP rémittente, tandis que les résultats étaient plus variables chez ceux atteints de SEP rapidement progressive. Ils ont attribué ces bénéfices à la remyélinisation induite par le DMSO, à la réduction de l'œdème, à l'amélioration de la communication entre les cellules nerveuses et à ses effets positifs sur l'immunité et la réparation tissulaire, sans aucun effet secondaire rapporté.
En outre :
• Un rapport de cas russe a
documenté le succès d'un traitement au DMSO chez un patient atteint de
SEP présentant des lésions trophiques et une cystostome.
• Le DMSO a également été utilisé par voie topique (mélangé à des anesthésiques) sur les zones de déclenchement pour gérer la névralgie du trijumeau chez les patients atteints de SEP, avec des résultats incluant la réduction de la carbamazépine aux doses minimales ou l'arrêt complet et l'obtention d'une rémission complète lors des exacerbations.
• Une étude menée auprès de 35 patients atteints de SEP (durée de la maladie : 2 à 18 ans) a recommandé des gels topiques contenant du DMSO mélangés à des analgésiques non stéroïdiens pour les douleurs neuropathiques chroniques, les douleurs myofasciales dues aux muscles spastiques et les douleurs le long des troncs nerveux périphériques chez les patients alités.
Rapports des lecteurs
Quelques lecteurs ont également signalé des améliorations de leur sclérose en plaques suite à l'utilisation de DMSO, ce qui corrobore les données précédentes.
L'épouse d'un lecteur, atteinte de névralgie du trijumeau liée à la sclérose en plaques et souffrant depuis plus d'un an et demi, a testé une crème à 70 % de DMSO sur une petite zone de son visage. Sa douleur a diminué de 90 %. Le lendemain matin, elle l'a appliquée sur toute la zone névralgique et la douleur avait quasiment disparu (à 99,9 %). Même trois jours plus tard, sans nouvelle application, la douleur n'était pas réapparue.
Une autre lectrice a rapporté que le DMSO « met fin à mes crises de sclérose en plaques. Avant que mon mari ne découvre ce produit pour moi, je devais les endurer ou aller à l'hôpital pour obtenir de la morphine. »
Une lectrice atteinte de SEP, de fibromyalgie, de fibrose hépatique, de SDRC et de lymphœdème a décrit le DMSO oral et topique comme « une aubaine » après environ un an d'utilisation.
Un patient atteint de sclérose en plaques prenant du DMSO par voie orale quatre fois par jour a déclaré que cela était « incroyablement utile pour la douleur et l'énergie ».
Un lecteur a rapporté que le MSM ⬖ (métabolite oxydé du DMSO), ainsi que d'autres suppléments, lui ont permis d'arrêter tous les médicaments prescrits pour la SEP et leurs médicaments associés aux effets secondaires, déclarant qu'il « se sent plus jeune et en meilleure forme que jamais ».
Note : un article de 1982 indiquait que le DMSO avait été présenté comme un médicament miracle pour de nombreuses affections, dont la sclérose en plaques, ce qui suggère que les expériences de ces lecteurs ne sont pas uniques.
Interactions de la myéline avec le DMSO
Des études de diffraction des rayons X ont révélé que le DMSO interagit directement avec la structure de la myéline et qu'à fortes concentrations, il induit une transformation totalement réversible de la myéline nerveuse en une nouvelle structure hautement ordonnée (le DMSO expulse l'eau entre les spires de myéline et modifie sélectivement la couche membranaire externe). <sup> 1,2 </sup>
• La clémastine , un antihistaminique étudié comme agent remyélinisant pour les maladies hypomyélinisantes, a également montré des effets préliminaires sur les processus de myélinisation in vitro.
Les oligodendrocytes sont les cellules qui produisent la myéline dans le système nerveux central, et leur régénération est essentielle à la remyélinisation. Il a été démontré que le DMSO augmente considérablement la génération de précurseurs d'oligodendrocytes à partir de cellules souches humaines <sup> 1,2,3 </sup> (et que cet effet est encore renforcé en association avec l'acide tout-trans-rétinoïque) <sup>1,2 </sup> . De plus, dans les cellules souches neurales, les inhibiteurs de la γ-sécrétase (dans le DMSO) modulent la voie de signalisation Notch1 et augmentent l'expression des marqueurs d'oligodendrocytes. De même, le clobétasol (dans le DMSO) favorise la différenciation des cellules souches neurales en neurones et en oligodendrocytes.
Remarque : une étude a révélé que le DMSO orientait les cellules souches vers la production d'astrocytes, suggérant que des doses plus faibles favorisent la différenciation des oligodendrocytes, tandis que des doses plus longues et soutenues favorisent celle des astrocytes.
Autres maladies démyélinisantes
L’encéphalomyélite auto-immune expérimentale (EAE), modèle animal de référence pour la sclérose en plaques (SEP), immunise les animaux contre les protéines de la myéline afin de déclencher une démyélinisation auto-immune et, de ce fait, fournit des informations précieuses pour le traitement de la SEP. Notamment, comme je le démontre ici , le vaccin contre l’hépatite B (qui agit en synergie avec la myéline, induisant une auto-immunité contre celle-ci) a été associé à plusieurs reprises à la sclérose en plaques et a également provoqué une EAE auto-immune.
Dans une étude de 1969, le DMSO a été mentionné comme option thérapeutique pour l'EAE, et dans les expériences sur l'EAE, les animaux sont fréquemment traités avec un agent thérapeutique dissous dans du DMSO. De ces études, une tendance constante s'est dégagée : les agents dissous dans du DMSO ont amélioré les scores cliniques de l'EAE, diminué l'infiltration de cellules inflammatoires et réduit la démyélinisation, chaque agent se distinguant par ses mécanismes d'action spécifiques et ses effets additionnels.
L'acide nordihydroguaïarétique, la tanshinone IIA et le sulforaphane ont augmenté les signaux antioxydants protecteurs et anti-inflammatoires tout en diminuant l'IL-17A inflammatoire dans les cellules immunitaires de l'EAE. L' acide nordihydroguaïarétique a également restauré la barrière hémato-encéphalique et, dans une étude distincte, l'acide nordihydroguaïarétique et la tanshinone IIA ont tous deux favorisé la remyélinisation et rétabli l'intégrité axonale. <sup> 1,2,3,4,5 </sup> La curcumine a retardé l'apparition de la maladie et , en plus de réduire l'infiltration inflammatoire et la perte de myéline, a normalisé l'autophagie altérée et diminué les cytokines inflammatoires.<sup> 1,2 </sup> L' inhibiteur de la division mitochondriale 1 a diminué l'apoptose des oligodendrocytes et de la moelle épinière, protégé l'intégrité axonale et favorisé les facteurs de croissance nerveuse. Le butylphtalide ( 1,2 ) a protégé les mitochondries, inhibé la nécroptose et diminué les taux de TNF-α et d'IL-1β, tandis que la ferrostatin-1 (un inhibiteur de la ferroptose) et la matrine ( 1,2 ) ont chacune réduit de façon similaire la gravité des symptômes neurologiques. Un inhibiteur de l'époxyde hydrolase a réduit la gravité de la maladie dans l'EAE chronique en supprimant plusieurs voies inflammatoires (signalisation TLR4/NF-κB, inflammasomes, COX-2 et synthases de l'oxyde nitrique) et , dans une étude distincte, a favorisé la remyélinisation via une expression accrue des protéines protéolipidiques de la myéline.
D'autres agents ont démontré leur efficacité dans l'EAE, notamment l'hydroxyfasudil (qui a également prévenu l'apparition de l'EAE et supprimé les principales cytokines pro-inflammatoires), un inhibiteur de la p38 MAPK <sup>1,2 </sup> ( qui a réduit l'expression de l'IL-17), le ginkgolide A <sup>⬖</sup> (qui a retardé l'apparition de la maladie et orienté les macrophages vers un état anti-inflammatoire), l'isoliquiritigénine <sup> ⬖</sup> (qui a supprimé les cellules Th1 inflammatoires et activé les astrocytes protecteurs), le chlorure de nitidine <sup>⬖</sup><sup> 1 </sup> (qui a augmenté l'IL-10 anti-inflammatoire en administration préventive), un inhibiteur de JAK2 (qui a retardé l'apparition de la maladie et diminué l'inflammation induite par les Th17), l'arctigénine <sup>⬖</sup> (qui a diminué les cellules Th1 et Th17 via l'activation d'AMPK/PPAR-γ et l'inhibition de p38), un inhibiteur de la caspase-1 (qui a retardé l'apparition de la maladie et diminué les taux d'IL-1β et d'IL-18), ainsi que la schisandrine B <sup> ⬖</sup> et la baicaline <sup>⬖</sup>. AG490 et NBP. 1 , 2 , 3
Outre les modèles d'EAE, dans les cellules de patients atteints de SEP nouvellement diagnostiquée et traitée par IFN-β, la silymarine a supprimé la prolifération des cellules Th1 et inhibé la production d'IFN-γ de façon dose-dépendante et temps-dépendante, suggérant qu'elle pourrait compléter les traitements existants de la SEP. La chrysine a réduit la gravité de la maladie et la démyélinisation dans la névrite auto-immune expérimentale (un modèle animal du syndrome de Guillain-Barré).
Enfin, un lecteur atteint du syndrome de Morvan , une canalopathie auto-immune rare et grave (survenue après une encéphalite virale), a rapporté qu'après deux semaines d'application topique d'une crème à 70 % de DMSO, l'inflammation de ses mains avait visiblement diminué et la douleur avait été réduite de 75 %. Son cas était particulièrement sévère, ayant nécessité de multiples interventions chirurgicales de décompression nerveuse, quatre arthroplasties, une arthrodèse cervicale et la pose de deux neurostimulateurs.
Modèles Cuprizone
La cuprizone est un chélateur du cuivre qui, administré à des souris, provoque une démyélinisation toxique, offrant ainsi un modèle pour étudier la remyélinisation indépendamment de la composante auto-immune. Chez les souris démyélinisées par la cuprizone, l'agoniste cannabinoïde WIN55212-2 (1 mg/kg dans du DMSO) a significativement réduit la perte de poids, amélioré la fonction motrice, diminué la démyélinisation du corps calleux, augmenté l'expression de la protéine basique de la myéline, réduit l'activation astrocytaire et stimulé l'expression de la juxtanodine et de Nkx2.2 (facteurs de transcription impliqués dans la réparation de la myéline).<sup> 1,2,3 </sup> L' hydroxyfasudil et le fasudil ont également amélioré les déficits comportementaux, atténué la démyélinisation et fortement inhibé la neuroinflammation induite par la microglie dans le modèle d'EAE induite par la cuprizone. L'inhibiteur de la division mitochondriale 1 a protégé les oligodendrocytes et supprimé l'activation du complément sur les oligodendrocytes du corps calleux. La biochanine A ⬖ a amélioré la force de préhension, la mémoire spatiale et de reconnaissance, et a atténué les dommages neuronaux de l'hippocampe et du cortex préfrontal.
Neuromyélite optique
La neuromyélite optique (NMO) est une maladie auto-immune démyélinisante apparentée qui s'attaque préférentiellement aux nerfs optiques et à la moelle épinière par le biais d'anticorps ciblant les canaux hydriques de l'aquaporine-4. Dans un modèle murin de NMO, la tanshinone IIa ⬖ (dans du DMSO) a réduit significativement la perte d'aquaporine-4, de GFAP et de protéine basique de la myéline, diminué l'infiltration de neutrophiles et de microglie, et augmenté l'apoptose des neutrophiles. De même, l'arbidol (dans du DMSO) a augmenté la survie des cellules corticales de 49 % à 79 % in vitro et réduit la perte d'aquaporine-4/GFAP in vivo.
Lésion de la substance blanche et myélinisation néonatale
Plusieurs études ont démontré que des agents associés au DMSO peuvent protéger ou restaurer la myélinisation lors de lésions de la substance blanche non auto-immunes. Le donneur de sulfure d'hydrogène, l'anéthol trithione, a favorisé la remyélinisation, la prolifération et la différenciation des précurseurs d'oligodendrocytes, l'élimination des débris de myéline par la microglie et la récupération fonctionnelle à long terme après un accident vasculaire cérébral sous-cortical de la substance blanche. Le siponimod a réduit la perte de myéline et l'atrophie cérébrale après une hémorragie intracérébrale. Un agoniste inverse du récepteur GABA<sub>A</sub> α5 a favorisé l'oligodendrogenèse, la myélinisation et amélioré la fonction motrice chez le rat ischémique. Dans un modèle de lésion de la substance blanche néonatale, le miconazole (dans le DMSO) a augmenté significativement l'expression de la protéine basique de la myéline et amélioré l'ultrastructure de la myéline. L'agomir miR-219 a amélioré la maturation des oligodendrocytes chez le rat nouveau-né présentant une neuroinflammation induite par le LPS via la voie ERK1/2. Lors d'une lésion de la moelle épinière, un inhibiteur du récepteur du facteur de croissance épidermique a réduit la démyélinisation et l'expression de la molécule inhibitrice associée à la myéline.
DMSO et repliement des protéines
Les chaperons chimiques sont
de petites molécules qui facilitent le repliement correct des protéines
et contribuent ainsi à leur stabilité ou à l'élimination des protéines
mal repliées. De nombreuses maladies complexes (notamment génétiques)
étant dues à des protéines mal repliées ou non fonctionnelles, les
chaperons chimiques représentent une stratégie thérapeutique
potentiellement précieuse.
Remarque : Je pense que le potentiel zêta physiologique joue un rôle important dans le repliement correct des protéines.
Parmi les chaperons chimiques les plus connus figurent le glycérol, l'eau deutérée et le DMSO ( dont l'efficacité serait en partie due à sa capacité à créer un encombrement plus compact autour des protéines et à stabiliser leur conformation). Le DMSO, quant à lui, s'est révélé prometteur dans le traitement des maladies liées à un mauvais repliement protéique, telles que le diabète insipide néphrogénique<sup> 1,2 </sup> , la mucoviscidose et la maladie de Machado-Joseph . Il peut également améliorer la capacité des cellules immunitaires déficientes (en raison d'un défaut de l'HLA-DM) à présenter les antigènes nécessaires au déclenchement d'une réponse immunitaire<sup> 1</sup> .
L'amylose, une maladie liée à un mauvais repliement des protéines, survient lorsque des protéines mal repliées pénètrent dans la circulation sanguine, s'agrègent en fibrilles amyloïdes et se déposent dans les tissus (ce qui, à terme, endommage les organes et peut entraîner une défaillance multiviscérale). Les options thérapeutiques étant limitées, le DMSO a été testé. Les premiers résultats positifs ont conduit à son utilisation répétée dans certaines régions (par exemple, au Japon), où les meilleurs résultats ont été obtenus avec des concentrations élevées appliquées directement sur la zone affectée (par exemple, la paroi de la vessie ou la peau). Bien que son efficacité ne soit pas systématique, de nombreuses études ont montré qu'il produisait régulièrement des résultats spectaculaires chez des patients atteints de pathologies autrement fatales, et ce, apparemment en dissolvant les amyloïdes et en facilitant leur excrétion urinaire (détaillé ici ).
Remarque : étant donné que de nombreuses protéines cancérigènes sont des protéines mal repliées, on pense que cela pourrait expliquer en partie les propriétés anticancéreuses du DMSO.
Outre les maladies évoquées précédemment, trois affections neurologiques caractérisées par des protéines défectueuses ont montré des réponses prometteuses au DMSO.
maladie de Niemann-Pick
La maladie de Niemann-Pick est une maladie génétique rare de surcharge lysosomale, caractérisée par une accumulation intracellulaire de sphingomyéline, due soit à un déficit en sphingomyélinase, l'enzyme qui la dégrade (types A et B), soit à un défaut de transport du cholestérol lysosomal (type C). Chaque type entraîne des lésions organiques et une neurodégénérescence. Le type A [NPA] est le plus sévère (le décès survient généralement entre 2 et 3 ans), le type B [NPB] le moins sévère (atteinte neurologique minime) et le type C [NPC] entraîne en moyenne le décès vers l'âge de 13 ans. Le DMSO, qui stabilise les protéines et améliore le transport cellulaire, a été étudié à plusieurs reprises pour le traitement de cette maladie (en particulier du type C).
Cette maladie est fréquemment étudiée sur des fibroblastes humains présentant cette anomalie. Il a été démontré que le DMSO produit les effets suivants :
Dans les fibroblastes normaux , une
exposition à 2 % de DMSO pendant 4 jours a augmenté l'activité de la
sphingomyélinase jusqu'à 230 % des valeurs témoins, de façon
dose-dépendante (avec une augmentation beaucoup plus faible des autres
hydrolases lysosomales). Dans les fibroblastes de patients atteints de
NPC, le DMSO à 2 % a augmenté l'activité de la sphingomyélinase de 480 %
(corrigeant ainsi le déficit), ainsi que d'une augmentation plus faible
(280 %) observée dans les fibroblastes de NPB.
Remarque :
dans la NPC, la diminution de l'activité de la sphingomyélinase résulte
de l'accumulation massive de cholestérol dans la cellule (et non d'une
altération génétique de l'enzyme).
Dans les fibroblastes normaux , le DMSO à 2 % a augmenté l'activité de la sphingomyélinase, principalement au sein des lysosomes, de 168 à 263 % (selon le pH). Dans les fibroblastes NPC (qui conservaient 30 % de l'activité de la sphingomyélinase), le DMSO a induit une augmentation de plus de deux fois cette activité, la ramenant à des niveaux proches de la normale, tandis qu'aucune amélioration n'a été observée dans les fibroblastes NPA et NPB. De plus, de plus faibles augmentations d'autres hydrolases lysosomales ont été constatées, indiquant que le DMSO cible spécifiquement la sphingomyélinase.
• Lorsque les fibroblastes NPC ont été exposés au LDL, le DMSO à 2 % a eu un effet minimal au cours des 12 premières heures, mais a considérablement réduit l'accumulation excessive de cholestérol non estérifié dans les lysosomes par la suite (en particulier entre 24 et 48 heures), ramenant les niveaux de cholestérol à des niveaux proches de ceux des cellules normales (fluorescence du cholestérol périnucléaire/lysosomal nettement diminuée) et rétablissant les réponses homéostatiques cellulaires altérées au cholestérol.
• Dans les fibroblastes normaux , douze médicaments spécifiques (par exemple, d'anciens médicaments psychiatriques) ont réduit significativement l'estérification du cholestérol (l'un d'eux a induit une réduction de 93 % pendant au moins 48 heures). Le DMSO (2 %) a partiellement contrecarré cet effet et restauré 16 à 20 % de la capacité de métabolisation du cholestérol perdue, suggérant une utilisation potentielle dans la maladie de Niemann-Pick de type C.
• Le DMSO à 2 % (mais pas à 1 % ni à 4 %) a augmenté significativement l'activité de la sphingomyélinase dans les fibroblastes normaux et ceux de la NPC. Cependant, contrairement aux autres études, aucune des concentrations testées n'a réduit le cholestérol cytoplasmique dans les fibroblastes de la NPC.
• Enfin, dans les fibroblastes de souris (modélisant NPA/B), 2 % de DMSO ont provoqué une augmentation de 2 à 3 fois de l'activité de la sphingomyélinase.
Ces résultats suggéraient que le DMSO pourrait améliorer partiellement la maladie, et ils (surtout les premiers) ont suscité un intérêt suffisant pour explorer l'utilisation du DMSO dans son traitement, ce qui a permis de constater ce qui suit :
Chez les souris NPA/B , l'administration orale de DMSO (0,25 % dans l'eau de boisson à partir de l'âge de 6 semaines) a prolongé la survie d'environ 12 semaines chez les souris non traitées à une moyenne de 15 semaines et 5 jours (maximum 17 semaines et 5 jours) et a retardé l'apparition de symptômes neurologiques tels que les tremblements. Cependant, elle n'a pas permis d'empêcher la progression des symptômes ni d'améliorer les manifestations déjà présentes et a eu un effet minime sur l'accumulation de cholestérol (légère diminution au niveau du foie, la rate et le cerveau restant inchangés).
• Chez les souris NPC , le flavopiridol (dissous dans du DMSO) et perfusé directement dans le cerveau a réduit de manière dose-dépendante l'hyperphosphorylation des protéines cytosquelettiques et amélioré le comportement.
Chez des patients atteints de NPC , une étude japonaise a rapporté que l'administration orale de DMSO entraînait certains bénéfices cliniques, notamment une diminution de la taille de l'hépatosplénomégalie, une réduction de la fréquence des crises d'épilepsie et une amélioration des résultats de l'EEG. Cependant, l'évolution clinique progressive de la maladie n'était pas modifiée, bien qu'elle semblât ralentie.
L'auteur de cet article a également publié :
• Observation clinique d'une fillette de 8 ans atteinte de NPC présentant une détérioration psychomotrice sévère, une atrophie corticale marquée, des crises d'épilepsie fréquentes, une dilatation ventriculaire modérée et une hépatosplénomégalie. L'administration orale de DMSO a permis de normaliser son activité sphingomyélinase. Après deux ans de traitement par DMSO, on a observé une légère amélioration de sa réactivité à son environnement, une diminution de la fréquence de ses crises d'épilepsie (permettant une réduction progressive de l'anticonvulsivant), une nette amélioration de son EEG (normalisation des ondes thêta et des fuseaux), une stabilisation de son atrophie corticale et une normalisation du volume de sa rate et de son foie.
• Un autre rapport sur des frères et sœurs atteints de NPC qui ont présenté une amélioration clinique grâce au DMSO.
•Une étude qui a de nouveau constaté que le DMSO corrigeait le déficit en sphingomyélinase dans les fibroblastes cultivés de patients atteints de NPC.
• Une étude montrant que d'autres substances aprotiques dipolaires, outre le DMSO, augmentaient également de manière sélective l'activité de la sphingomyélinase.
Remarque : enfin, un dernier rapport de cas détaille l'échec du traitement du NPC par DMSO oral.
Maladie de Creutzfeldt-Jakob et maladies à prions
Les maladies à prions (comme la MCJ chez l'homme et la tremblante du mouton chez l'animal) résultent du repliement anormal de protéines prions normales en une forme pathogène (PrPSc) qui s'agrège en fibrilles toxiques et détruit progressivement le tissu cérébral. Ces maladies sont systématiquement mortelles et il n'existe aucun traitement approuvé .
Le DMSO a démontré un potentiel thérapeutique par de multiples mécanismes. En tant que chaperon chimique, il a stabilisé la structure en hélice alpha normale de la protéine prion nouvellement synthétisée dans les cellules de neuroblastome infectées, inhibant sa conversion en forme pathogène. Dans les cellules porteuses d'une mutation de la MCJ familiale, le DMSO a inversé le phénotype mutant en réduisant l'accumulation lysosomale de la protéine prion mal repliée et en restaurant sa distribution normale à la surface cellulaire. <sup> 1,2 </sup> Dans des modèles de prion chez la levure, le DMSO a guéri plusieurs variants de prion plus efficacement que le chlorhydrate de guanidine en augmentant l'activité chaperonne (Hsp104) et en reconvertissant la protéine agrégée en formes solubles.
Le DMSO a également inhibé partiellement l'agrégation de PrPSc, produisant des agrégats amorphes dont l'infectiosité prionique était inférieure à 1 % de celle des agrégats en forme de bâtonnets non traités, après inoculation chez le hamster. <sup>1,2,3 </sup> Chez les hamsters infectés par le prion, le DMSO a prolongé la durée d'incubation, réduit le taux d'accumulation de PrPSc dans le cerveau et (comme observé dans l'amylose) augmenté l'élimination urinaire de la protéine prion résistante aux protéases – sans toutefois constituer à lui seul un traitement curatif. <sup> 1,2 </sup>
Les complexes ruthénium-DMSO (apparentés à NAMI-A) ont montré des effets encore plus marqués, désagrégeant les fibrilles de peptide prion, réduisant le stress oxydatif induit par le cuivre et restaurant la viabilité des cellules neuronales de 33 % à 85 %. <sup> 1,2 </sup>
Une lectrice a rapporté que sa cousine atteinte de MCJ s'était améliorée après environ un mois de perfusions intraveineuses de DMSO ; nous avons appris par la suite qu'elle dirigeait un centre de perfusion et avait utilisé des perfusions à haute dose de vitamines et de DMSO pour traiter de nombreuses affections graves, sa cousine étant toujours en vie plusieurs années plus tard.
Remarque : deux études sur les prions ont trouvé des résultats moins favorables, 1 , 2 indiquant que les résultats peuvent varier selon l'espèce, la souche ou le protocole.
Enfin, les propriétés stabilisatrices de protéines du DMSO s'étendent probablement au-delà des protéines mal repliées : il a été démontré qu'il agit comme un chaperon pharmacologique qui restaure le trafic normal des récepteurs membranaires et (dans de nombreuses études) qu'il stabilise les microtubules cérébraux lors de l'isolement en empêchant la dépolymérisation de la tubuline en situation de stress. <sup> 1,2 </sup> Étant donné que les microtubules sont essentiels à la fonction neuronale et sont altérés dans les maladies neurodégénératives, cela renforce probablement les effets neuroprotecteurs du DMSO dans des pathologies telles que les AVC ou les traumatismes crâniens, où l'effondrement des microtubules dû au stress oxydatif ou à l'ischémie aggrave les lésions neuronales.
Remarque : les bénéfices observés dans la dernière maladie, le syndrome de Down (abordé plus loin), pourraient résulter des effets neuroprotecteurs et antioxydants du DMSO, combinés à sa capacité à agir comme un chaperon chimique (ce qui pourrait aider les cellules à gérer la surcharge de protéostasie due à un excès de protéines et à favoriser l'élimination des protéines mal repliées ou endommagées), ou à sa capacité à améliorer le transport des nutriments essentiels à travers les membranes compromises.
Troubles cognitifs et démence
Les mêmes processus dégénératifs à l'origine de la démence déclenchent initialement des troubles cognitifs. Par conséquent, pouvoir les prévenir précocement permet non seulement d'améliorer considérablement la qualité de vie, mais aussi d'éviter des situations bien plus graves. Ces processus neurodégénératifs (comme une mauvaise circulation sanguine et une inflammation) étant également impliqués dans de nombreux autres troubles neurologiques traités par le DMSO, des données importantes ont été recueillies concernant l'efficacité du DMSO, seul ou en association avec une autre thérapie, pour inverser le déclin cognitif.
La recherche animale dans ce domaine est la suivante :
Lorsque les artères carotides de rats ont été modifiées chirurgicalement afin de réduire considérablement la quantité de sang irriguant leur cerveau, on a constaté qu'après 3 mois, le DMSO prévenait à la fois les lésions neuronales et la perte importante de mémoire spatiale et d'apprentissage qui résultaient autrement de cette perte chronique de flux sanguin cérébral.
Dans une étude similaire, des rats âgés de 14 semaines ont été soumis soit à une occlusion bilatérale permanente des artères carotides, soit à une occlusion simulée (mimant les troubles vasculaires chroniques que beaucoup rencontrent avec l'âge), puis leur mémoire visuospatiale a été évaluée. Après 14 semaines, quatre rats présentant des troubles de la mémoire persistants et sévères ont reçu du DMSO et du FDP pendant 7 jours, ce qui a amélioré leur mémoire de 54 %, atteignant presque les performances cognitives des témoins. Malheureusement, cette amélioration a été partiellement perdue à l'arrêt du traitement par DMSO-FDP (l'apport sanguin restant occlus). <sup> 1,2 </sup>
Les souris Lurcher sont utilisées pour étudier les troubles olivaires et cérébelleux car leurs cellules de Purkinje ne survivent pas (par exemple, dès l'âge de 30 jours, leur démarche est fortement anormale). L'administration de DMSO à ces souris a permis de prévenir le déclin cognitif lié à l'âge de certaines fonctions (par exemple, la mémoire et les capacités d'apprentissage spatial). <sup> 1,2 </sup>
Le DMSO a également démontré des effets cognitifs directs dans d'autres contextes. Il a réduit de 80 à 86 % la nécrose neuronale induite par le MK-801 dans le cortex cingulaire et rétrosplénial du rat, même administré jusqu'à 4 heures après la prise – une observation pertinente pour la sécurité de l'anesthésie et la neuroprotection. Chez des souris sensibilisées à la morphine , le DMSO a amélioré indépendamment la formation de la mémoire spatiale dans le labyrinthe aquatique de Morris (effets encore renforcés par la curcumine ) . Dans un modèle murin de carence en thiamine (pertinente pour l'encéphalopathie de Wernicke), le DMSO a partiellement amélioré les déficits comportementaux et réduit les lésions thalamiques ; combiné à une forte dose de thiamine, il a amélioré la récupération au-delà de celle obtenue avec la thiamine seule . Le DMSO seul n'a également induit aucun déficit d'apprentissage spatial lorsqu'il a été injecté dans l'hippocampe lors d'une tâche de labyrinthe radial à 8 bras, confirmant ainsi son innocuité en tant que vecteur dans la recherche cognitive.
Troubles cognitifs induits par l'anesthésie
L'anesthésie générale, en particulier une exposition prolongée ou répétée, peut entraîner des déficits cognitifs durables et est reconnue pour augmenter significativement le risque de maladie d'Alzheimer (ce qui constitue une préoccupation croissante chez les jeunes enfants dont le cerveau est encore en développement et chez les personnes âgées). Face au nombre important de cas de démence survenus (certains neurones anesthésiés pendant l'intervention chirurgicale ne semblant jamais se réactiver par la suite), nous nous efforçons de minimiser les interventions chirurgicales, de privilégier l'utilisation d'anesthésiques moins toxiques (les anesthésiques inhalés étant les plus problématiques) et d'avoir recours à des nutraceutiques pour contrer la sédation.
Heureusement, le DMSO agit à la fois sur les mécanismes reconnus de la toxicité de l'anesthésie (par exemple, la neuroinflammation, le stress oxydatif, le dysfonctionnement mitochondrial ou l'apoptose neuronale) et sur ce que nous considérons comme le problème clé ( le blocage des cellules en phase dormante ). Malheureusement, toutes les recherches existantes sur ce sujet ont utilisé le DMSO en association avec un autre agent ; il n'existe donc pas de preuve définitive que le DMSO seul soit un antidote à la toxicité de l'anesthésie.
Le sévoflurane , l'un des anesthésiques inhalés les plus utilisés, est aussi celui qui a fait l'objet du plus grand nombre d'études. Le resvératrol dissous dans du DMSO a protégé de façon répétée les rats âgés et nouveau-nés contre les déficits cognitifs induits par le sévoflurane en activant la voie SIRT1, en réduisant la neuroapoptose, en augmentant l'expression du BDNF et en améliorant la mémoire spatiale. 1 , 2 , 3 D'autres combinaisons protégeant contre les troubles cognitifs induits par le sévoflurane incluent l'arctigénine (qui réduit l'inflammation via la voie Akt/NF-κB et augmente l'expression de CTRP6), l'honokiol ⬖ (qui active SIRT3, réduisant la neuroinflammation, le stress oxydatif et le dysfonctionnement mitochondrial), le SAHA (qui inhibe l'activation de l'inflammasome NLRP3 et améliore les troubles cognitifs chez les souris âgées), 1 , 2 la curcumine ⬖ 1 , 2 (qui améliore les troubles de la récupération de la mémoire et inverse l'augmentation d'Aβ et la surexpression de BACE-1 induites par le sévoflurane chez les rats âgés), un agoniste de S1P (qui prévient l'apoptose de l'hippocampe chez les rats nouveau-nés), la progestérone (qui atténue les lésions neuronales induites par le sévoflurane dans les neurones hippocampiques primaires via les récepteurs de la progestérone et la signalisation Akt), et des inhibiteurs de la Voie TLR4-p38MAPK-NF-κB (qui a atténué le déclin cognitif).
Remarque : dans une étude sur des rats nouveau-nés , le resvératrol a amélioré les marqueurs moléculaires (SIRT1, PGC-1α, FOXO3α, SOD) et réduit les dommages pathologiques cérébraux après le sévoflurane, mais les tests du labyrinthe aquatique de Morris n'ont montré aucune amélioration comportementale significative entre les groupes.
Le propofol , un autre anesthésique largement utilisé, provoque une apoptose neuronale dose-dépendante et des déficits cognitifs persistants en cas d'exposition néonatale répétée. Parmi les agents dissous dans du DMSO qui protègent contre la neurotoxicité du propofol, on trouve la dexmédétomidine (qui active la voie PI3K/Akt/GSK-3β dans de nombreuses études), l' étanercept ( qui bloque les dommages induits par le TNF-α), le SAHA (qui inverse les troubles de l'apprentissage et de la mémoire en modulant l'acétylation des histones, les protéines synaptiques et la phosphorylation de CREB), le 17β-estradiol (qui corrige les déficits via la voie ERK), l'hydroxylfasudil (qui réduit l'apoptose par inhibition de la p38 MAPK et améliore les performances au test du labyrinthe aquatique de Morris) et la coenzyme Q10 ( qui inverse partiellement l'inhibition de la chaîne respiratoire mitochondriale induite par le propofol dans les neurones hippocampiques primaires).
L'altération cognitive induite par l'isoflurane a été contrecarrée par la dexmédétomidine dissoute dans du DMSO (qui a activé la voie PI3K/Akt et réduit l'apoptose hippocampique), le lévosimendan administré par voie intranasale (qui a protégé le cerveau des rats nouveau-nés) et le modafinil (qui a amélioré la reconnaissance d'objets nouveaux et la mémoire de la peur contextuelle pendant la période d'éveil). La dexmédétomidine dans du DMSO a également protégé, de manière dose-dépendante, les neurones hippocampiques des rats nouveau-nés contre les lésions induites par l'étomidate via la même voie PI3K/Akt.
Autres anesthésiques : La dexmédétomidine a atténué la toxicité mitochondriale induite par la ropivacaïne via la voie p38 MAPK. La curcumine dans le DMSO a également protégé le cerveau en développement du rat contre la neurotoxicité induite par la kétamine via la voie antioxydante Nrf2-ARE, et a aussi protégé les neurones de l’hippocampe néonatal contre la neurotoxicité des anticonvulsivants phénobarbital et acide valproïque, réduisant significativement la perte neuronale. 1,2
Le dysfonctionnement cognitif postopératoire (DCPO), qui touche un pourcentage important de patients âgés opérés, a également répondu aux agents administrés par DMSO. Le jasplakinolide (un stabilisateur de l'actine F) a inversé les déficits du DCPO chez des souris âgées en restaurant le nombre d'épines dendritiques, l'expression des récepteurs du glutamate et l'activation neuronale hippocampique. Parmi les autres agents améliorant le DCPO, on trouve un inhibiteur de P300 (qui a amélioré les performances dans le labyrinthe aquatique et réduit l'apoptose hippocampique après une circulation extracorporelle), l'ononine (qui a réduit la neuroinflammation et le stress oxydatif après une néphrectomie chez des souris âgées) et l' Iduna , un modulateur de la voie Hippo/YAP . Dans une série d'expériences, la rapamycine a activé l'autophagie hippocampique pour atténuer les troubles cognitifs postopératoires chez des rats âgés, l'exendine-4 a protégé la cognition en stabilisant la glycémie et le propofol, à doses thérapeutiques, a prévenu l'autophagie excessive induite par un choc électroconvulsif (chacun de ces mécanismes étant complémentaire).
Autres causes de troubles cognitifs
De nombreuses affections altèrent les fonctions cognitives, et dans nombre d'entre elles, des agents thérapeutiques administrés dans du DMSO ont démontré une protection cognitive.
Les troubles du sommeil constituent une cause importante et sous-estimée du déclin cognitif. Chez des rats privés de sommeil, le sulfure de diallyle dissous dans du DMSO a inversé les troubles cognitifs, réduisant les comportements anxieux et le stress oxydatif hippocampique, tandis que le resvératrol a prévenu les déficits cognitifs induits par la privation de sommeil en réduisant la neuroinflammation et en augmentant l'expression des protéines de plasticité synaptique. Dans les modèles d'hypoxie intermittente chronique (qui simulent l'apnée obstructive du sommeil), les agents améliorant la cognition comprennent un inhibiteur du TGF-β1 (qui améliore la mémoire spatiale en réduisant la signalisation TGF-β1/Smad3 hippocampique), la capsaïcine , des inhibiteurs de la voie STAT3 , un agoniste du récepteur nicotinique de l'acétylcholine α7 (qui augmente l'expression du BDNF et du CREB) et des antagonistes des récepteurs A1 de l'adénosine. 1,2
L'altération cognitive chez les patients diabétiques a été améliorée par divers agents en association avec le DMSO. La rapamycine a amélioré la cognition dans plusieurs études en réduisant l'activité de mTOR, l'hyperphosphorylation de la protéine tau et l'apoptose 1,2,3, tandis que le captopril et le losartan ont amélioré la fonction cognitive par un mécanisme distinct : l'inhibition de l'axe ACE-angiotensine II-AT1R dans l'hippocampe de souris diabétiques. Un agoniste de TRPV4 a inversé les déficits cognitifs et stimulé la neurogenèse hippocampique, et le CNTF a amélioré le temps de latence d'échappement et augmenté l'expression de la choline acétyltransférase hippocampique via JAK2/STAT3. D'autres agents améliorant les troubles cognitifs diabétiques comprennent la pentaméthylquercétine ⬖ (signalisation Akt/CREB et augmentation des protéines synaptiques), le sulforaphane ⬖ (PI3K/Akt/GSK-3β et inhibition de l'apoptose mitochondriale), le nicotinate de curcumine ⬖ (amélioration de l'apprentissage spatial par la régulation de l'autophagie), l'huile de krill/EPA ⬖ (voie antioxydante NRF2), l'Urtica dioica ⬖ et la pioglitazone (marqueurs du stress oxydatif et fonction mitochondriale), et les inhibiteurs de PSD-95/nNOS (réduction des lésions neuronales via Sirt3).
L'encéphalopathie associée à la septicémie a répondu à un inhibiteur de HIF-1α (améliorant les fonctions cognitives et réduisant l'autophagie), au resvératrol (activant SIRT1 et réduisant l'apoptose hippocampique et l'activation microgliale), aux inhibiteurs de ROCK (réduisant les lésions cérébrales et l'inflammation, et améliorant la mémoire spatiale) et à l'hydrogène moléculaire (améliorant la survie et la cognition via la voie de signalisation Nrf2). Parmi les autres agents améliorant la cognition dans d'autres pathologies, on peut citer le Babao Dan pour l'encéphalopathie hépatique minime, l' hespéridine pour l'hyperhomocystéinémie et la curcumine pour l'hypoperfusion cérébrale associée au diabète.
Les troubles cognitifs liés à l'épilepsie ont été améliorés par le rolipram (un inhibiteur de la PDE4 qui a sauvé l'apprentissage spatial, la potentialisation à long terme de l'hippocampe et le CREB phosphorylé après un état de mal épileptique), 1 , 2 , 3 un inhibiteur de l'eEF2K (qui a restauré l'expression de l'AMPKα1 et amélioré la cognition et le comportement social chez les souris épileptiques chroniques), le sémaglutide (qui a amélioré la fonction cognitive et protégé les neurones de l'hippocampe via SIRT-1/NLRP3) et le pérampanel (qui a amélioré l'apprentissage spatial et réduit les dommages à l'hippocampe chez les souris immatures atteintes d'épilepsie du lobe temporal).
La douleur neuropathique altère fréquemment les fonctions cognitives, et cet effet a été inversé par un agoniste inverse des récepteurs GABA<sub>A</sub>α5 ( qui a restauré la signalisation GABAergique et amélioré la reconnaissance et la mémoire spatiale chez des rats présentant une lésion du nerf sciatique), par le SAHA (qui a amélioré l'apprentissage spatial chez des rats souffrant de douleurs cancéreuses osseuses) et par la curcumine (qui a stimulé la neurogenèse hippocampique et la plasticité synaptique). La rutine a également protégé contre les troubles cognitifs induits par le cadmium en restaurant l'équilibre antioxydant.
Les lésions cérébrales néonatales dues à l'hypoxie-ischémie ont été traitées par le coumestrol (qui a partiellement inversé les déficits cognitifs, la perte tissulaire et l'astrogliose réactionnelle), le C2-céramide (qui a réduit les lésions cérébrales hypoxiques-ischémiques néonatales de 45 à 65 %) et la chémérine humaine recombinante (qui a amélioré à la fois la fonction neurologique à court terme et les résultats cognitifs à long terme via la voie ChemR23/CAMKK2/AMPK/Nrf2). La stimulation magnétique transcrânienne répétitive combinée à la signalisation BDNF/TrkB a également amélioré l'apprentissage spatial chez les rats présentant des déficits cognitifs induits par le stress prénatal.
Le stress oxydatif et la neuroprotection ont été abordés par la ferrostatin-1 et un inhibiteur de caspase (qui ont amélioré la fonction cognitive et préservé les protéines synaptiques chez les rats surchargés en fer), et par des antagonistes des récepteurs du glutamate (qui ont protégé la substance blanche et l'ultrastructure de la myéline dans un modèle d'ischémie focale pertinent pour le déclin cognitif vasculaire).
Les agents ciblant les troubles cognitifs liés à la psychiatrie comprennent un antagoniste du CB1R (qui a permis de corriger les déficits de mémoire induits par les électrochocs sans affecter l'efficacité des antidépresseurs), la fisétine ⬖ (qui a inversé les troubles cognitifs induits par le MK-801 dans un modèle de schizophrénie en restaurant ERK/CREB/CaMKII) et la 7,8-dihydroxyflavone ⬖ (qui a amélioré la cognition spatiale et restauré les épines dendritiques de l'hippocampe dans un modèle de schizophrénie).
D'autres agents améliorant la cognition dans différents modèles incluent un antagoniste du récepteur C3a du complément (dysfonctionnement cognitif induit par le LPS), un agoniste du GPER (traumatisme crânien), de nouveaux inhibiteurs de la PDE4, le roflupram et le chlorbipram (qui ont inversé les déficits cognitifs induits par la scopolamine sans les effets secondaires émétiques des inhibiteurs de la PDE4 existants), et la prégnénolone (qui a amélioré l'apprentissage spatial et augmenté l'activité de la choline acétyltransférase chez les rats âgés). Les extraits de Sonchus asper et de Launaea procumbens ont chacun amélioré la cognition et le statut antioxydant cérébral (Sonchus asper inhibant également l'acétylcholinestérase), tandis que la 7,8-dihydroxyflavone a amélioré l'apprentissage des réponses via la phosphorylation du récepteur TrkB et que l' épigallocatéchine gallate a inversé les troubles cognitifs induits par un régime riche en graisses et la rapamycine, tout en améliorant l'activité de la sérotonine et de l'acétylcholinestérase.
Études humaines
Ces résultats ont été reproduits chez l'humain. Une étude a évalué 104 adultes âgés atteints d'une maladie cérébrale organique due à une maladie cérébrovasculaire (par exemple, un antécédent d'AVC, d'embolie cérébrale ou d'athérosclérose cérébrale), à un traumatisme crânien, à la sénilité ou à une maladie dégénérative (par exemple, la maladie de Parkinson, l'hyperthyroïdie ou l'épilepsie). Ces patients ont reçu deux mélanges de DMSO, Merinex (DMSO avec des acides aminés ) et Ipran (DMSO avec des substances vasoactives), généralement en alternance, le plus souvent par voie injectable et plus rarement par voie orale (les résultats les plus rapides étant obtenus lorsque les deux voies d'administration étaient utilisées simultanément). Dans tous les cas, des améliorations remarquables ont été observées. 1,2 Pour citer l'auteur :
La thérapie par acides aminés et DMSO est indéniablement précieuse dans le traitement de nombreuses maladies cérébrales organiques. Par ailleurs, grâce à l'amélioration de la circulation sanguine cérébrale obtenue par l'utilisation du DMSO en association avec des substances vasoactives, un effet très favorable sur les fonctions psychiques et somatiques des patients séniles a été observé.
Remarque : une autre étude a montré que Merinex traitait également les patients souffrant de troubles de l’humeur et d’anxiété. 1 , 2
Une étude chilienne a évalué 100 patients atteints de maladies cérébrovasculaires (par exemple, antécédents d'AVC, d'embolie cérébrale ou d'athérosclérose cérébrale), dont beaucoup étaient séniles, qui ont reçu du DMSO par voie orale et par injections intramusculaires pendant 50 jours. Il a été constaté que leur maladie coronarienne et leur hypertension artérielle s'étaient nettement améliorées chez 74,35 % des patients ayant reçu du DMSO, que 21,77 % avaient présenté une réponse modérée et que 3,88 % n'avaient présenté aucune réponse. 1,2 Les neurologues en charge de ces patients ont fait remarquer que :
« L’amélioration des symptômes généraux a été positive ; on a constaté des changements favorables se traduisant par un sentiment de bien-être, un regain d’agilité, une amélioration de l’humeur (passage de la dépression à la gaieté), un meilleur sommeil et une élocution plus claire. Concernant les résultats spécifiques, on a observé une récupération plus rapide de l’hémiplégie et de l’hémiparésie. On a également constaté une récupération plus rapide de la parole dans les cas d’aphasie diagnostiquée ou indiquée. »
De plus, chez 127 patients âgés (75-85 ans) atteints de troubles cérébrovasculaires, l'électrophorèse bitemporale avec Neuromidine en solution dans du DMSO a entraîné une amélioration clinique dès la 5e procédure chez 86 % d'entre eux, avec notamment une normalisation du sommeil, une réduction des vertiges, une amélioration de la mémoire et de l'audition, ainsi qu'une diminution des troubles cognitifs (comparativement à une amélioration retardée chez les sujets témoins recevant le traitement standard seul). Dans une autre étude portant sur 250 patients atteints de pathologies vasculaires cérébrales, l'utilisation du DMSO comme solvant de la vinpocétine lors d'une électrophorèse de la zone cervicale a stabilisé les paramètres du débit sanguin cérébral et amélioré la vascularisation des grosses artères cérébrales. De même, une monographie russe de physiothérapie gériatrique recommande l'utilisation du DMSO dans les protocoles d'électrophorèse transcrânienne pour l'encéphalopathie dyscirculatoire (ischémie cérébrale chronique), notamment avec des solutions à 50 % de DMSO associées à l'aspirine. Dans une étude clinique portant sur 154 patients subissant une revascularisation ouverte pour une ischémie aiguë des membres inférieurs, l'administration intraveineuse de DMSO (10 mg/kg) avant la reperfusion dans le cadre d'un protocole de prévention complet a entraîné une réduction des marqueurs de lésions de reperfusion, une diminution des cas de dysfonctionnement rénal, une moindre aggravation cardiopulmonaire et des problèmes cognitifs plus légers par rapport aux soins standard.
Note : dans un sanatorium militaire russe traitant des victimes d'attaques terroristes et d'autres urgences, le DMSO à 25 % figurait parmi les agents les plus fréquemment utilisés pour les lésions neurologiques (principalement les douleurs spinales et les maladies cérébrovasculaires), le plus souvent dans le cadre d'un programme de rééducation par électrophorèse de 21 jours (qui s'est avéré efficace pour soulager la douleur).
Rapports des lecteurs
Plusieurs lecteurs ont fait état d'améliorations cognitives suite à la prise de DMSO :
J'ai subi plusieurs petits AVC en août 2023. Je prends une cuillère à café de DMSO à 99 % deux fois par jour et les résultats sont remarquables ! L'amélioration de ma concentration est impressionnante et le soulagement de mes douleurs corporelles est le meilleur que j'aie jamais connu.
J'ai souffert de « brouillard cérébral » pendant 6 à 8 semaines après une opération totale de la hanche, probablement dû à l'anesthésie. J'ai commencé à boire 2 cuillères à café de DMSO dans 240 ml d'eau environ 6 à 7 semaines après l'opération et j'ai l'impression que cela m'a complètement guéri en une semaine environ. Maintenant, mon cerveau fonctionne à nouveau normalement.
J'avais autrefois un esprit brillant, capable de réussir facilement des études dans une université prestigieuse. Grâce à vos écrits sur le DMSO et la thérapie nutritionnelle de Walsh, j'ai commencé ces dernières semaines à ressentir à nouveau cette étincelle qui brûlait en moi, cette capacité de réflexion exceptionnelle que je tenais pour acquise. Mon cerveau fonctionne enfin !
C'est la seule chose qui ait presque soulagé mes effets secondaires du vaccin Moderna. Gastroparésie, brouillard cérébral extrême, œdème, neuropathie des petites fibres, MCAS, POTS, acouphènes, insomnie, troubles de l'humeur… tous ces symptômes s'améliorent pour la première fois en trois ans et demi !
Plusieurs autres lecteurs ont rapporté que l'application topique de DMSO sur la nuque améliorait la confusion mentale après une vaccination contre la COVID-19 1,2 , tandis que d'autres ont constaté que le DMSO par voie orale dissipait la confusion mentale induite par le zolpidem , les statines , le syndrome de fatigue chronique , un traumatisme crânien , une intoxication aux fluoroquinolones ou les symptômes persistants de la COVID-19 1,2
Mémoire
Outre le fait que la santé cérébrale (bonne circulation sanguine et inflammation minimale, ou cellules piégées dans le mécanisme de réponse au danger cellulaire) est étroitement liée au sommeil, les deux sont également liés à la santé mentale, à la cognition et à la mémoire. C'est pourquoi j'ai reçu plusieurs témoignages d'amélioration de la mémoire 1 , 2 , 3 , 4 , 5 , 6 , comme ceux-ci :
MWD, votre méthode est révolutionnaire. Nous utilisons désormais votre formule pour le potentiel zêta et avons constaté des résultats visibles en peu de temps ; c'est devenu une habitude quotidienne. Nous avons également intégré le DMSO (en application locale) et sommes émerveillés par son pouvoir réparateur et curatif (et oui, nous avons constaté des rêves lucides !). Ces deux produits constituent la base de notre trousse de premiers secours, que nous emportons partout. Merci de nous avoir transmis ce savoir. Après la pandémie, nous avons commencé à « étudier » presque par hasard, en lisant et en écoutant une quantité impressionnante d'informations, et en nous endormiant souvent pendant ce temps. Cet article explique pourquoi nous semblons retenir autant d'informations à la soixantaine, bien plus qu'à notre jeunesse .
Je suis médecin de famille et on m'a diagnostiqué un trouble cognitif léger (TCL) au service de neurologie du Mass General Hospital. J'ai réagi en adoptant une alimentation plus saine, en faisant de l'exercice quotidiennement et en prenant de nombreux compléments alimentaires, dont du DMSO par voie orale tous les jours. Ma mémoire est aujourd'hui meilleure qu'il y a des décennies.
Les bienfaits sont nombreux et remarqués… La mémoire est incroyablement bonne maintenant.
On considère généralement que le DMSO seul a un impact minimal ici (par exemple, un article indique : « Dans toutes les expériences, le diméthylsulfoxyde (DMSO) a été utilisé comme véhicule, car il n'a pas d'effet significatif sur l'apprentissage et la mémoire d'évitement passif »), de sorte qu'il existe diverses études où le DMSO a facilité un autre agent améliorant la mémoire.
Les études qui ont combiné un agent thérapeutique avec du DMSO pour améliorer l'apprentissage et la mémoire sont les suivantes :
Dans trois études différentes menées sur des rats, la pémoline (Pm) ou la pémoline magnésienne (MgPm) ont été dissoutes dans du DMSO afin d'influencer la mémoire et l'apprentissage. Dans l'une d'elles, où le nombre d'essais nécessaires à l'apprentissage d'un labyrinthe complexe était évalué chez les rats, par rapport à une valeur de référence obtenue avec une solution saline, les réductions suivantes ont été observées : DMSO seul (11,1 %), Pm (25,3 %), MgPm à faible dose (32,5 %) et MgPm à forte dose (44,6 %). L'amphétamine, quant à elle, a aggravé l'apprentissage de 14,5 %. 1,2 Dans une deuxième étude , la MgPm (à faible et à forte dose) dissoute dans du DMSO a complètement prévenu l'amnésie rétrograde induite par électrochocs (ECS). Enfin, une troisième étude a montré que ces substances n'amélioraient pas l'apprentissage par inversion (la capacité à modifier cognitivement une habitude ancrée lorsque la règle de récompense change).
À noter : il a également été démontré que le DMSO augmentait le transport de la pémoline dans le cerveau.
D'autres agents améliorant l'apprentissage ou la mémoire chez des animaux sains ou âgés comprennent la prégnénolone ⬖ (qui a amélioré l'apprentissage spatial et régulé à la hausse la choline acétyltransférase chez les rats âgés), la capsaïcine ⬖ (qui a amélioré l'acquisition et la rétention et atténué les effets négatifs d'un agoniste CB1/CB2 sur l'apprentissage), la rapamycine (qui a amélioré la reconnaissance de nouveaux objets et la mémoire de travail spatiale chez les souris d'âge moyen tout en protégeant les neurones de l'hippocampe), la testostérone (qui a presque doublé la densité des épines dendritiques de l'hippocampe via la signalisation ERK/MAPK et restauré la mémoire spatiale chez les rats gonadectomisés), 1 , 2 la nandrolone (qui a amélioré l'apprentissage spatial et la potentialisation à long terme chez les rats adolescents) et la DHEA ⬖ intracérébroventriculaire (qui a amélioré la rétention de la mémoire et prévenu l'amnésie). La datumétine a modulé la signalisation des récepteurs NMDA dans l'hippocampe et le cortex préfrontal, en augmentant la phosphorylation de CREB et l'expression de BDNF, tandis que l' extrait de sumac a amélioré l'apprentissage d'évitement passif et la rétention de la mémoire. Chez C. elegans , un découpleur mitochondrial a préservé les neurones mécanosensoriels, la mémoire à court terme et prolongé la durée de vie. L'aniracétam et le 1-BCP ont inversé les déficits de mémoire de travail induits par la pyrilamine et restauré la puissance thêta hippocampique.
Ces agents thérapeutiques (dans du DMSO) ont démontré de puissants effets protecteurs contre les troubles de la mémoire dans divers modèles de lésions. Après un AVC, la 4-méthylumbelliférone a réduit le volume de l'infarctus et amélioré l'apprentissage et la mémoire en inhibant l'expression de HAS1/HAS2, en modulant les cytokines inflammatoires et en réduisant le stress oxydatif. Chez les rats âgés, la pioglitazone a amélioré l'apprentissage et la mémoire en réduisant le stress oxydatif et en augmentant l'activité des enzymes antioxydantes dans l'hippocampe et le cortex. Chez des rats modèles de la maladie d'Alzheimer, la quercétine administrée par voie orale a significativement amélioré l'apprentissage et la mémoire spatiale tout en atténuant le stress oxydatif hippocampique et les lésions neuronales. Les agonistes des récepteurs 5-HT2A ont protégé les souvenirs à long terme de la perturbation causée par de nouveaux souvenirs formés peu après. Chez des rates ovariectomisées, modèle de déficit hormonal, un agoniste des récepteurs ERβ a inversé les déficits d'apprentissage spatial et de mémoire de référence, ainsi que les altérations de la densité des épines dendritiques et de l'intégrité structurale synaptique. Une supplémentation en œstrogènes a partiellement restauré l'apprentissage spatial et augmenté significativement l'expression de CD147 (une protéine neuroprotectrice impliquée dans la fonction synaptique et l'élimination du peptide β-amyloïde). Parmi les autres agents protecteurs contre les troubles de la mémoire, on peut citer Artemisia absinthium ( qui a inversé les déficits induits par la scopolamine et neutralisé le stress oxydatif), un agoniste des cannabinoïdes (qui a prévenu les troubles de la mémoire spatiale induits par la scopolamine), un antagoniste sélectif des récepteurs CB1 (qui a amélioré la consolidation de la mémoire associative aversive) et la 7,8-dihydroxyflavone ( qui a restauré l'apprentissage spatial chez les rates soumises au stress de la séparation maternelle).
Remarque : dans des études détaillées dans d’autres parties de cet article, des améliorations de la mémoire et de l’apprentissage ont également été démontrées par des agents combinés au DMSO dans un large éventail de modèles de lésions, notamment l’hypoperfusion cérébrale chronique ( fructose 1,6-diphosphate ⬖ ), la contention chronique et le stress psychologique ( nécrostatine-1 , flupirtine et rétigabine ), la privation de sommeil ( quercétine ⬖ et almorexant ), l’encéphalopathie associée à la septicémie ( un inhibiteur de LRRK2 ), la neurotoxicité du manganèse ( para-aminosalicylate de sodium ), l’exposition à l’anesthésie pendant la grossesse ( acide suberoylanilide hydroxamique ), l’hyperthyroïdie ( agonistes des récepteurs AMPA et NMDA ) et le blocage des récepteurs NMDA modélisant le dysfonctionnement glutamatergique ( Ptychopetalum olacoides ⬖ ), renforçant collectivement le fait que les avantages cognitifs des thérapies administrées par DMSO s’étendent à pratiquement toutes les catégories de lésions neurologiques qui altèrent la mémoire.
Enfin, dans une étude montrant que l'altération du drainage lymphatique dural (méningé) perturbe la mémoire de travail spatiale et la cohérence interhémisphérique, six semaines d'injections quotidiennes de DMSO n'ont eu aucun effet indésirable sur la mémoire.
Troubles du mouvement
Les troubles du mouvement regroupent des affections caractérisées par des mouvements volontaires ou involontaires anormaux, notamment les tremblements, l'ataxie (perte de coordination), la dystonie et la spasticité musculaire. Nombre d'entre eux résultent d'un dysfonctionnement du cervelet, des ganglions de la base ou de leurs connexions neuronales, des zones particulièrement sensibles aux perturbations circulatoires et inflammatoires que le DMSO cible (voir par exemple l'étude mentionnée précédemment sur les souris Lurcher, où le DMSO a neutralisé les lésions cérébelleuses). Par exemple :
Dans un modèle ovin de carence en cuivre , une seule injection sous-cutanée de DMSO associée à du sulfate de cuivre en milieu de gestation a totalement prévenu l'ataxie enzootique (dos creux) chez les agneaux (0 % d'incidence contre 60 % chez les témoins non traités), avec une efficacité comparable à celle de plusieurs doses orales de cuivre. Ces résultats suggèrent que le DMSO améliore suffisamment l'apport systémique de cuivre pour protéger le développement neurologique fœtal. Dans des cas cliniques vétérinaires, l'administration intraveineuse de DMSO a contribué à la guérison d'une jument atteinte d'ataxie et de déficits des nerfs crâniens dus à une ostéoarthropathie temporo-hyoïdienne (état neurologique quasi normal à la sortie de l'hôpital, le 5e jour). Chez un poulain atteint d'abiotrophie cérébelleuse , le DMSO, intégré à un traitement multi-agents, a induit une amélioration neurologique transitoire avant une rechute liée à la nature progressive de la maladie génétique sous-jacente. Chez un autre cheval , le DMSO a été utilisé pour traiter une atteinte vestibulaire et une cécité survenues suite à une complication liée à un cathéter jugulaire lors de la récupération anesthésique.
Chez les rats, un antagoniste de la neurotensine (dans du DMSO) a atténué les mouvements de mastication vides induits par les neuroleptiques (un modèle de dyskinésie tardive), soutenant un rôle de la neurotensine dans sa pathogenèse, tandis que l'acide abscissique ⬖ (dans du DMSO) a amélioré les tremblements et les performances motrices induits par l'harmaline.
Des témoignages de lecteurs suggèrent que le DMSO peut soulager plusieurs troubles du mouvement. Un lecteur atteint du syndrome de la personne raide suite à une vaccination a indiqué que l'application topique de DMSO pur à 100 % était le seul traitement capable de soulager ses spasmes musculaires constants – touchant le dos, les mollets, les pieds et la poitrine – pendant plus de 22 mois de douleurs incontrôlables, ajoutant : « Je l'ai toujours sur moi. » Un lecteur de 74 ans souffrant de tremblements essentiels , de multiples fractures vertébrales et thoraciques et d'une tendinite avancée a attribué sa survie au DMSO, et à lui seul, à son efficacité pour éviter l'utilisation d'un fauteuil roulant. D'autres lecteurs ont rapporté des améliorations de leurs tremblements essentiels , de leurs tremblements consécutifs à une vaccination et d'un tremblement du cou ayant répondu à l'application topique de DMSO.
Plusieurs lecteurs ont également signalé que l'application topique de DMSO améliorait considérablement leur syndrome des jambes sans repos, leur permettant dans certains cas d'interrompre la prise de médicaments à long terme qu'ils prenaient depuis des décennies.
De plus, plusieurs propriétaires de chiens ont rapporté que l'application topique de DMSO sur les tempes ou derrière les oreilles résolvait rapidement les épisodes vestibulaires — des événements semblables à un AVC caractérisés par une désorientation, des troubles de l'équilibre et des vomissements — l'un d'eux décrivant une guérison en moins d'une heure et une utilisation préventive continue dès la réapparition des symptômes, tandis qu'un autre a attribué au DMSO (associé à la mise à la terre) le fait d'avoir permis à son chien âgé de vivre un an et demi de plus. 1 , 2
Crises d'épilepsie
L'épilepsie est un trouble neurologique caractérisé par des crises récurrentes (décharges soudaines d'activité électrique anormale dans le cerveau pouvant provoquer des mouvements involontaires), des troubles de la conscience et, dans les cas graves, des crises prolongées entraînant des lésions cérébrales permanentes, voire le décès. La capacité du DMSO à traverser la barrière hémato-encéphalique, à contrer le stress oxydatif, à moduler les canaux ioniques et à inhiber la signalisation excitotoxique du glutamate suggère qu'il pourrait être bénéfique dans le traitement de l'épilepsie ; toutefois, comme détaillé ci-dessous, ses effets sont fortement dépendants de la dose.
Propriétés anticonvulsives
Plusieurs études ont examiné directement les effets du DMSO sur l'activité épileptique, révélant un profil biphasique constant : les doses thérapeutiques suppriment les crises tandis que les fortes doses peuvent les provoquer. Chez des rats génétiquement prédisposés à l'épilepsie, une faible dose de DMSO (1,65 mg/kg) a diminué significativement le nombre et la durée totale des décharges pointe-onde, tandis que des doses élevées (825–1651 mg/kg) les ont augmentées significativement – tous ces effets étant totalement réversibles (ce qui est corroboré par le fait que des concentrations plus élevées de DMSO commencent à bloquer les courants chlorure induits par le GABA ). De même, lorsque 50 % de DMSO ont été injectés dans les ventricules cérébraux (se diluant à environ 6 % dans le LCR), aucune activité épileptique n'a été générée au cours de l'heure suivante, alors que 75 % et 100 % ont induit un pic significatif des potentiels évoqués hippocampiques chez la souris.
Dans un autre modèle d'épilepsie du lobe temporal , une forte dose de DMSO (1651 mg/kg) a produit des effets anticonvulsivants significatifs : un allongement de 32 % de la latence d'apparition des crises, une réduction de 34 % de leur durée et une diminution de 45 % de la durée des post-décharges. Les auteurs ont attribué ces effets à la suppression de l'influx de calcium glutamatergique médié par les récepteurs NMDA/AMPA. Chez des souris atteintes d'épilepsie chronique du lobe temporal , seule une concentration de DMSO à 100 % (1651 mg/kg) a réduit le nombre et la durée cumulée des crises (de 19 à 41 % selon le sexe), tandis que des concentrations plus faibles sont restées sans effet. De manière notable, le DMSO n'a pas modifié le seuil épileptogène aigu chez les souris non épileptiques, ce qui suggère que son action anticonvulsivante est spécifique au cerveau épileptique chronique. Une autre étude a confirmé ce résultat , montrant qu'une concentration de DMSO de 10 % réduisait significativement l'activité épileptiforme induite par le PTZ, tandis qu'une concentration de DMSO à 100 % l'augmentait. Le DMSO a également augmenté les seuils de crise d'environ 9 % par rapport à deux agents convulsivants différents et a prolongé la latence des convulsions suite à une exposition à l'oxygène hyperbare (réduisant ainsi les crises).
Dans certains contextes, le DMSO a montré des effets protecteurs ciblés : il a partiellement prévenu les convulsions induites par l’acide 5-aminolévulinique (en réduisant leur nombre et leur durée), probablement grâce à la neutralisation des radicaux hydroxyles, et il a été démontré qu’un prétraitement au DMSO prévenait les décharges épileptiformes induites par le fer, suggérant un rôle potentiel dans la prévention de l’épilepsie post-traumatique.
Remarque : la réponse biphasique à la dose est un facteur important à prendre en compte lors de l’utilisation du DMSO, que ce soit à des fins thérapeutiques ou comme véhicule de recherche dans les études sur l’épilepsie. Plusieurs études ont spécifiquement documenté des effets proconvulsivants : le DMSO a prolongé les post-décharges épileptiques corticales chez les rats immatures (effet plus marqué chez les plus jeunes), abaissé le seuil des crises toniques dans un modèle de PTZ et, dans une étude, même une concentration de 0,1 % de DMSO a accéléré la sensibilisation au PTZ et potentialisé les lésions neuronales de l’hippocampe. Ces résultats soulignent l’importance du choix de la dose et de la présence de véhicules de contrôle appropriés dans la recherche sur l’épilepsie.
De plus, la capacité du DMSO à ouvrir la barrière hémato-encéphalique lui confère une propriété à double tranchant : l’administration périphérique d’acides aminés excitateurs (L-aspartate ou L-glutamate) dans du DMSO induit des crises d’épilepsie qui ne se produiraient pas autrement. Bien que cela soulève des questions de sécurité, cette propriété s’est avérée utile pour étudier l’implication des récepteurs NMDA dans les circuits épileptiques et pour démontrer le rôle crucial de l’amygdale sensibilisée dans l’expression des crises généralisées . 1,2,3,4
Réduction des crises
Les preuves cliniques les plus directes de l'efficacité du DMSO pour réduire les crises d'épilepsie proviennent de patients atteints de la maladie de Niemann-Pick de type C (décrite précédemment). Chez ces patients , l'administration orale de DMSO a diminué la fréquence des crises et amélioré les résultats de l'EEG. Plus particulièrement, chez une fillette de 8 ans présentant des crises fréquentes et une importante détérioration psychomotrice, deux années de traitement par DMSO oral ont permis de réduire suffisamment la fréquence des crises pour diminuer progressivement la posologie d'un antiépileptique, d'obtenir une nette amélioration de l'EEG (avec normalisation des ondes thêta et de la morphologie des fuseaux) et de stopper la progression de l'atrophie corticale.
En médecine vétérinaire, le DMSO intraveineux est utilisé dans le cadre d'une prise en charge multimodale des crises d'épilepsie. Chez un cheval ayant présenté des crises d'épilepsie post-opératoires, l'administration de DMSO à 10 % par voie intraveineuse (1 g/kg deux fois par jour pendant quatre jours) – pour ses propriétés antioxydantes et inhibitrices du thromboxane, afin de maintenir la vascularisation cérébrale – a permis l'arrêt des crises dès le troisième jour et une évolution favorable à long terme. Chez un poulain de deux jours souffrant d'asphyxie périnatale et présentant des crises d'épilepsie, un œdème cérébral et une insuffisance rénale aiguë, le DMSO intraveineux a permis une nette résorption de l'œdème cérébral et une récupération neurologique complète au douzième jour. Chez un poulain de trois jours présentant des convulsions et une ataxie secondaires à des troubles électrolytiques consécutifs à une rupture de la vessie, l'administration de DMSO intraveineux, intégrée aux soins de soutien, a permis la résolution des signes neurologiques en quelques jours.
Enfin, comme mentionné précédemment , un chien dont les crises d'épilepsie étaient dues à une hydrocéphalie a vu ces crises s'améliorer grâce à l'administration intraveineuse de DMSO.
Études combinées
De nombreux agents associés au DMSO ont démontré des effets anticonvulsivants ou neuroprotecteurs dans des modèles de crises d'épilepsie.
Parmi les agents réduisant directement la gravité des crises, le glibenclamide a produit les effets les plus marqués : après un état de mal épileptique, il a significativement réduit l’œdème cérébral, les lésions de la barrière hémato-encéphalique et la perte neuronale, tout en plus que doublant la survie à 28 jours (47,8 % contre 22,2 %). Le resvératrol a prolongé la latence des crises, raccourci leur durée, réduit le marqueur de lésions cérébrales S100B dans le liquide céphalo-rachidien et le sérum, protégé les neurones CA1 et CA3 de l’hippocampe et amélioré l’apprentissage spatial et la mémoire chez les rats sensibilisés au PTZ. 1,2 Le resveratrol a également protégé contre les convulsions induites par l’oxygénothérapie hyperbare. La quercétine (10–20 mg/kg) a significativement prolongé le délai d’apparition des crises, réduit leur gravité et raccourci leur durée dans les crises généralisées induites par le PTZ, bien qu’à des doses plus élevées (40 mg/kg), elle ait perdu son efficacité et, paradoxalement, raccourci le délai d’apparition des crises dans un modèle de picrotoxine. L'association de palmitoyléthanolamide (PEA) et du neurostéroïde ganaxolone dans du DMSO a considérablement amplifié la suppression des crises et éliminé la mortalité, tandis que le PEA seul s'est avéré inefficace dans ce modèle (bien qu'il ait présenté une activité anticonvulsivante lors de crises amygdaliennes induites par kindling). 1,2 Le montélukast a potentialisé l'effet anticonvulsivant du phénobarbital (lorsque les deux étaient dissous dans du DMSO), diminuant la dose efficace tout en réduisant la sédation induite par le phénobarbital. Le ruxolitinib a raccourci la durée des crises, diminué leur fréquence sur 4 semaines et amélioré la mémoire. Un inhibiteur de la p38MAPK a prolongé la latence des crises de 45 % et réduit de moitié leur fréquence. Un antagoniste des récepteurs 5-HT 6 a réduit la fréquence des crises récurrentes spontanées, augmenté l'expression du canal potassique protecteur (KCNQ2/3) et, en association avec des inhibiteurs d'ERK1/2 ou de Fyn, a inversé la prolifération aberrante des fibres moussues qui perpétue l'épilepsie chronique. 1 , 2 Le triptolide ⬖ a inhibé l'épilepsie chez les souris en améliorant l'inhibition GABAergique hippocampique et en réduisant les niveaux d'IL-1β.
Le carvédilol a supprimé l'activité épileptique spontanée dans des tranches d'hippocampe de souris modèles de la maladie d'Alzheimer — une découverte qui a des implications sur la susceptibilité aux crises fréquemment observée dans cette maladie.
Lors d'un criblage à haut débit de 343 huiles essentielles réalisé sur un modèle d'épilepsie induite par le PTZ chez le poisson-zèbre, 52 ont démontré une activité antiépileptique, dont 15 (incluant les huiles de patchouli et de cannelle ) présentant une puissance nettement supérieure à celle de la phénytoïne. L'acide maslinique , identifié par profilage bioinformatique de l'expression génique, a montré une activité antiépileptique significative dans ce même modèle et a inhibé sélectivement les sous-types de canaux sodiques voltage-dépendants Nav1.2 et Nav1.7.
De nombreux agents, associés au DMSO, ont également protégé contre les lésions neuronales consécutives à un état de mal épileptique. L'inhibiteur de la division mitochondriale 1 (Mdivi-1) a réduit de manière répétée l'apoptose neuronale et le stress oxydatif dans plusieurs études, augmentant parfois la latence des crises, diminuant leur fréquence et améliorant les fonctions cognitives post-crise.<sup> 1,2,3,4,5 </sup> L' érythropoïétine humaine recombinante a protégé les neurones de l'hippocampe via la voie de signalisation anti-apoptotique PI3K/Akt dans plusieurs modèles de crises. 1,2 L'acide ganodérique a réduit les lésions de l'hippocampe par de multiples voies (réduction de la caspase-3, modulation de CaSR/JNK/P38 et amélioration de la densité des épines dendritiques et de la mémoire spatiale). <sup> 1,2,3 </sup> Le salidroside a augmenté la latence des crises de manière dose-dépendante, renforcé les défenses antioxydantes et réduit l'apoptose induite par le stress du réticulum endoplasmique. La gastrodine a réduit la gravité des crises, protégé les neurones de l'hippocampe, augmenté l'expression des récepteurs GABA<sub>A</sub> et régulé l'autophagie post-état de mal épileptique. <sup> 1,2 </sup> Le rolipram a corrigé les déficits cognitifs, la potentialisation à long terme de l'hippocampe et la phosphorylation de CREB chez les rats immatures après un état de mal épileptique. La curcumine a diminué la prolifération aberrante des fibres moussues par la modulation de miR-134/LIMK1. Les inhibiteurs d'ERK1/2 et de p38 MAPK ont réduit les marqueurs inflammatoires, l'expression des chimiokines et l'activation microgliale dans l'hippocampe de rats immatures atteints d'épilepsie induite par l'acide kaïnique.
D'autres agents présentant des effets neuroprotecteurs dans des modèles d'état de mal épileptique incluent l'acide glycyrrhizique ( amélioration de l'autophagie mitochondriale et des défenses antioxydantes chez les rats épileptiques juvéniles), la glycyrrhizine (réduction de HMGB1/p38MAPK dans l'hippocampe), un inhibiteur d'Omi/HtrA2 (ucf-101 ; augmentation des facteurs anti-apoptotiques XIAP et HAX-1), le lévétiracétam (réduction dose-dépendante du stress oxydatif et de la caspase-3 chez les souris épileptiques issues de la descendance), un inhibiteur de la caspase-12 , l'olomoucine (un inhibiteur de CDK réduisant la neuroinflammation et l'apoptose), le 2-méthoxyestradiol (via la suppression de HIF-1α), un inhibiteur de CaMKII , l' honokiol , un donneur de sulfure d'hydrogène (via PI3K/Akt), un inhibiteur d'IRAK1/4 et un inhibiteur d'exosomes (prolongant la latence des crises). en réduisant les changements de perméabilité de la BBB), un inhibiteur de l'eEF2K qui a restauré l'expression de l'AMPKα1 et amélioré la fonction mitochondriale, la cognition et le comportement social chez les souris épileptiques chroniques, et un inhibiteur de PARP-1 (DPQ) qui a réduit l'apoptose neuronale et activé la voie de survie PI3K/Akt-SIRT1.
Il est intéressant de noter que l'activation du GPER-1 (récepteur des œstrogènes couplé aux protéines G) par le G1 a amélioré l'apprentissage spatial, la mémoire et réduit la prolifération des fibres moussues chez les rats épileptiques chroniques. Cependant, l'activation de ce même récepteur par le G-1 ou l'œstradiol a augmenté la susceptibilité aux crises aiguës et les niveaux d'oxyde nitrique dans le cortex et l'hippocampe lors de la sensibilisation au PTZ, ce qui suggère que les effets des œstrogènes sur l'épilepsie diffèrent entre la génération de crises aiguës et la récupération post-épileptique chronique.
Parmi les composés naturels ayant démontré des effets anticonvulsivants chez le poisson-zèbre ou les rongeurs, on trouve la vitexine ⬖ (comparable au diazépam), la sésamine ⬖ (via PI3K/Akt), l'onopordia ⬖ (via la voie de l'oxyde nitrique/nNOS), le linalol ⬖ et le trans-nérolidol ⬖ (le nérolidol ⬖ présentant une efficacité supérieure), l'association d'acide ursolique ⬖ et d'acide caprylique ⬖ , l'extrait de Lippia sidoides ⬖ (comparable au diazépam), les polyphénols de noyaux d'olive ⬖ (qui protègent contre la neurotoxicité induite par l'acide kaïnique), un dérivé tryptaminique de la sécurinine ⬖ (aux propriétés antioxydantes, chélatrices et anticonvulsivantes), l'ε-viniférine ⬖ (qui inhibe l'activation de l'inflammasome NLRC4 dans les astrocytes), la thymoquinone ⬖ et le progabide (qui, spécifiquement , La lamotrigine, associée à l'anakinra, a partiellement normalisé les troubles psychoneurologiques (anxiété, activité locomotrice, comportement social) chez des rats épileptiques chroniques, ce qui suggère que leur association permet de contrôler à la fois les crises et les comorbidités comportementales.
La rapamycine combinée au pitolisant a nettement amélioré l'anxiété (2,7 fois au test du labyrinthe) et la dépression (amélioration de 37,5 % au test de nage) chez les rats épileptiques sensibilisés au PTZ, soulignant que les agents administrés par DMSO peuvent traiter les comorbidités psychiatriques qui accompagnent fréquemment l'épilepsie.
Dans les modèles de toxicité des stimulants , le MK-801 dissous dans du DMSO a aboli les post-décharges EEG et les crises induites par la cocaïne, l'amphétamine et la méthamphétamine — bien que, de manière notable, l'élimination des crises n'ait pas empêché la mort due à la méthamphétamine ou à la cocaïne, démontrant que les voies de toxicité indépendantes des crises entraînent la létalité des stimulants.
Remarque : Le CBD ⬖ dans le DMSO a bloqué les canaux sodiques voltage-dépendants et a démontré des effets anticonvulsivants dans un modèle PTZ, tandis que le cannabigérol a produit un blocage comparable des canaux sodiques mais sans effet anticonvulsivant, indiquant que l’inhibition des canaux sodiques seule ne confère pas de protection contre les crises. Le 3-carène ⬖ a modulé l’activité cérébrale au repos mais n’a pas réduit l’activité épileptiforme. La rétigabine , bien qu’étant un antiépileptique reconnu, a paradoxalement augmenté le nombre et la durée des décharges pointe-onde chez les rats WAG/Rij âgés, révélant des effets pro-épileptiques dépendants de l’âge dus à l’activation des canaux potassiques neuronaux. Deux extraits de plantes (Searsia dentata ⬖ et Searsia pyroides ⬖ ) ont inhibé les courants des récepteurs NMDA et réduit l’influx de calcium intracellulaire, confirmant leur utilisation traditionnelle dans le traitement de l’épilepsie.
Interactions entre le DMSO et les médicaments antiépileptiques
Plusieurs résultats sont pertinents quant à l'utilisation du DMSO en association avec les antiépileptiques conventionnels. Le DMSO a été utilisé sans danger comme excipient pour le diazépam dans des études sur le traitement des crises d'épilepsie. Les antiépileptiques carbamazépine et lamotrigine dissous dans du DMSO n'ont montré aucune interaction préoccupante sur les tissus reproducteurs humains, suggérant une compatibilité pendant la grossesse. Une étude pharmacologique a démontré des interactions moléculaires favorables entre le lévétiracétam et des mélanges eau-DMSO, confirmant l'intérêt potentiel du DMSO dans la formulation de médicaments antiépileptiques. Les antiépileptiques stabilisateurs de l'humeur (zonisamide, carbamazépine, valproate) dissous dans du DMSO ont augmenté l'activité des systèmes monoaminergiques et cholinergiques dans le striatum et l'hippocampe aux doses thérapeutiques, tout en la diminuant aux doses suprathérapeutiques — un profil biphasique qui pourrait expliquer en partie leurs effets thérapeutiques et certains effets indésirables. L'association de DMSO et d'éthosuximide pourrait augmenter de façon synergique les concentrations d'adrénaline cérébrale, car le DMSO seul peut stimuler le système nerveux central et accroître la production de catécholamines, renforçant potentiellement les modifications des neurotransmetteurs induites par l'antiépileptique. Le menthol dissous dans le DMSO a démontré des effets anticonvulsivants dose-dépendants : à la dose de 400 mg/kg, l'activité épileptique est significativement réduite en dessous des niveaux témoins, tout en contrant l'effet proconvulsivant du DMSO à forte concentration. Ces résultats suggèrent que le menthol pourrait être un adjuvant utile lorsque le DMSO est utilisé comme excipient pour les médicaments antiépileptiques.
Remarque : plusieurs études ont confirmé que le DMSO , aux concentrations utilisées dans le véhicule, n’avait aucun effet indépendant sur les paramètres des crises d’épilepsie, ce qui confirme son innocuité en tant que solvant aux doses appropriées. <sup> 1,2,3 </sup> Une étude utilisant la spectroscopie de résonance paramagnétique électronique (RPE) avec le DMSO a démontré que les crises d’épilepsie induisent une accumulation rapide d’ascorbate (un antioxydant) dans l’hippocampe, parallèlement à la progression des crises – probablement en réponse à une production excessive de radicaux libres lors de l’excitotoxicité – ce qui explique pourquoi des antioxydants comme le DMSO peuvent être neuroprotecteurs dans le contexte des crises d’épilepsie.
Encéphalite
En plus d'atténuer l'encéphalomyélite auto-immune expérimentale, le DMSO atténue également l'inflammation cérébrale déclenchée par diverses sources infectieuses.
Encéphalite virale
Du DMSO administré par voie intranasale, mélangé à un mélange de nucléases, a été utilisé chez des patients humains pour traiter les méningites et les méningo-encéphalites causées par des infections respiratoires virales aiguës. 1 , 2
Plusieurs articles ont mentionné l'utilisation du DMSO chez les chevaux pour traiter la myéloencéphalopathie herpétique, mais aucune donnée n'a été fournie, si ce n'est l'administration de traitements plus longs lors des crises les plus sévères. <sup> 1,2 </sup> Dans le seul cas rapporté que j'ai trouvé, l'administration de 500 mg/kg de DMSO par voie intraveineuse (toutes les 24 heures à un cheval hospitalisé) a permis de stabiliser les déficits neurologiques, d'observer une amélioration clinique, puis une guérison complète.
Plusieurs articles ont rapporté que le DMSO était utilisé pour traiter l'encéphalomyélite suspectée du virus du Nil occidental, 1 , 2 dont l'un a rapporté que des cas légers à modérés se sont complètement rétablis après un protocole anti-inflammatoire qui comprenait du DMSO.
L'administration intrapéritonéale d'arctigénine β (un
lignane végétal dissous dans du DMSO), un jour après une infection
intraveineuse, a conféré une protection complète aux souris contre une
infection par le virus de l'encéphalite japonaise, autrement mortelle
(tout en réduisant l'inflammation cérébrale, le stress oxydatif, la mort
cellulaire et les troubles comportementaux associés).
Chez des souris atteintes
d'une infection virale d'encéphalomyocardite (EMCV) 100 % fatale,
l'administration intrapéritonéale de DMSO combinée à un dérivé de la
DHEA a réduit la mortalité à 72,73 %, atténué considérablement les
symptômes neurologiques (par ailleurs sévères), prévenu les lésions
inflammatoires cérébrales et diminué la charge virale cérébrale. Dans une autre étude, le
DMSO combiné à un inhibiteur de la furine ou à un autre dérivé de la
DHEA a démontré une forte activité antivirale contre les virus Zika et
de l'encéphalite japonaise dans des cellules humaines et de moustiques.
Un inhibiteur de p38-MAPK dissous dans du DMSO a amélioré le taux de survie, réduit les scores de paralysie, diminué la charge virale dans les muscles squelettiques et diminué les cytokines inflammatoires chez les souris allaitantes infectées par l'entérovirus 71.
Chez les chiens atteints de maladie de Carré neurologique , le DMSO, seul ou en association avec la ribavirine et la prednisone, a permis de maintenir des taux d'hémoglobine plus élevés et de réduire la gravité de l'anémie par rapport aux traitements sans DMSO. Dans une autre étude similaire , le DMSO a potentialisé l'efficacité du traitement par la ribavirine.
Encéphalite parasitaire
La myéloencéphalite protozoaire équine (EPM) est une maladie fréquente et grave chez les chevaux, difficile à traiter en raison de la faible absorption orale des médicaments. Une étude de 2009 a montré que la dissolution du ponazuril dans du DMSO plutôt que dans l'eau triplait approximativement sa biodisponibilité et améliorait sa capacité à atteindre le cerveau, ce qui pourrait révolutionner la prise en charge de l'EPM. <sup> 1,2 </sup> Une autre étude a également démontré que le DMSO améliorait considérablement l'absorption du toltrazuril (la biodisponibilité du toltrazuril administré par voie orale atteignant 56 % de celle du toltrazuril administré par voie intraveineuse). Dans le seul cas clinique rapporté que j'ai pu trouver, un dysfonctionnement neurologique sévère dû à une EPM s'est initialement amélioré après l'administration de DMSO et de ponazuril, ainsi que de quelques autres traitements, mais le cheval âgé a finalement succombé à la maladie. Enfin, un article vétérinaire de 2014 a indiqué que l'administration intraveineuse de DMSO et de ponazuril constituait un traitement viable de l'EPM.
Le Megazol, formulé sous forme de gel dans du DMSO et combiné avec du mélarsoprol, a permis de guérir avec succès la trypanosomiase expérimentale du SNC chez la souris.
L'arctigénine a amélioré les comportements de type dépressif chez les souris infectées par Toxoplasma gondii, réduit la neuroinflammation et rétabli l'équilibre des neurotransmetteurs en inhibant la voie TLR4/NF-κB et la surexpression d'IDO. La sertraline a également inhibé la prolifération cérébrale de Toxoplasma gondii, réduit la neuroinflammation (TNF-α, TRAF2, translocation nucléaire de NF-κB p65) et protégé les neurones dans des modèles in vitro et in vivo d'infection aiguë à T. gondii. <sup> 1,2 </sup>
Une complication rare chez les chiens atteints de babésiose est l'ataxie cérébelleuse, et dans un cas où celle-ci était accompagnée de cécité et de tétraparésie, une dose de DMSO par voie intraveineuse, puis d'autres traitements, ont précédé une guérison rapide.
Deux espèces d'Acanthamoeba (responsables d'infections oculaires et, occasionnellement, d'encéphalites) se sont révélées environ deux fois plus sensibles (et dans un cas, quatre fois plus sensibles) à l'huile d'arbre à thé lorsqu'elle était mélangée à du DMSO. La croissance d'une autre amibe (utilisée comme modèle de l'amibe N. fowleri, responsable d'infections cérébrales mortelles) a été inhibée par le Torin-1 dissous dans du DMSO.
Note : un article de synthèse citant de nombreux manuels vétérinaires des années 1990 a déclaré que le DMSO a été indiqué dans les cas d'encéphalite virale et bactérienne, d'herpès virus I et de myélite due à des protozoaires [parasites].
Méningite bactérienne.
Une étude russe a rapporté que chez l'homme, le DMSO améliorait l'efficacité des protocoles de traitement de la méningite. 1 , 2
Chez un poulain présentant une suspicion de méningite bactérienne ,
l'administration intraveineuse de DMSO a été intégrée au traitement de
soutien intensif pour ses propriétés anti-inflammatoires, analgésiques,
neuroprotectrices et antioxydantes. Le poulain a présenté une
amélioration clinique (récupération du réflexe de succion et de la prise
de lait) entre le 7e et le 8e jour, date à laquelle l'administration de
DMSO a été interrompue.
Encéphalopathie associée à une septicémie
Lorsque les infections atteignent la circulation sanguine, elles peuvent fréquemment déclencher une septicémie, une réaction inflammatoire en chaîne potentiellement mortelle. Comme une toxine présente chez de nombreuses bactéries (LPS) peut induire une septicémie, cette affection est souvent étudiée chez l'animal par injection de LPS.
L'un des organes touchés par la septicémie étant le cerveau (par exemple, l'encéphalopathie septique est de loin la forme d'encéphalopathie la plus courante chez les patients gravement malades), de nombreuses études ont évalué comment des agents protègent le système nerveux contre la septicémie, comme une étude sur des moutons où le DMSO intraveineux a considérablement réduit les signes cliniques de la septicémie et abaissé les niveaux de protéines de la phase aiguë (haptoglobine, amyloïde sérique A, céruloplasmine et fibrinogène).
Il a également été démontré que divers agents, en association avec le DMSO, réduisent les lésions cérébrales déclenchées par le LPS :
• Chez le rat, le prétraitement à la dexmédétomidine a réduit l'inflammation systémique et cérébrale dans l'encéphalopathie liée à la septicémie en diminuant les cytokines inflammatoires et en supprimant la signalisation NF-κB dans l'hippocampe.
• L’ibrutinib a réduit la neuroinflammation et les lésions cérébrales chez les souris en diminuant les cytokines pro-inflammatoires (TNF-α, IL-6, IL-1β), en augmentant l’IL-10 et en supprimant la voie inflammatoire TLR4/AKT/PI3K/STAT3.
•Le dasatinib a réduit la neuroinflammation et les lésions cérébrales chez la souris en diminuant plusieurs médiateurs pro-inflammatoires et en modulant des voies de signalisation clés, tout en augmentant la cytokine anti-inflammatoire IL-10. 1 , 2
• L’astaxanthine ⬖ a réduit l’inflammation systémique , les marqueurs de lésions cérébrales, le stress oxydatif et l’œdème cérébral tout en améliorant l’activité antioxydante et les dommages histopathologiques chez les rats.
• La dexaméthasone a réduit l'inflammation cérébrale et systémique et a atténué les comportements de maladie (hypophagie) chez les souris.
• L’acétate d’incensole ⬖ a amélioré l’apprentissage et la mémoire, réduit la neuroinflammation et le stress oxydatif, et augmenté les défenses antioxydantes et le BDNF chez les rats exposés au LPS.
• La pioglitazone a inversé la neurotoxicité de l'hippocampe du rat en réduisant la signalisation inflammatoire et apoptotique (p-JNK, pc-Jun, Caspase-3) et en restaurant les voies protectrices (p-Akt et p-p70S6K).
• La ziprasidone (dans du DMSO) a réduit l'activation microgliale et le stress oxydatif chez le rat.
• La rapamycine dissoute dans du DMSO a augmenté la consommation alimentaire et réduit la signalisation métabolique inflammatoire et hypothalamique chez les poulets.
• Un inhibiteur de LRRK2 a réduit l'inflammation microgliale et les voies de mort cellulaire in vitro, et a amélioré les lésions neuronales, la polarisation microgliale et les performances cognitives chez les rats.
• Le glibenclamide a partiellement amélioré la pathologie du tissu cérébral et l'expression de la protéine basique de la myéline chez les rats nouveau-nés présentant une lésion cérébrale induite par une infection intra-utérine provoquée par le LPS (ce qui a une pertinence clinique, car l'étude a également révélé que les nourrissons prématurés nés de mères présentant une infection intra-utérine subclinique avaient des résultats neurodéveloppementaux moins bons).
De plus, le DMSO a empêché la perturbation de la communication par jonctions communicantes induite par le LPS dans les astrocytes de rat en piégeant les radicaux hydroxyles provenant du peroxynitrite. Plusieurs autres composés ont également démontré des effets protecteurs dans des modèles gliaux et neuronaux stimulés par le LPS :
L'icariine ⬖ a réduit l'activation des astrocytes et la production de cytokines inflammatoires (TNF-α et IL-1β) dans les astrocytes primaires.
La génistéine ⬖ a réduit le TNF-α et l'IL-1β induits par le LPS dans les cellules microgliales BV2 via un mécanisme dépendant du récepteur des œstrogènes.
L'acétate d'incensole ⬖ a réduit la neuroinflammation et le stress oxydatif, et a augmenté les défenses antioxydantes et le BDNF.
L'acide chlorogénique ⬖ a réduit plusieurs cytokines pro-inflammatoires (TNF-α, IL-1β, IL-6, IL-12), diminué la signalisation iNOS, NLRP3 et NF-κB, tout en augmentant l'IL-10.
L'ibrutinib a supprimé l'oxyde nitrique, le TNF-α, la sénescence cellulaire, la signalisation TLR4/NF-κB et les espèces réactives de l'oxygène.
L’icaritine a protégé les neurones et, dans une autre étude, les astrocytes des dommages induits par les cellules gliales activées par le LPS, via un mécanisme dépendant de l’IGF-1R et en réduisant les cytokines inflammatoires. <sup> 1,2 </sup>
L'acide asiatique a protégé les neurones hippocampiques primaires de la toxicité induite par le LPS en réduisant le TNF-α et l'IL-1β, en diminuant le stress oxydatif et en activant la voie Nrf2/HO-1 tout en inhibant NF-κB. Ses effets protecteurs ont été partiellement bloqués par un inhibiteur de Nrf2.
Enfin, l'hélénaline ⬖ a réduit significativement la destruction osseuse crânienne induite par le LPS.
Remarque :
lors d'interventions neurochirurgicales d'urgence, les fragments osseux
du crâne prélevés sont souvent congelés en vue d'une réinsertion
ultérieure. Dans 39 cas de ce type , les os congelés avec du DMSO ont présenté une résorption moindre et de meilleurs résultats que ceux congelés sans DMSO.
Encéphalopathie
Outre les agents pathogènes qui provoquent directement des lésions cérébrales inflammatoires, divers autres facteurs peuvent également induire une encéphalopathie. Le DMSO, seul ou en association avec d'autres agents, a montré un potentiel bénéfique contre plusieurs d'entre eux (par exemple, cet article russe cite le DMSO comme méthode de traitement de l'encéphalopathie).
L'ébsélène (dissous dans du DMSO ) a réduit les symptômes du stress oxydatif et nitratif dans un modèle de rat d'encéphalopathie hépatique induite par le thioacétamide.
Dans une revue de 2015 ,
le DMSO a été proposé comme traitement potentiel de la
polioencéphalomalacie bovine d'origine naturelle. Cette hypothèse
reposait sur la plausibilité de son mécanisme d'action, le succès de son
utilisation par certains vétérinaires et le manque général de preuves
solides concernant les options thérapeutiques pour cette affection.
Cette maladie résulte souvent d'une carence en thiamine , répond à des degrés variables à des perfusions intraveineuses répétées de thiamine à haute dose et présente des similitudes symptomatiques avec l'encéphalopathie de Wernicke, une carence en thiamine observée
chez l'humain (en particulier chez les alcooliques), ce qui suggère que
le DMSO pourrait être utile dans cette pathologie. Confirmant cette hypothèse , dans un modèle murin de carence en thiamine développé en 2021 , le
DMSO (administré par voie intrapéritonéale) a partiellement amélioré
les déficits comportementaux et réduit les lésions thalamiques (une
région clé affectée dans l'encéphalopathie de Wernicke). Associé à de
fortes doses de thiamine, le DMSO
a amélioré la récupération de la fonction locomotrice, de la
coordination motrice et de la viabilité des cellules thalamiques, comparativement à la thiamine seule , et a contribué à minimiser les séquelles neurologiques à long terme. Remarque : les interactions chimiques du DMSO avec la thiamine ( par exemple, pour améliorer l’administration de thiamine ) ont également fait l’objet de nombreuses études. <sup> 1,2,3 </sup>
Dans un groupe de chevaux ayant développé une leucoencéphalomalacie due aux mycotoxines de Fusarium moniliforme présentes dans leur nourriture, une thérapie combinée au DMSO visant à réduire l'œdème cérébral a réduit de moitié leur taux de mortalité (de 66 % à 33 %) et a permis aux chevaux survivants de se rétablir complètement.
Myasthénie grave
Pour que les muscles squelettiques se contractent, ils doivent recevoir de l'acétylcholine du nerf qui les innerve. Dans la myasthénie grave (MG), l'organisme produit des anticorps dirigés contre les récepteurs de l'acétylcholine (AChR) des muscles. À mesure que ces récepteurs sont détruits, les muscles ont besoin de quantités croissantes d'acétylcholine, transmises par les nerfs, pour s'activer. La MG est prise en charge par divers médicaments immunosuppresseurs, qui éliminent les anticorps anti-AChR du sang, et par des inhibiteurs de l'acétylcholinestérase (qui augmentent les taux d'acétylcholine). Ces observations suggèrent que les propriétés anti-inflammatoires et d'augmentation des AChR du DMSO (via l'inhibition de l'acétylcholinestérase ) pourraient être bénéfiques pour les patients atteints de cette maladie.
Le potentiel du DMSO dans le traitement de la myasthénie grave a été découvert initialement (par hasard) en 1980, lorsque deux chercheurs testaient divers agents pour leur capacité à réduire les anticorps anti-récepteurs de l'acétylcholine (AChR). Ils ont alors constaté que le DMSO, utilisé comme excipient pour ces agents, réduisait indépendamment ces anticorps. Ils ont ensuite observé que l'administration quotidienne d'injections intrapéritonéales de 1 mL de DMSO à des rats pendant deux semaines entraînait une diminution de 52 % des anticorps anti-AChR (mais pas du taux d'IgG totales), diminution qui persistait pendant six semaines supplémentaires après l'arrêt du traitement. <sup> 1,2 </sup>
Note : après cette découverte, les chercheurs ont exprimé leur vif désir de tester le DMSO chez l'homme atteint de MG ( le New York Times en a même parlé ).
Une étude de suivi menée sur des rats a ensuite révélé que le DMSO diminuait les taux d'anticorps anti-AChR de 53 % à 76 % en moyenne, cet effet étant similaire quelle que soit la voie d'administration (orale, rectale ou intrapéritonéale). De plus, le traitement au DMSO supprimait la réponse des anticorps anti-AChR à une stimulation antigénique primaire faible. Fait intéressant, administré lors de fortes réponses immunitaires primaires ou secondaires, le DMSO augmentait au contraire la production d'anticorps de 1,7 à 2,8 fois, ce qui indique une modulation immunitaire bidirectionnelle dépendant du moment et de l'intensité de la stimulation (ou de la capacité du DMSO à potentialiser les allergènes).
Ces résultats concernant les anticorps ont été complétés par des preuves directes démontrant que le DMSO restaure la fonction neuromusculaire. Dans des préparations neuromusculaires ex vivo de souris, où la tubocurarine a été utilisée pour simuler la myasthénie grave (réduisant la force des contractions musculaires induites par stimulation nerveuse), le DMSO a induit une restauration rapide, dose-dépendante et durable de la force de secousse : une concentration de 0,1 % a permis de restaurer 20 à 30 % de la force, tandis qu’une concentration de 0,75 % a permis une restauration complète qui s’est maintenue pendant plus de 150 minutes. L’électrophysiologie a confirmé que le DMSO augmentait l’amplitude des signaux nerveux au niveau du muscle d’environ 25 à 30 %, ce qui concorde avec ses propriétés inhibitrices de l’acétylcholinestérase.
Des études complémentaires sur des préparations neuromusculaires de grenouille et de mammifères ont confirmé que le DMSO, à des concentrations ≤ 1 %, améliorait la transmission neuromusculaire par inhibition de l'acétylcholinestérase, tandis que des concentrations supérieures à 1 % commençaient à avoir des effets dépresseurs chez les mammifères. Le THC (mais pas le CBD) a contrecarré cette restauration de la fonction neuromusculaire. <sup> 1,2,3,4 </sup> Il a également été démontré que le DMSO inverse le blocage neuromusculaire induit par les organophosphorés ( qui inhibent le même système acétylcholinestérase que celui ciblé thérapeutiquement dans la myasthénie grave ) . <sup> 1,2,3,4,5,6 </sup>
Note : ces recherches ont inspiré une étude menée en 1982 visant à déterminer si le DMSO supprimait les auto-anticorps thyroïdiens (induits expérimentalement chez le rat). Ce fut le cas, et le DMSO augmentait également le rapport IgM/IgG dans les cellules formant des plaques (ce qui suggérait un véritable effet immunorégulateur). Par ailleurs, certains patients rapportent que le DMSO améliore leur thyroïdite auto-immune.
Divers agents combinés au DMSO ont également montré des effets bénéfiques dans des modèles expérimentaux de MG auto-immune, notamment le resvératrol ⬖ (qui a réduit les anticorps anti-AChR et protégé la densité d'AChR à la jonction neuromusculaire), les glucosides totaux de pivoine ⬖ et l'artémisinine ⬖ (qui ont tous deux réduit les scores cliniques et les anticorps anti-AChR tout en modulant les cellules T régulatrices), les exosomes dérivés de l'atorvastatine, 1 , 2 , 3 et un inhibiteur de la caspase-1 (qui a supprimé la progression de la maladie via les voies IL-1β/IL-17).
Par ailleurs, la perturbation de l'agrégation des récepteurs de l'acétylcholine sur les cellules musculaires induite par la septicémie a été inversée par l'inhibition de la GSK3β, restaurant ainsi l'agrégation des récepteurs nécessaire à une transmission neuromusculaire normale. <sup>1,2 </sup> Dans un modèle de septicémie chez le rat, la rapamycine a également amélioré la vitesse de conduction nerveuse, l'amplitude du potentiel d'action musculaire et la survie en restaurant l'homéostasie des récepteurs de l'acétylcholine.
Malheureusement, bien que des médecins aient souligné le potentiel du DMSO pour les patients , aucune étude clinique n'a été menée sur son utilisation chez les personnes atteintes de myasthénie grave (MG). Cependant, une lectrice souffrant de MG généralisée a rapporté qu'après avoir commencé un traitement par DMSO oral et topique en 2022, sa fatigue musculaire, ses fonctions cognitives et sa vision se sont considérablement améliorées, et elle n'a plus présenté de crise myasthénique depuis. Elle a noté que des doses plus élevées prises le soir lui permettaient de se réveiller une heure plus tard, alerte et en pleine forme – ce qu'elle a attribué à l'augmentation de son taux d'acétylcholine grâce au DMSO – et a décrit cet effet comme « meilleur que celui de la pyridostigmine que je prenais six fois par jour ». Une autre lectrice, également atteinte de MG généralisée et de plusieurs autres maladies auto-immunes, n'a rapporté aucune crise myasthénique depuis le début de son traitement par DMSO en 2022, ainsi qu'une réduction spectaculaire de sa fatigue musculaire, une nette amélioration de ses fonctions cognitives et une vision quasi normale – après avoir pris 30 médicaments sur ordonnance, elle n'en prend presque plus aucun. <sup> 1,2 </sup>
Hydrocéphalie
Le liquide céphalo-rachidien (LCR) est principalement produit et circule dans des cavités du cerveau appelées ventricules. En cas de production excessive de LCR, d'obstruction de son drainage ou de son écoulement hors des ventricules (ou d'altération de son absorption), les ventricules se dilatent et exercent une pression sur les tissus cérébraux environnants. Ceci peut entraîner des troubles cognitifs (y compris des symptômes apparentés à la démence), des troubles de la coordination ou de la marche, et une incontinence urinaire. Le DMSO, en facilitant la circulation et le drainage du liquide, pourrait potentiellement être bénéfique en cas d'hydrocéphalie.
Malheureusement, les recherches dans ce domaine sont assez limitées. Les études principalement citées proviennent d'une équipe qui a constaté que la lésion des ventricules (par perforation suivie d'injection de DMSO) provoquait une hydrocéphalie dose-dépendante : une concentration de 2 % de DMSO entraînait une légère augmentation du volume ventriculaire (8 à 16 % des patients développaient une hydrocéphalie, soit une augmentation moyenne de 50 %), tandis que des concentrations de 10 % ou 100 % la provoquaient beaucoup plus fréquemment. Ces résultats ont conduit les auteurs à émettre l'hypothèse que l'effet observé pourrait expliquer pourquoi une hydrocéphalie est parfois constatée suite à d'autres thérapies impliquant l'injection de fortes concentrations de DMSO dans la circulation cérébrale . <sup> 1,2,3 </sup>
Étant donné que ces concentrations sont beaucoup plus élevées que celles qui peuvent être atteintes avec des perfusions standard de DMSO (sans parler de toute autre voie d'administration) et que les injections intraventriculaires de diverses substances autres que le DMSO provoquent de manière fiable une hydrocéphalie, il est peu probable que ces résultats soient pertinents pour les utilisateurs de DMSO, surtout si les perfusions intraveineuses de DMSO à forte dose sont évitées.
En dehors de cette étude, deux rapports de cas suggèrent que le DMSO peut être bénéfique en cas d'hydrocéphalie :
Chez un chien Shih Tzu présentant des symptômes neurologiques aigus sévères (par exemple, crises d'épilepsie et opisthotonos) dus à une hydrocéphalie non communicante, l'administration intraveineuse de DMSO à 10 % (1 g/kg sur 50 minutes) a permis une nette amélioration des symptômes (par exemple, les crises d'épilepsie ont été largement supprimées et la conscience a été rétablie). Les auteurs ont attribué cette amélioration à la réduction de la pression intracrânienne et à la protection du tissu neurologique par le DMSO. Le chien est finalement décédé 50 jours plus tard, mais son pronostic s'est avéré bien meilleur que prévu. <sup> 1,2 </sup>
• Une encéphalopathie cérébrale diffuse associée à une hydrocéphalie et à des granulomes cholestériiques [à cholestérol] chez un cheval a présenté une amélioration partielle grâce à un traitement à base de DMSO. Chez un cheval présentant un volumineux kyste épidermoïde intracrânien provoquant ataxie, pression de la tête et mouvements circulaires, l'administration intraveineuse de DMSO associée à des glucocorticoïdes et à de la pénicilline a induit une amélioration clinique progressive (malgré une rechute survenue six mois plus tard en raison de la nature progressive de la lésion).
En revanche, dans une étude sur l'hydrocéphalie induite expérimentalement où le DMSO a été utilisé pour administrer un inhibiteur de l'aquaporine 4 (qui a aggravé l'hydrocéphalie), le DMSO intrapéritonéal (à une dose non spécifiée) n'a pas apporté de bénéfice thérapeutique.
Enfin, un lecteur a partagé l'histoire de son frère, atteint d'une maladie neurologique progressive (syringomyélie, astrocytome cervical ayant entraîné une paralysie, complications suite à son ablation complexe, puis hydrocéphalie). Ses neurologues (de renom) avaient finalement déclaré que son état serait fatal en quelques années (probablement à cause d'une encéphalite). Il s'est alors tourné vers Stanley Jacob, qui a accepté de le traiter expérimentalement avec du DMSO. Ce traitement s'est avéré miraculeux pour lui et sa moelle épinière. Ses neurologues ont déclaré n'avoir jamais vu un cas similaire se stabiliser, un événement historique. Il a vécu trente années supplémentaires heureuses, dont vingt en tant que patient de Stanley Jacob. Malheureusement, le DMSO par voie intraveineuse lui a été le plus bénéfique, et il n'a plus pu y avoir accès après avoir cessé d'être suivi par Jacob.
Note : un autre lecteur , dont la fille de 9 ans souffre de paralysie cérébrale (et porte une valve de dérivation pour hydrocéphalie), a indiqué que l'application topique de DMSO atténuait les symptômes de la paralysie cérébrale.
affections psychiatriques
Examinons maintenant le reste des données accumulées concernant l'utilisation du DMSO en psychiatrie et notons à quelle fréquence elles reflètent les conclusions des chercheurs russes.
Études humaines
L’étude la plus détaillée sur l’utilisation du DMSO chez les patients psychiatriques a été menée dans un hôpital psychiatrique péruvien. Quarante-deux patients (25 schizophrènes, 4 maniaco-dépressifs, 4 alcooliques, 4 névrosés obsessionnels-compulsifs et 5 patients souffrant d’anxiété sévère) ont été sevrés de tous leurs médicaments, puis ont reçu 2 à 5 injections intramusculaires de DMSO par jour (avec un nombre plus élevé pour les patients les plus psychotiques). Leurs résultats ont été comparés à ceux de 16 sujets témoins recevant les soins standards. <sup> 1,2 </sup>
Parmi les schizophrènes, les 14 cas aigus ont tous connu une amélioration rapide et spectaculaire (notamment de leur agitation, surtout chez les patients catatoniques-paranoïdes), et tous ont pu quitter l'hôpital dans les 45 jours (trois d'entre eux ayant guéri complètement 15 jours après leur admission), sans aucune rechute. L'un d'eux a déclaré :
« J’ai perdu la raison. Je ne sais pas ce qui m’est arrivé. Je me demande ce que mes enfants vont dire. »
Parmi les 11 patients atteints de schizophrénie chronique, 4 ont nécessité des hospitalisations périodiques et ont connu une rémission complète après la prise de DMSO (ce qui leur a permis de sortir de l'hôpital beaucoup plus rapidement que prévu). Chez ceux qui ont rechuté par la suite, on a de nouveau observé une réponse positive au DMSO. Les 7 autres patients présentaient des cas plus graves (par exemple, ils avaient été hospitalisés pendant plus de 6 ans et avaient connu des années d'échec thérapeutique) et ont constaté une amélioration grâce au DMSO, mais celle-ci n'a pas été suffisante pour permettre leur sortie de l'hôpital.
Remarque : des résultats comme ceux-ci (j’en ai observé de similaires avec d’autres thérapies) me laissent penser que notre compréhension actuelle de la schizophrénie est loin d’être complète. Pour étayer cette affirmation, cet auteur a également présenté le cas d’un patient schizophrène paranoïde souffrant de délires sévères et ayant répondu au DMSO.
Les 4 psychotiques maniaco-dépressifs (qui étaient en phase maniaque, avec en moyenne 15 jours d'agitation psychomotrice) se sont rapidement calmés et ont perdu leur manie après le DMSO (leur rétablissement étant beaucoup plus rapide que ce qu'ils avaient connu auparavant avec une thérapie conventionnelle).
Les
quatre patients alcooliques psychotiques (deux présentant des
hallucinations et deux un delirium tremens) avaient déjà été
hospitalisés pour ces troubles. Ils ont rapidement répondu au DMSO :
leur agitation s’est atténuée dès les premiers jours, tandis que les
hallucinations ont mis plus de temps à disparaître.
Les
autres patients (névrose obsessionnelle-compulsive et anxiété sévère)
ont également bien répondu au DMSO (ils étaient plus calmes, les idées
les perturbaient moins, ils agissaient plus spontanément et ils
parvenaient à maîtriser leurs compulsions obsessionnelles).
Note : les auteurs de l’article de 1967 ont noté que le DMSO possédait des propriétés antipsychotiques et anxiolytiques et que son action différait de celle des tranquillisants, car elle induisait peu de sédation ou de dépression centrale. Un article ultérieur, paru en 1992, a suggéré que les effets antipsychotiques observés lors de cet essai résultaient de la suppression par le DMSO d’une production excessive d’interleukine-2 (IL-2) par les lymphocytes T, un mécanisme également attribué à certains antipsychotiques dans le même modèle.
Malheureusement (comme beaucoup de choses en médecine), ces résultats de 1967 ont suscité un intérêt minimal et aucune tentative n'a été faite pour les reproduire (bien qu'une revue russe de 1982 ait noté que le DMSO pouvait être utilisé pour les troubles psychiatriques et qu'une revue de la littérature russe de 2006 ait noté que les injections intramusculaires de 50 % de DMSO avaient un effet sédatif sur les patients psychotiques).
À ma connaissance, seules cinq autres études psychiatriques humaines ont été réalisées avec le DMSO :
Chez 17 patients (âgés
de 28 à 55 ans) souffrant de dépression chronique (depuis au moins 5 à
20 ans) réfractaire aux antidépresseurs et dont le dernier épisode
dépressif avait duré de 8 mois à 2 ans, le DMSO s'est avéré efficace.
Plus précisément, le traitement antidépresseur de base (amitriptyline,
pirasidol, anafranil) a été associé à 1 ml de DMSO à 50 % par voie
orale, trois fois par jour. Chez 14 patients (82,3 %), la dépression a
disparu et cette amélioration s'est maintenue pendant les 1 à 4 années
de suivi.
Remarque : les études évaluant l'association du DMSO et des antidépresseurs ISRS sont rares. L'une des rares que j'ai trouvées a montré une diminution de l'appétit pour le sucre chez le rat, tandis que dans une autre ( une étude cardiaque ),
les effets observés se sont produits à des concentrations bien
supérieures à celles atteintes dans le sang d'un utilisateur d'ISRS.
• Une étude menée auprès de 210 femmes souffrant d'une parodontite chronique généralisée exacerbée a révélé que 10 % de DMSO mélangés à 0,2 % d'oxymétacil et administrés par ultrasons soulageaient efficacement leur parodontite et réduisaient leur anxiété.
• Dans deux études chiliennes, une combinaison de DMSO et d'acides aminés a été utilisée pour traiter les névroses dépressives (par exemple, les troubles de l'humeur et l'anxiété), tandis que dans une autre, lorsqu'elle a été utilisée pour traiter les troubles cognitifs et la démence, les patients ont également constaté une amélioration significative de leur humeur (passage d'un état dépressif à un état de bien-être). 1 , 2
Chez les femmes souffrant de dépression post-partum (DPP),
les analyses sanguines ont systématiquement révélé des taux
significativement plus faibles de vitamine D, de sérotonine et de
noradrénaline. L' administration
de vitamine D dans du DMSO à des neurones hippocampiques en culture a
induit une augmentation de leur prolifération ainsi que de la sécrétion
de sérotonine et de noradrénaline (probablement via la voie PI3K/Akt). À noter : dans les lymphoblastoïdes de femmes atteintes de DPP ,
le bréxanolone (un traitement approuvé pour la DPP) dans du DMSO a
modulé l'expression de 98 gènes potentiellement liés à la DPP (ce qui
expliquerait son effet rapide sur la DPP).
Cependant, diverses études sur des animaux ont été et seront résumées (toutes, sauf indication contraire, ont été réalisées sur des rats ou des souris).
TSPT
• Dans une étude conçue pour modéliser le SSPT (via un stress traumatique à l'adolescence), l'inhibiteur de la méthyltransférase Unc0642 (dissous dans du DMSO) a atténué l'anxiété (autrement permanente), la dépression, le dysfonctionnement social et cognitif et a normalisé le développement cérébral altéré par le SSPT.
Dans un modèle modifié de stress post-traumatique induit par un stress unique et prolongé (SPS), une dose modérée d'extrait de feuilles de Cannabis sativa ( dissous dans du DMSO) a significativement amélioré l'efficacité de la thérapie d'exposition pour l'extinction du souvenir de peur conditionnée. Ce bénéfice était dépendant des récepteurs CB1 et persistait lors d'un test sans médicament 14 jours plus tard.
Stresser
Outre le stress à l'origine du syndrome de stress post-traumatique (SSPT), de nombreuses études sur les rongeurs ont modélisé diverses autres situations stressantes (provoquant fréquemment anxiété ou dépression). Ces études constituent la majorité des recherches psychiatriques sur le DMSO et, collectivement, leurs résultats contribuent à étayer la théorie de la maladie psychiatrique proposée par les chercheurs russes mentionnés précédemment.
Dans le cadre d'un stress chronique de « défaite sociale » induit par une exposition répétée à un mâle agressif qui soumet un autre rongeur par l'attaque, le DMSO combiné à la dihydromyricétine a significativement amélioré l'apprentissage et la mémoire, diminué le temps d'immobilité et réduit l'anxiété. Dans une autre étude , l'épothilone D, dissoute dans du DMSO, a prévenu les modifications cérébrales du cortex préfrontal et de l'hippocampe causées par ce type de stress. La naringénine a atténué les déficits neurocomportementaux induits par la défaite sociale, réduit le stress oxydatif (MDA cérébrale), restauré le glutathion et diminué les taux de TNF-α et d'IL-1β.
De nombreuses études ont montré des résultats prometteurs quant à l'atténuation des effets du stress émotionnel et douloureux chronique (généralement trois semaines de symptômes extrapyramidaux).
• Dans une étude, l' administration de
DMSO avant le stress a augmenté l'activité de la superoxyde dismutase
(SOD) dans les homogénats de cerveau et le sérum. Dans une autre, le
DMSO a également augmenté l'activité de la SOD et diminué l'activité de
la céruloplasmine-transferrine, suggérant que la capacité du DMSO à neutraliser le stress chronique est liée à sa capacité à réduire le stress oxydatif.
• Dans une autre étude encore ,
l'administration de DMSO avant un syndrome extrapyramidal chronique a
complètement prévenu le développement d'ulcères gastriques, bloqué les
modifications comportementales induites par le stress lors du test en
champ ouvert (hyperactivité, redressements et exploration réduite du
centre, signes d'anxiété) et normalisé les réponses cardiovasculaires et
autonomes, notamment l'hypertension et les modifications des fréquences
cardiaque et respiratoire observées pendant le stress et lors de
l'immobilisation subséquente. De plus, comme dans les études
précédentes, il a augmenté de façon marquée l'activité de la SOD dans le
cerveau. Remarque : le
DMSO ayant interféré avec la formation de malondialdéhyde (un marqueur
de la peroxydation lipidique), les chercheurs n'ont pas pu mesurer s'il
réduisait sa formation dans le cerveau.
Le test de nage forcée (FST), controversé, évalue la dépression à travers le passage de comportements d'adaptation actifs à une immobilité passive chez des souris confrontées à un facteur de stress inévitable. Seul ou en association avec le test de suspension par la queue, des études ont montré que le DMSO , combiné aux substances suivantes, induisait une activité antidépressive : flavonoïdes d’ Alpinia oxyphylla , extrait de cannelle , acide asiatique ( comparable au midazolam), trans -resvératrol , chrysine ( dont l’ effet était potentialisé par le Prozac et similaire à celui du diazépam), extrait éthanolique de Ptychopetalum olacoides , huile essentielle de Nepeta rtanjensis ( un inhibiteur de la monoamine oxydase), riparine III (issue d’une plante amazonienne), extraits méthanoliques de Cuminum nigrum (L.) et de Centratherum anthelminticum ( qui réduisaient également l’anxiété ) , acide ganodérique A et extrait méthanolique de Withania. qaraitica ⬖ (d'efficacité similaire au citalopram ou à la désipramine), l'oridonine , ⬖ l'alarine , l'ODQ et le 7-NI , le Prozac et un agoniste des récepteurs cannabinoïdes CB1.
Le stress chronique par contention est un test couramment utilisé chez les rongeurs pour modéliser la dépression et l'anxiété chez l'humain. Chez les rats soumis à ce stress, en association avec du DMSO :
• Un inhibiteur de la caspase-1 a réduit l'immobilité, l'évitement social et l'anhédonie qui faisaient suite au stress chronique et au stress de défaite sociale.
•Xiao Yao San ⬖ et un inhibiteur de c-Jun (JNK) ont amélioré de façon répétée les comportements de type anxieux. De plus, la formule de phytothérapie chinoise a réduit l'expression des protéines et des ARNm de JNK phosphorylée, JNK et Pc-Jun dans l'hippocampe, de façon comparable à l'inhibiteur de JNK, chez des rats atteints de CRS présentant une dépression hépatique et un syndrome de déficience splénique. 1 , 2
• La quercétine intrapéritonéale ⬖ a significativement atténué les comportements de type anxiété et dépression chez les rats CRS qui présentaient également un débit sanguin cérébral restreint (via une sténose bilatérale de l'artère carotide), tout en atténuant la démyélinisation de l'hippocampe, en restaurant l'épaisseur de la gaine de myéline, en réduisant l'inflammation cérébrale (via une réduction de l'IL-1β/TNF-α, une augmentation de l'IL-10/IL-4, une polarisation M2 microgliale favorisée) et en améliorant la phagocytose (élimination) microgliale des fragments de myéline nocifs.
• Un antagoniste du récepteur de type 1 de l'hormone de libération de la corticotropine a empêché les diminutions induites par le stress du poids corporel, de la préférence pour le saccharose et de la locomotion, ainsi que la régulation positive du BDNF et du GAP-43 dans l'hypothalamus (contrairement à l'hippocampe, les augmentations hypothalamiques sont inadaptées).
• Le safranal ⬖ a protégé contre les dommages cérébraux oxydatifs induits par le stress de contention et a atténué les changements comportementaux induits par le stress.
• La saikosaponine A ⬖ et la paeoniflorine ⬖ ont soulagé l'inhibition du flux autophagique induite par la corticostérone dans les cellules PC12 en réduisant l'expression de LC3II/I, P62 et mTOR, suggérant un rôle dans le stress chronique.
Dépression
Le test de stress chronique imprévisible et léger (CUS), qui reproduit l'évolution de la dépression chez l'humain, est l'un des tests les plus utilisés pour l'évaluer chez les rongeurs. Des composés naturels, des inhibiteurs de voies de signalisation ciblées et des médicaments pharmaceutiques utilisés en clinique (administrés en association avec du DMSO) ont montré les effets bénéfiques suivants chez les rats exposés au CUS :
• Un extrait de ptychopetalum olacoides ⬖ a prévenu l'anxiété et l'hyperglycémie.
L’ administration intrapéritonéale de curcumine a amélioré les comportements de type dépressif et augmenté l’expression (neurotrophe) du BDNF, du PSD-95, de la synaptophysine, de la p-Limk1 et de la p-cofiline dans le cortex préfrontal. Dans une autre étude , elle a également inversé les comportements induits par le stress chronique imprévisible et augmenté l’expression de ces trois protéines neurotrophiques dans l’amygdale latérale.
• L'oridonine ⬖ (issue de Rabdosia rubescens ) a réduit l'anxiété sociale et la dépression, amélioré la préférence pour le saccharose, l'activité en champ ouvert, la morphologie neuronale et le nombre de cellules dans le cortex préfrontal et l'hippocampe et a supprimé la voie inflammatoire p38 MAPK/NF-κB/NLRP3.
Le bloqueur de JNK, SP600125, a partiellement modulé l'axe HPA hyperactif en diminuant significativement les taux d'ACTH hypophysaire et en augmentant l'expression du récepteur des glucocorticoïdes (GR) dans la région CA3 de l'hippocampe, comparativement au groupe témoin (solvant). Il a également réduit l'augmentation de la caspase-12 induite par le stress (inhibant ainsi l'apoptose neuronale hippocampique), diminué l'expression de C-Jun (une voie souvent hyperactivée en cas de stress chronique) et potentialisé l'effet dépresseur de l' électroacupuncture . <sup> 1,2,3,4 </sup>
• La nécrostatine-1 (qui bloque la mort des cellules inflammatoires) a également amélioré les comportements de type dépressif.
• L'administration intracérébroventriculaire d'a larin a réduit la dépression, diminué le temps d'alimentation et restauré l'activité p-ERK/ERK et p-AKT/AKT (neurotrophique/neuroplasticité) dans le cortex préfrontal.
• L’agomélatine a réduit l’afflux de calcium médié par TRPV1, le stress oxydatif et l’apoptose dans les neurones de l’hippocampe de rats soumis à un stress chronique, améliorant ainsi les comportements liés à la dépression.
• La pioglitazone a amélioré les comportements de type dépressif, supprimé l'augmentation des cytokines pro-inflammatoires (TNF-α, IL-1β, IL-6), réduit le rapport microglial M1/M2, diminué l'expression de NF-κB et amélioré la perte d'expression du récepteur gamma activé par les proliférateurs de peroxysomes (PPARγ) dans le cortex préfrontal et l'hippocampe.
• La quétiapine a amélioré le comportement de type dépressif chez les rats soumis à un stress chronique imprévisible, a augmenté l'expression du BDNF et du phospho-ERK1/2 dans l'hippocampe et a favorisé la neurogenèse (et a été renforcée de manière synergique par la combinaison avec la stimulation magnétique transcrânienne).
Remarque : le DMSO seul a diminué l'expression élevée de la protéine caspase-12 dans l'hippocampe (qui peut entraîner la mort neuronale).
La séparation des rats nouveau-nés de leur mère induit des comportements dépressifs à long terme (anhédonie, dérèglement de l'axe hypothalamo-hypophyso-surrénalien et réduction de la neurogenèse hippocampique) similaires à ceux observés chez les adultes humains souffrant de dépression et de stress chronique. Chez ces rats séparés , la mélatonine dissoute dans du DMSO a augmenté significativement le nombre de cellules BrdU-positives et diminué l'expression du récepteur des glucocorticoïdes dans le gyrus denté, contrant ainsi directement le processus dépressif.
Remarque : Le terme « dépression » désigne à la fois un état psychiatrique (psychologique/de l’humeur) et une réduction de l’activité et de la vigilance induite par le SNC (dépression neurologique ou altération de l’état mental). Ces deux états sont liés, car les maladies inflammatoires ou infectieuses peuvent affecter le système nerveux et entraîner son dysfonctionnement partiel, déclenchant des symptômes communs aux deux, tels qu’une baisse de la vigilance/des facultés mentales et des changements d’humeur (souvent qualifiés de « comportements de maladie »). Dans certains cas, comme celui d’un poulain ayant subi des lésions cérébrales suite à une interruption de l’irrigation sanguine à la naissance , l’action thérapeutique du DMSO sur le système nerveux a également permis d’atténuer la dépression neurologique (amélioration de la vigilance et des facultés mentales). Dans d’autres cas, le DMSO a contribué à la résolution de la dépression psychiatrique consécutive à une maladie, probablement grâce à ses effets anti-inflammatoires et neuroprotecteurs sur les voies nerveuses communes.
Anxiété
Chez le poisson-zèbre, la volonté de quitter les zones sombres pour entrer dans les zones claires est utilisée pour évaluer l'anxiété, et dans ce modèle, le DMSO seul a réduit l'anxiété (de même que le DMSO en combinaison avec la chalcone C2OHPDA ).
Chez les souris et les rats, leur comportement dans des labyrinthes spécifiques (par exemple, le test du labyrinthe en croix surélevé) ou lors de déplacements en champ libre est utilisé pour évaluer l'anxiété. Dans une étude, la microinjection de DMSO seul (10 %, 0,5 µL) dans la DPAG (une structure du mésencéphale) a considérablement réduit l'anxiété et augmenté le comportement exploratoire. <sup> 1,2 </sup> En association avec le DMSO, les agents suivants ont permis de réduire l'anxiété : l' eucalyptol (principal composant de l'huile d'eucalyptus), le cinnamomum (extrait hydroalcoolique), la marjolaine (extraite au DMSO), la lutéoline (après une colite expérimentale aiguë), l'acide asiatique , la caséarine X , les valépotriates , le 5-MeO-DMT , le CCK-8 , les agonistes du CCK₂ et les agonistes des récepteurs cannabinoïdes et vanilloïdes (TRPV1).
• Un agoniste mGluR2/3 dissous dans du DMSO a réduit l'anxiété chez les poussins stressés par une brève séparation sociale.
Note : l'extrait de feuille de Withania somnifera ⬖ (dans du DMSO) a protégé contre la neurotoxicité induite par le benzo[a]pyrène chez le poisson-zèbre en restaurant l'anxiété normale , en améliorant le statut antioxydant du cerveau et en réduisant les dommages neuronaux dans le tectum optique.
Facteurs de stress biologiques
En plus de placer les animaux dans des situations psychologiquement stressantes, on a également observé que divers facteurs de stress qui endommagent directement le corps déclenchent de l'anxiété et de la dépression et répondent à des combinaisons thérapeutiques contenant du DMSO.
Deux potentialisateurs des récepteurs du glutamate de type AMPA ont réduit l'hypersensibilité à la douleur et les comportements de type dépressif chez les rats souffrant de douleurs neuropathiques et inflammatoires.
Dans les douleurs neuropathiques consécutives à une lésion nerveuse épargnée (LNE), un inhibiteur de la méthyltransférase de l'ADN (dans du DMSO) a significativement amélioré les symptômes dépressifs et augmenté les taux de BDNF, facteur neurotrophique cérébral. Dans une autre étude sur les LNE , un inhibiteur chémogénétique de DREADD (dans du DMSO) a soulagé à la fois la douleur et les symptômes dépressifs, et dans une troisième , la rapamycine a atténué l'anxiété, la dépression et la douleur liées à une LNE L5.
Chez les rats atteints d'épilepsie déclenchée par le pentylènetétrazol (qui produit systématiquement de l'anxiété et de la dépression), la rapamycine et le pitolisant (dissous dans du DMSO) ont nettement amélioré l'anxiété (amélioration de 2,7 fois sur un test de labyrinthe) et la dépression (amélioration de 37,5 % au test de nage).
Chez les souris dont la dépression a été induite par le LPS, le resvératrol ⬖ dans le DMSO a inversé leur dépression, ainsi que l'inflammation neuronale et le déclenchement de la neurogenèse (en particulier dans l'hippocampe).
Chez les souris atteintes de toxoplasmose déclenchant une dépression, l'arctigénine ⬖ dans le DMSO a réduit de manière significative les comportements dépressifs et l'inflammation cérébrale en inhibant les principales voies pro-inflammatoires (TLR4/NF-κB et TNFR1/NF-κB).
Chez des souris ovariectomisées (OVX) modélisant la ménopause, le resvératrol ⬖ dans le DMSO a réduit de manière significative l'anxiété et la dépression induites par l'ovariectomie (ablation des ovaires) ainsi que l'inflammation neuronale (en particulier dans l'hippocampe).
Chez des souris souffrant d'anxiété induite par un régime riche en graisses, le ginseng japonais ⬖ dans du DMSO a réduit de manière significative les comportements de type anxieux, augmenté les niveaux de BDNF et de synaptophysine dans le cerveau et inversé la résistance du cerveau au FGF21 (un facteur clé de l'anxiété).
Chez les souris, la naringénine a amélioré la dépression et l'anxiété déclenchées par l'hypoxie, tout en réduisant le stress oxydatif et l'inflammation cérébrale, en augmentant l'expression du BDNF et en protégeant les neurones de l'amygdale.
Chez des souris exposées aux rayons X après avoir consommé de la saccharine (ce qui les conditionne à éviter cet édulcorant), l'application topique de DMSO avant l'exposition aux rayons X a largement empêché cette aversion (la consommation de saccharine a diminué de 8 % au lieu de 66 %). Une étude ultérieure a abouti à des résultats similaires, suggérant que le DMSO contrecarre le stress qui, autrement, induirait cette aversion. <sup> 1,2 </sup>
Remarque : enfin, certaines des combinaisons de DMSO décrites dans les sections précédentes ont été utilisées pour traiter des affections directement déclenchées par un médicament (par exemple, la dépression due à la corticostérone ou l'anxiété due aux salicylates ).
Psychose
• Il a été proposé que le DMSO exerce des effets antipsychotiques en modulant l'activation chronique des macrophages et la dérégulation des cytokines en aval, en particulier la signalisation de l'interleukine-2, réduisant ainsi les symptômes de la schizophrénie à travers les phases de la maladie par la régulation immunitaire.
Le MK-801, une substance dont le mécanisme d'action est similaire à celui de la phencyclidine (PCP) et de la kétamine, induisant des psychoses, est utilisé pour provoquer la schizophrénie chez les rongeurs. Une étude a montré que les antipsychotiques atypiques et l'inhibiteur de la kinase Src, le PP1, dissous dans du DMSO, atténuaient significativement les lésions corticales (cérébrales) induites par le MK-801 chez le rat. L'efficacité protectrice des antipsychotiques était corrélée à leur efficacité clinique dans le traitement des psychoses.
• Dans une étude sur des rats MK-801 , trois médicaments différents qui activaient le récepteur α7nAChR (lorsqu'ils étaient combinés avec du DMSO) ont amélioré de manière significative les comportements schizophréniques en augmentant le comportement de suivi et le temps d'interaction total, en diminuant le temps de comportement d'évitement et en créant des changements thérapeutiques au sein du cortex préfrontal et de l'hippocampe (augmentation de l'expression de la protéine α7 nAChR, augmentation des niveaux d'AMPc, diminution de l'expression des protéines PDE4A et PDE4D).
• Diosmine ⬖ a atténué l'hyperactivité , les déficits comportementaux, le stress oxydatif et la neuroinflammation dans un modèle murin de symptômes de type schizophrénie induits par le LPS et la kétamine.
• Dans une autre étude sur la schizophrénie MK-801 , le flavonoïde Fisetin ⬖ (administré par voie intrapéritonéale dans du DMSO) a diminué de manière significative la latence d'échappement du rat, augmenté le temps d'exploration spatiale et les traversées de la plateforme et (bénéfiquement) phosphorylé CaMKII, ERK1/2 et CREB.
En plus de ces combinaisons traitant la schizophrénie, le tinospora cordifolia ⬖ (une herbe ayurvédique) dissous dans du DMSO a démontré une activité antipsychotique chez des souris ayant reçu des amphétamines (induisant la psychose) (ainsi que la curcumine ⬖ dans du DMSO contrecarrant la neurotoxicité induite par la méthamphétamine et les troubles de la mémoire spatiale chez les rats).
Note : une étude (qui a révélé que les rates étaient plus susceptibles de développer une dépendance à la méthamphétamine que les rats mâles) a montré que le modafinil dissous dans du DMSO atténuait le comportement de recherche de méthamphétamine chez les deux sexes. Une autre étude a montré que le parthénolide (dissous dans 1 % de DMSO) bloquait partiellement les effets de la cocaïne sur le cerveau (mais il est peu probable que cela puisse être transposé à un traitement de la dépendance à la cocaïne).
La sédation et la relaxation sont parfois rapportées suite à l'utilisation de DMSO (par exemple, une sédation a été observée à plusieurs reprises chez l'homme et l'animal à fortes doses ; l'administration intrapéritonéale de DMSO a entraîné une diminution de l'activité motrice spontanée et, dans un essai clinique de grande envergure ,
3 % des utilisateurs de DMSO ont rapporté une fatigue accrue). Ceci est
probablement dû à l'augmentation du tonus parasympathique induite par
le DMSO ( en raison de son inhibition de l'acétylcholinestérase )
et pourrait expliquer en partie ses propriétés psychiatriques,
l'hyperactivité sympathique jouant un rôle clé dans l'anxiété, la manie
et la psychose.
Remarque :
je constate qu'une part importante des troubles psychiatriques résulte
d'une hyperactivité sympathique ou d'une hypoactivité parasympathique
(par exemple, l'« excitation » que cet état provoque engendre
fréquemment de l'anxiété), et de même, nombreux sont ceux (moi y
compris) qui pensent qu'un nombre important de problèmes de santé sont
dus à un dysfonctionnement vagal (parasympathique). Étant donné que le
DMSO peut à la fois augmenter directement la fonction parasympathique et
guérir ou restaurer la fonction des nerfs (tout en relâchant
potentiellement les muscles tendus qui les compriment), il est possible
que certains des bienfaits du DMSO dans les affections psychiatriques
proviennent de son effet sur la fonction vagale.
Enfin, comme de nombreux autres agents thérapeutiques, le DMSO a également été associé à des antipsychotiques. Par exemple, avec l'halopéridol administré par voie intrapéritonéale , il a favorisé une augmentation de 1,8 fois de l'ARNm de la préproenképhaline striatale et de 1,6 fois des peptides opioïdes endogènes totaux induits par l'halopéridol (sans effet sur d'autres régions cérébrales), augmentant ainsi l'efficacité de l'antipsychotique et pouvant potentiellement réduire la douleur ou les effets secondaires extrapyramidaux des antipsychotiques.
Remarque : divers antipsychotiques ont utilisé le DMSO comme véhicule (par exemple, cette étude l'a fait avec l'olanzapine intrapéritonéale, l'amisulpride, la quétiapine et l'aripiprazole, tandis que celle-ci l'a fait avec l'halopéridol, la clozapine, le RMI-81582 et la rispéridone).
Dormir
Le sommeil est l'un des aspects les plus importants, et pourtant les moins appréciés, de notre existence. En effet, la guérison du corps et l'harmonisation de l'esprit par le sommeil constituent un processus extrêmement complexe qui peut facilement être perturbé (par exemple, un mauvais sommeil entraîne une neurodégénérescence, et la neurodégénérescence aggrave les troubles du sommeil). Malheureusement, au lieu de le soutenir, notre système médical a tendance à traiter l'insomnie par des sédatifs (comme les somnifères) qui, certes, « endorment », mais qui inhibent également le processus réparateur du sommeil. C'est tragique, car le rétablissement d'un sommeil sain figure souvent parmi les trois actions prioritaires pour soigner les maladies chroniques.
Étant donné que le DMSO soigne le système nerveux et rétablit la circulation des fluides altérée (ce qui, je crois, est à l'origine de nombreux cas d'insomnie), j'espérais donc que le DMSO puisse être une aide remarquable au sommeil pour faciliter un sommeil réparateur.
Pourtant, parmi les 6 000 signalements que j’ai reçus de lecteurs, seuls quelques-uns indiquent que cela s’est produit. 1 , 2 , 3 , 4 , 5 , 6 , 7 , 8 , 9 , 10 , 11
Ce que j'ai surtout remarqué récemment, c'est une diminution de la fatigue. Avant, je faisais une sieste tous les jours, puis je dormais 8 à 9 heures de plus la nuit. Maintenant, si j'essaie de faire une sieste, je n'en ai tout simplement pas envie. Je dors normalement la nuit et je me réveille reposé.
Note : un autre lecteur a vécu une expérience presque identique, tandis qu'un autre a indiqué que le DMSO avait résolu le problème de sommeil excessif dont il avait longtemps besoin suite à un AVC.
Prendre quelques millilitres avant de me coucher améliore considérablement mon sommeil.
Je me sens merveilleusement bien . Mon sommeil est généralement remarquable.
J'adore le sommeil profond qu'il me procure . Après des mois de travail intense et prolongé, j'étais épuisée. Un matin, j'en ai pris une petite dose, comme ça, sans raison particulière. Une heure plus tard, impossible de résister à l'envie de dormir. Je me suis réveillée des heures plus tard, complètement reposée. C'est vraiment génial.
J'ai commencé à l'utiliser à la place de l'hydroxyzine , que je prends occasionnellement. Aucun effet secondaire !
Remarque : quelques lecteurs ont également signalé un effet énergisant du DMSO, leur permettant de se réveiller après des périodes beaucoup plus courtes et de se sentir rafraîchis (ce qui peut être positif ou négatif).
Cependant, dans les rapports que j'ai reçus, deux tendances constantes se dégagent.
Premièrement , bien que le DMSO n'agisse pas intrinsèquement comme un somnifère, de nombreuses personnes ont rapporté qu'il avait guéri un trouble provoquant de l'insomnie. J'ai moi-même reçu des dizaines de témoignages de personnes affirmant que le DMSO, en leur permettant de mieux dormir, avait profondément amélioré leur vie (y compris des cas où elles avaient eu des pensées suicidaires). Ceci met en lumière les failles de l'approche symptomatique de la médecine, car de nombreux cas d'insomnie dont les causes sont clairement identifiables (mais jamais traitées) sont simplement « traités » par des somnifères.
Le plus souvent, cela était dû au DMSO utilisé pour traiter des douleurs musculo-squelettiques qui les empêchaient de s'endormir (ou les réveillaient régulièrement la nuit). Les douleurs à l' épaule ( par exemple , bursite, conflit sous - acromial ou rupture de la coiffe des rotateurs ) <sup> 1,2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17 </sup> étaient les plus fréquentes , suivies des lombalgies ( par exemple , radiculopathie , hernies ou déchirures discales , échec de chirurgie rachidienne , métastases vertébrales ) <sup> 1,2,3,4,5,6,7,8,9,10,11,12,13,14 </sup> , de l' arthrite ( par exemple , polyarthrite rhumatoïde et douleurs aux mains ou aux orteils ) <sup> 1,2,3,4,5,6,7,8,9 </sup> et des douleurs au genou . (par exemple, arthrite, lésion du ménisque ou entorse chez un enfant de 2 ans), 1 , 2 , 3 , 4 , 5 , 6 , 7 douleur à la hanche ( par exemple , bursite ) , 1 , 2 , 3 , 4 douleur au coude (par exemple, tennis elbow), 1 , 2 , 3 douleur au cou (coup du lapin ou discopathie dégénérative) 1 , 2 douleur à la main, 1 , 2 douleur à la mâchoire 1 , 2 tendinopathie des membres inférieurs (par exemple, fessier) 1 , 2 plus des cas individuels d'amélioration importante du sommeil après la résolution d'une sciatique , d' une douleur au pied , d'un pouce lancinant , de muscles tendus et d' un traumatisme maxillo-facial contondant (par exemple, projeté sur le trottoir par une voiture).
Le DMSO a également permis de résoudre d'autres types de douleurs qui empêchent le sommeil, comme la neuropathie périphérique (par exemple, dans les pieds), 1 , 2 , 3 , 4 , 5 , 6 , 7 les maux de tête (par exemple, les migraines, les commotions cérébrales), 1 , 2 , 3 les douleurs cancéreuses 1 , 2 des cas individuels de douleurs oculaires , le syndrome douloureux régional complexe (SDRC), et que syndrome douloureux ( et névralgie du trijumeau . De plus , de nombreuses douleurs non spécifiées, sources de troubles du sommeil , ont été résolues <sup> 1,2,3,4,5,6,7,8 .
Le DMSO a également amélioré d'autres affections neurologiques complexes, au point d'améliorer considérablement le sommeil, comme le syndrome des jambes sans repos ( 1 , 2 , 3 , 4 , 5 , 6 ), la maladie de Lyme ( 1 , 2 ), les effets indésirables des vaccins (Moderna ou le vaccin contre le zona) ( 1 , 2) , ainsi que des cas individuels de syndrome de Down , de polyneuropathie démyélinisante , de syndrome de fasciculations spasmodiques (semblable à la SLA et ayant provoqué chez le lecteur des pensées suicidaires sous l'effet du DMSO), de tics chez un chien âgé et de troubles neurologiques chroniques non spécifiés qui l'empêchaient de bien dormir depuis des années. Par exemple, pour citer un patient atteint de la maladie de Lyme :
Puis je me suis réveillé un matin et j'ai été stupéfait de constater que j'avais dormi toute la nuit, alors qu'avant le DMSO, je me réveillais 3 ou 4 fois par nuit à cause de la douleur.
Enfin, outre son action sur la douleur et les neuropathies qui perturbaient le sommeil, le DMSO agissait également sur d'autres problèmes affectant le sommeil. Le plus souvent, cela se traduisait par une amélioration de la respiration, notamment en traitant la sinusite (par exemple : « J'ai très bien dormi la nuit dernière, je n'avais pas envie de me lever ce matin. ») <sup> 1,2,3 </sup> ou les problèmes pulmonaires ( par exemple, l'asthme, la BPCO ou les lésions pulmonaires dues aux fosses d'incinération en Afghanistan). <sup> 1,2 </sup> Un lecteur a envoyé un témoignage particulièrement intéressant, suggérant que le DMSO peut parfois améliorer la saturation en oxygène nocturne :
J'ai essayé une petite quantité de solution à 70 % sur un coton-tige dans chaque narine avant de me coucher pour voir si cela soulagerait ma congestion nocturne. Étonnamment, je ne ressens aucune démangeaison ni picotement à l'intérieur des narines… peut-être grâce au mucus ? Quoi qu'il en soit, je porte une bague de suivi du sommeil et mon taux d'oxygène ainsi que les baisses d'oxygène se sont considérablement améliorés. Je dors plus longtemps et je me réveille moins souvent ! Je suis stupéfait et j'ai cherché des études qui pourraient expliquer ces améliorations. J'ai trouvé des recherches sur les cycles de sommeil chez les rongeurs, mais elles sont difficiles à interpréter. Je voulais simplement vous en informer et vous remercier de partager vos connaissances. Je vais poursuivre mon expérience et, jusqu'à présent, mes données de sommeil se sont améliorées chaque nuit.
Remarque : d'autres problèmes pour lesquels les lecteurs ont signalé une amélioration du sommeil grâce au DMSO incluent l'œsophage de Barrett , l'eczéma sévère , l'hypertrophie de la prostate , l'hypothyroïdie ou un rhume aigu .
En bref, étant donné l'importance d'un sommeil sain pour le système nerveux (détaillé ici ), on peut donc affirmer que l'un des principaux mécanismes par lesquels le DMSO « guérit le système nerveux » résulte du traitement des affections qui empêchaient un sommeil sain.
Deuxièmement , j'ai constaté que de nombreux lecteurs ont indiqué, indépendamment les uns des autres, que leurs rêves étaient devenus plus vifs ou plus lucides après la prise de DMSO. 1 , 2 , 3 , 4 , 5 , 6 , 7 , 8 , 9 , 10 , 11 , 12 , 13 , 14 , 15 , 16
Par ailleurs, après plusieurs semaines de prise de DMSO par voie orale, j'ai effectivement constaté une augmentation de mes rêves. Pendant la majeure partie de ma vie, je n'ai pas rêvé du tout ou du moins je n'en ai aucun souvenir. En revanche, j'ai toujours dormi profondément et réparateur. Je m'endormais généralement en quelques secondes après m'être allongé et je n'avais aucun souvenir de mes rêves jusqu'au lendemain matin. Lorsque j'ai pris des compléments de 5-HTP pendant un certain temps, il y a quelques années, j'ai commencé à rêver beaucoup pour la première fois de ma vie.
Deux facteurs pourraient potentiellement expliquer cela. Premièrement, en soignant le système nerveux et en restaurant la circulation, le DMSO favorise probablement le fonctionnement de l'appareil neurologique impliqué dans les rêves. Deuxièmement, deux composés sont couramment utilisés pour faciliter les rêves lucides : le 5-HTP (utilisé par le lecteur mentionné plus haut) et la galantamine (l'une des rares substances que j'ai testées, principalement pour ses effets remarquables sur les rêves lucides, à condition de ne pas en abuser ). La galantamine est un inhibiteur de l'acétylcholinestérase, et comme le DMSO est également reconnu pour cette propriété, cela explique probablement l'augmentation de la vivacité des rêves. Cependant, les effets que j'ai observés avec les deux sont très différents (à tel point que je n'aurais jamais imaginé qu'un mécanisme similaire soit en jeu). Si cette théorie est valide, il me semble donc que le DMSO devrait être considéré comme un inhibiteur de l'acétylcholinestérase beaucoup plus faible, n'affectant les rêves que d'une partie de la population.
Les réactions face à ces rêves semblaient très diverses (les adorer, apprécier de pouvoir enfin s'en souvenir, être neutre ou les trouver difficiles), la majorité étant positive. Ces réponses illustrent bien cette diversité :
J'ai commencé à utiliser ces produits après avoir lu vos publications, et ça m'a donné des rêves incroyablement vivants, certains même complètement lucides, haha ! Je n'ai rien remarqué d'autre pour l'instant, mais rien que les rêves valent le coup. Je recommande à 100 % !
Quand j'en bois... après quelques jours... je dors très profondément et je fais des rêves incroyablement émouvants... ce qui peut être difficile, mais je me réveille reposée (mais triste ou contemplative).
C'est drôle que tu parles de rêves et de DMSO, car depuis que j'en prends par voie orale, mes rêves sont extrêmement vifs et parfois très désagréables ! Des gens auxquels je n'avais pas pensé depuis des décennies apparaissent dans mes rêves… La mélatonine provoquait aussi des rêves vifs, mais rien de comparable à ce que le DMSO me fait faire !
Globalement, mon histoire de rêve préférée était probablement celle-ci :
Je dois vous raconter une chose … Le premier soir où j'ai appliqué du DMSO sur ma nuque, je suis allée me coucher et, pendant la nuit, j'ai entendu une voix dire : « LES ARBRES TE GUÉRIRONT ». Dans mon état de somnolence, j'ai pensé : « Oh, c'est merveilleux, j'aime tellement nos arbres ; je vis dans une forêt. » Mais à mon réveil, j'ai réalisé que le DMSO provient des arbres et que ce message concernait justement le DMSO !
Dernièrement, un lecteur a indiqué que le DMSO lui permettait de réduire considérablement la dose de Xanax nécessaire pour s'endormir, tandis qu'un autre a déclaré qu'il le rendait beaucoup plus sensible aux perturbations de son sommeil causées par le café ou la bière. Ceci concorde avec la capacité connue du DMSO à potentialiser les effets des benzodiazépines et de l'alcool et suggère qu'il convient d'être prudent lors de l'utilisation conjointe de ces substances. Cependant, étant donné que seuls deux lecteurs ont constaté cet effet, contrairement à l'interaction DMSO-alcool , son impact reste incertain. Par ailleurs, deux lecteurs ont rapporté que les effets soporifiques du DMSO étaient renforcés par son association avec du magnésium ( ce qui est plausible). <sup> 1,2 </sup>
Recherche sur le sommeil
Les rares publications scientifiques sur le DMSO et le sommeil montrent ce qui suit :
1. Le DMSO seul a généralement un impact minime sur le cycle du sommeil. Par exemple, une étude menée en 2005 sur des rats a
montré que l'administration intrapéritonéale de DMSO à 5 % et 10 %
n'avait aucun effet sur l'architecture du sommeil, tandis que des
concentrations de 15 % et 20 % induisaient un passage du sommeil profond
au sommeil léger. Cela indique que les doses ingérées par les individus
sont peu susceptibles d'affecter le sommeil, sauf chez les personnes
appartenant à une minorité sensible. De même, dans une étude où l'administration intrapéritonéale de
facteur de libération de la corticotropine a transformé le sommeil
paradoxal en sommeil lent chez les rats, le DMSO seul (à une dose non
précisée) n'a eu aucun effet sur l'architecture du sommeil.
Remarque : une revue de la littérature cite
un rapport russe faisant état de troubles du sommeil parmi les effets
secondaires du DMSO, mais je n'ai trouvé aucune autre mention de ce
phénomène.
2. Quelques références corroborent que les propriétés curatives du DMSO améliorent le sommeil en soignant un autre facteur à l'origine de l'insomnie :
Dans une étude menée auprès de 35 hommes souffrant d'arthrose du genou exacerbée (et d'hémorragie digestive haute), l'application topique de DMSO à 50 % (associé à de l'hydrocortisone, de la lidocaïne et de l'iodure de potassium) a non seulement réduit leurs douleurs au genou, mais a également amélioré leur sommeil (et leur capacité de travail). Plus précisément, sur une échelle de -3 (très mauvais) à 3 (meilleur), leur score de sommeil initial (0,4 ± 0,2) est passé à 1,1 ± 0,4 avec l'association DMSO, et à 2,8 ± 0,5 lorsque cette association était combinée à de la kinésithérapie.
• Chez 40 patients ( âgés en moyenne de 53,7 ans) atteints d'ostéochondrose cervicale compliquée par un syndrome de douleur myofasciale de l'épaule, le DMSO topique (en association avec d'autres analgésiques) et la physiothérapie et l'acupuncture ont complètement résolu la douleur chez 34 (85 %), l'ont partiellement améliorée chez 6 (15 %) et chez tous les patients, il y a eu une amélioration significative du sommeil.
Dans un guide clinique ouzbek sur les infections chirurgicales de la main et des doigts, le DMSO était recommandé comme traitement conservateur (en association avec de la novocaïne et un antibiotique) pour les abcès de la pulpe digitale, afin de prévenir l'aggravation de la douleur et l'insomnie qui pourraient nécessiter une intervention chirurgicale. Dans un manuel dentaire ukrainien , le DMSO était recommandé pour la guérison (et la prévention des infections) des alvéolites sèches, car il permettait de traiter ces affections et d'améliorer de nombreux symptômes associés, notamment les troubles du sommeil.
• Dans une étude menée auprès de patients atteints de sclérodermie localisée, l'application topique quotidienne de DMSO (et de quelques autres thérapies) a significativement amélioré les lésions cutanées, prévenu les rechutes et amélioré la santé émotionnelle, l'appétit et le sommeil.
3 : La plupart des recherches existantes sur le DMSO et son utilisation pour le sommeil l’ont décrit comme un vecteur associé à un autre agent favorisant le sommeil, soit pour faciliter son action, soit pour en accroître l’efficacité. Ces recherches se répartissent en quatre catégories, dont deux corroborent les observations des lecteurs.
Potentialisation des somnifères :
• L’administration préalable de DMSO a augmenté de 78 % la durée du sommeil induit par le pentobarbital sodique. À l’inverse, une autre étude a montré que la durée du sommeil induit par l’hexobarbital n’était pas modifiée lorsque 2,5 g/kg de DMSO à 25 % étaient administrés par voie sous-cutanée à des souris au préalable.
• Une fraction dissoute dans du DMSO d'un extrait de Coriandrum sativum ⬖ a accéléré et prolongé le sommeil induit par le pentobarbital plus que tout autre agent testé (y compris le diazépam).
•Un extrait de Marjolaine DMSO ⬖ et séparément un extrait de rhizome de Nardostachys jatamansi ⬖ ont augmenté de manière significative la durée du sommeil induit par la kétamine. 1 , 2
Modulation des rythmes circadiens de sommeil (avec une utilité potentielle pour le décalage horaire) :
La mélatonine , qui a
accéléré la resynchronisation du rythme circadien de la souris après un
décalage de phase de 6 heures et a également rendu les souris plus
sensibles aux décalages circadiens induits par la lumière. <sup> 1,2 </sup>
Dans deux autres études, le triazolam (un somnifère dissous dans du
DMSO) a décalé et allongé le rythme circadien des hamsters, tandis que
le DMSO seul n'a induit qu'un léger décalage non significatif. <sup> 1,2 </sup> Enfin, le métabolite du DMSO, le MSM, a également été étudié. ( présent
dans le DMSO), a atténué les troubles neurocomportementaux, le stress
oxydatif et les perturbations de l'expression des gènes de l'horloge
chez les souris exposées à l'alcool et présentant une perturbation du
rythme circadien. Remarque :
nous suspectons une synergie significative entre le DMSO et la
photobiomodulation, mais nous ne disposons pas encore de suffisamment de
données pour tirer des conclusions définitives.
Améliorer l'apnée du sommeil :
Traitement intrapéritonéal à base d'une composition de plantes médicinales chinoises (Gastrodia elata) ⬖ et de Cinnamomum cassia ⬖ (dissoutes dans du DMSO) a réduit la pression et la fréquence du ronflement chez les rats âgés et a augmenté l'activité des nerfs phrénique, laryngé récurrent et hypoglosse, tout en prolongeant les temps inspiratoire, expiratoire et pré-inspiratoire, suggérant une modulation de l'activité neuronale des voies aériennes supérieures.
Chez des souris atteintes d'apnée obstructive du sommeil, le dronabinol, un agoniste cannabinoïde vagal, a réduit significativement les épisodes d'apnée du sommeil lorsqu'il était associé à 100 % de DMSO, mais pas lorsqu'il était associé à 25 % de DMSO (alors qu'à ces deux concentrations, le sommeil paradoxal était supprimé). <sup> 1,2 </sup> Par ailleurs, l'anandamide (un cannabinoïde endogène) a augmenté les niveaux de sommeil et d'adénosine dans le cerveau antérieur basal.
Dans un modèle d'hypoxie intermittente de l'apnée du sommeil chez des rats ayant subi des crises cardiaques, le Paxil a empêché l'hypoxie intermittente de provoquer une résistance systémique à l'insuline ou d'autres dommages au cœur lésé (par exemple, la fibrose et l'apoptose ont été réduites).
Contrer les effets néfastes du manque de sommeil chronique
Chez des souris, diverses substances, en association avec du DMSO, ont permis de contrer les effets néfastes d'une privation chronique de sommeil. La kaempféritrine (issue du fruit du moine) a augmenté la capacité antioxydante, réduit le stress oxydatif et l'obésité. L'astragaline a significativement amélioré le stress oxydatif hépatique. Les flavonoïdes de Siraitia grosvenorii et la mélatonine ont augmenté la capacité antioxydante et réduit le stress oxydatif et l'inflammation. L'almorexant a amélioré l'apprentissage et la mémoire spatiale et réduit l'astrogliose (neuro-inflammatoire). Un inhibiteur de la migration des macrophages … inhibiteur du facteur inhibiteur de la migration des macrophages a amélioré l'apprentissage et la mémoire spatiale et a partiellement protégé les neurones de l'hippocampe.
Modafinil (un stimulant utilisé pour augmenter l'éveil chez les personnes souffrant de privation chronique de sommeil) a diminué de manière significative le temps de sommeil total et augmenté la latence d'endormissement chez les bouledogues anglais souffrant de troubles respiratoires du sommeil, soulageant efficacement l'hypersomnolence (fatigue).
Chez les rats, le Paxil s'est dissous dans du DMSO (pour une mini-pompe osmotique) a prolongé de manière significative la durée des épisodes de sommeil paradoxal et a réduit le nombre d'épisodes de sommeil paradoxal sur plusieurs périodes de 6 heures (ce qui constitue un changement positif dans la privation chronique de sommeil).
Syndrome de Down et troubles du développement
Lorsque j'ai initialement examiné la littérature sur le DMSO, ce qui m'a le plus paru difficile à croire, c'était l'amélioration significative du syndrome de Down rapportée. Comme la plupart des médecins, je pensais qu'il s'agissait d'une maladie génétique incurable. Cependant, après avoir constaté les bienfaits rapportés dans de nombreuses études cliniques et les comptes rendus officiels du Congrès , j'ai réalisé que mon hypothèse était peut-être erronée et j'ai décidé de prendre le risque de publier ces données, au risque de compromettre ma crédibilité.
Peu après, j'ai reçu ces témoignages des parents d'une petite fille de deux ans atteinte du syndrome de Down. Son père a écrit en premier :
Nous donnons du DMSO à notre jeune fille atteinte de trisomie 21, ainsi que des vitamines supplémentaires (par exemple, des acides aminés ) , conformément au protocole de traitement de certaines études. Presque immédiatement, nous avons constaté une nette amélioration de son sommeil, une plus grande aisance à s'exprimer (elle semble désormais vouloir dire des mots plus intentionnellement) et un appétit nettement supérieur. Elle paraît beaucoup plus active, et c'est vraiment formidable !
Sa mère a ensuite enchaîné :
Même depuis la remarque de mon mari, nous avons constaté des changements chez notre petite fille. Le plus important, c'est qu'elle rampe maintenant ! Pendant longtemps, elle semblait complètement désintéressée, mais maintenant, elle s'y met (elle a commencé le jour de ses deux ans, d'ailleurs !). Sa coordination et sa motricité s'améliorent constamment, et elle est sur le point de s'asseoir toute seule, ce qui m'inquiétait beaucoup. C'est comme si elle n'était plus la même enfant qu'il y a deux semaines. Le DMSO a vraiment changé la donne pour nous. Je suis ravie de continuer à apprendre et à découvrir tout ce qui est possible !
L'expérience de ces parents fait écho à ce qui a été présenté lors d'une audition du Congrès en 1980, convoquée pour faire pression (sans succès) sur la FDA afin qu'elle mette fin à son embargo sur le DMSO, où un témoignage a été donné concernant un enfant atteint du syndrome de Down ayant eu une réponse tout aussi miraculeuse, mais sur une période beaucoup plus longue.
On y a évoqué le cas de Melody Clark, qui, à l'âge de 11 mois, avait commencé un traitement au DMSO prescrit par le Dr Jacob. À ce moment-là, ses jambes étaient « comme celles d'une poupée de chiffon », elle ne pouvait pas se retourner du dos sur le ventre et ses yeux ne parvenaient pas à se fixer. Son évaluation initiale, à six mois, avait prédit qu'elle ne progresserait jamais mentalement au-delà de l'âge de six ans.
Après sept ans de traitement au DMSO, Melody, qui était dans un état quasi végétatif selon un médecin, ne présentait plus qu'un léger retard de développement – un phénomène inédit chez un enfant atteint de trisomie 21, d'après ses enseignants. Concrètement, elle avait le niveau d'un élève de CE1 (excellente en mathématiques, lecture phonétique, orthographe et capacité à formuler des phrases complètes), savait sauter à la corde, faire des roulades et jouer sur un trampoline. Très appréciée de ses camarades, elle était passée d'une enfant solitaire observant les autres depuis l'autre côté de la classe à une enfant qui prenait l'initiative d'activités de groupe et participait activement avec ses pairs. Son enseignante a écrit au Congrès pour demander, au vu des progrès de Melody, que le DMSO fasse l'objet d'essais et d'évaluations rigoureux afin d'aider les personnes handicapées.
Son dentiste a également témoigné que son palais, sa mâchoire et sa langue avaient considérablement évolué vers la normale, un phénomène qu'il n'avait jamais observé chez ce type de patients. Le palais très proéminent de Melody à la naissance était désormais dans la norme.
Deux autres cas similaires ont également été signalés :
À 10 mois , Bronwyn Nash (atteinte de trisomie 21) était fragile et peinait à prendre du poids. Sa mère a alors commencé à lui administrer du DMSO. Elle a commencé à prendre du poids, a développé une conscience accrue des personnes et des objets qui l'entouraient et a commencé à tendre la main pour toucher les choses. À 18 mois, elle a pu se tenir debout, puis a pu accéder aux placards de sa mère, a commencé à manger seule et tenait bien son verre d'eau. Lorsqu'une journaliste spécialisée en santé lui a rendu visite à 28 mois, c'était une petite fille éveillée et joyeuse, très appréciée et aimée de sa famille, et son état s'améliorait constamment.
À 14 ans , Billy King pouvait marcher et se nourrir seul, mais son développement mental était celui d'un enfant de dix mois. Il a alors commencé à boire du lait additionné de DMSO chaque matin et, deux ans plus tard, son développement mental correspondait à celui d'un enfant de sept ans et il a commencé à perdre les caractéristiques physiques du syndrome de Down.
Il continua à progresser et finit par trouver un emploi dans une librairie de Portland.
Remarque : une autre version de
l’histoire de Billy King présente une chronologie différente (par
exemple, il a commencé à prendre du DMSO à 8 ans et non à 14, et a
également pris la formule d’acides aminés ⬖ ).
Des recherches existent pour étayer ces anecdotes incroyables.
• En Oregon , 67 enfants (âgés de 4 à 17 ans) atteints du syndrome de Down et présentant une déficience intellectuelle modérée ou sévère ont été répartis aléatoirement en deux groupes recevant une dose élevée ou faible de DMSO. Leurs résultats ont ensuite été comparés à ceux de 23 enfants similaires dont les parents refusaient l'administration d'un médicament expérimental. 1 , 2 Aucun effet secondaire n'a été observé et une amélioration dose-dépendante a été constatée.
Au Chili , 55 enfants atteints d'un handicap mental sévère dû au syndrome de Down (le plus âgé ayant 14 ans) ont reçu du DMSO et des acides aminés par injection intramusculaire ou ont servi de groupe témoin. Les flacons d'injection contenaient du DMSO ainsi que de l'acide gamma-aminobutyrique (GABA ) , de l'acide gamma-amino-bêta-hydroxybutyrique (GABOB ) et de l'acétylglutamine ( à doses réduites pour les enfants de moins de 3 ans et demi). Le développement des enfants a ensuite été évalué à l'aide des scores de Gesel et une amélioration significative a été observée dans le groupe DMSO.
Remarque : cette étude (et les améliorations supplémentaires qui y ont été apportées) peut être consultée ici et ici .
En Argentine , 13 enfants handicapés mentaux (5 cas graves, 4 cas modérés et 4 cas légers), qui n'étaient pas atteints du syndrome de Down, ont reçu un mélange d'acides aminés DMSO ( connu sous le nom de Merinex) trois fois par semaine par injection pendant 180 jours (avec des périodes périodiques de 15 jours où les acides aminés sans DMSO étaient administrés par voie orale).
Remarque : d’autres auteurs ont rapporté que des patients jeunes (et plus âgés) présentant des difficultés d’apprentissage, un faible quotient intellectuel, un TDAH, des troubles anxieux, de l’épilepsie, de la nervosité, une dyscalculie, une dyslexie, de la fatigue et des problèmes de concentration bénéficient tous de ce protocole. De plus, certains ont avancé que l’ajout de galactose en renforce l’efficacité.
Dans une étude de 1969 , 44 enfants souffrant d'un retard de développement sévère ont reçu le mélange d'acides aminés DMSO ⬖ , dont beaucoup ont connu une capacité d'apprentissage accrue dans un laps de temps relativement court et plus de 70 % ont eu des réponses favorables telles que « une augmentation du QI, des progrès évidents et accélérés dans les acquis de base, une amélioration globale de la capacité intellectuelle, des progrès évidents en lecture, en écriture et en mathématiques, une meilleure coordination des mouvements et une habileté manuelle améliorée, et une diminution des problèmes de comportement », ainsi qu'une meilleure maîtrise psychomotrice, la disparition des accès de colère sans raison, une réduction générale de l'irritabilité et une diminution de la désobéissance.
Une autre étude de 1969 a administré le mélange d'acides aminés DMSO pendant six mois à 30 enfants présentant des troubles d'apprentissage et des troubles du langage (sans maladie neurologique associée) et les a comparés à 20 témoins, et a observé que cela entraînait :
• Disparition de la léthargie mentale.
• Apparition de réactions sensorielles.
• Disparition des mouvements automatiques.
• Disparition de l'inertie, de la passivité et de la négativité.
• Intérêt et initiative croissants dans les tâches et les activités.
• Amélioration de l'expression corporelle et du langage oral.
• Activité lucide, interactions sociales et disparition de l'agressivité non provoquée.
• Perte de la timidité et développement de l'estime de soi.
• Acquisition de l'autonomie pour accomplir les tâches ménagères, faire les courses, manger et s'habiller sans aide, etc.
• Apprentissage de la lecture, de l'écriture et des devoirs.
Une étude chilienne de 1976 a administré du DMSO et des acides aminés (GABA, GABOB , L-acétylglutamine et arginine ) à 15 enfants (âgés de moins de 3 ans et demi ) atteints du syndrome de Down et les a comparés à 13 enfants témoins non traités. Après 12 mois de traitement intensif, selon le quotient de développement de Gesell, la moyenne des scores moteurs est passée de 56 à 72, celle des scores adaptatifs de 50 à 66, celle des scores langagiers de 52 à 58 et celle des scores sociaux de 40 à 64 (de nombreux enfants ont enregistré une amélioration supérieure à 10 points, notamment dans les domaines moteur, adaptatif et social), tandis que les scores des enfants témoins sont restés globalement inchangés. Les améliorations physiques observées chez les enfants traités incluaient une réduction de la macroglossie, une meilleure expressivité faciale, une augmentation du tonus et de la coordination musculaire, ainsi que des modifications posturales. Au cours de la phase de maintien de six mois (soit 18 mois au total), les progrès des enfants traités se sont globalement maintenus, voire légèrement améliorés (par exemple, motricité : 74 ; adaptation : 69 ; compétences sociales : 67), sans régression significative et avec seulement quelques pertes mineures et isolées (par exemple, au niveau du langage pour quelques-uns), tandis que les enfants du groupe témoin n’ont montré aucun progrès ou de légers reculs. Les auteurs n’ont constaté aucun effet indésirable significatif et ont conclu qu’une intervention précoce semblait bénéfique pour la stimulation et le développement neuronal . <sup> 1,2,3 </sup>
Un auteur a fait état d'une étude argentine (que je n'ai pas pu retrouver) menée par ce médecin , dans laquelle 18 enfants atteints du syndrome de Down ont reçu du DMSO et des acides aminés ⬖ et ont été comparés à 91 témoins, et pour citer l'auteur, cela a donné les résultats suivants :
une tendance à une maturation accélérée chez les enfants traités, avec des progrès marqués dans l'intégration du langage ; ceci a pu être établi de manière statistiquement significative chez les enfants traités
De plus :
• Cette étude , ainsi que cette autre étude , ont également constaté que le mélange d’acides aminés DMSO était bénéfique aux enfants présentant un handicap développemental. • Une revue de la littérature espagnole de 1982 a mis en lumière le DMSO comme traitement potentiel du syndrome de Down. • Un ouvrage russe sur le diabète, paru en 2009, préconisait l’application
régulière d’un mélange topique de DMSO, de peroxyde d’hydrogène et de
sulfate de cuivre pour le diabète et la régénération tissulaire. Il
citait le cas d’une femme enceinte dont le fœtus était atteint du
syndrome de Down ; cette femme avait suivi ce protocole et avait ensuite
donné naissance à un enfant en bonne santé. • Des articles de 1980 et 1982 , rédigés par des médecins sceptiques, reconnaissaient que le DMSO était étudié comme traitement potentiel du syndrome de Down.
Remarque : outre le syndrome de Down, la communauté allemande du DMSO a connu un succès significatif en utilisant le DMSO et les acides aminés ⬖ pour les troubles d'apprentissage, les retards de développement, les troubles de l'humeur et de l'anxiété, et les maladies neurodégénératives, dont les troubles d'apprentissage mineurs ou graves constituent l'application la plus courante.
Autisme
L'une des questions les plus fréquentes que l'on me pose est de savoir si le DMSO peut être utilisé pour traiter l'autisme (car de nombreux facteurs mécanistiques plaident en sa faveur), mais malheureusement, mis à part quelques témoignages vagues de parents que j'ai pu trouver suggérant son efficacité (que je n'ai pas pu corroborer), je ne dispose d'aucune donnée parentale directe pour répondre à cette question.
Cependant, plusieurs études menées sur des souris (modifiées pour modéliser l'autisme) ont montré que le DMSO, en association avec un autre traitement, atténuait leurs comportements de type autistique. Plus précisément, avec le DMSO :
L'épothilone D (un agent stabilisateur des microtubules) a amélioré les comportements répétitifs de type autistique dans plusieurs études 1,2,3,4,5,6 > grâce à un mécanisme constant : stabilisation des microtubules, augmentation du nombre de synapses excitatrices et amélioration de l'expression de la protéine basique de la myéline dans le cortex cérébral. Ces études ont systématiquement mis en évidence une réduction du temps consacré au toilettage et une amélioration des aptitudes sociales. Certaines études ont également démontré une amélioration des comportements répétitifs restreints lors des tests d'enfouissement de billes, une normalisation de la myélinisation et une augmentation de la densité des épines dendritiques .
La curcumine a amélioré la sociabilité, réduit les comportements répétitifs et restauré la neurogenèse hippocampique dans de nombreuses études 1,2,3,4 , avec des résultats constants montrant une augmentation du nombre de neurones hippocampiques et une réduction du nombre excessif d'astrocytes (un élément clé du processus pathologique), ainsi qu'une amélioration de l'apprentissage, de la mémoire et de la communication sociale. Des études individuelles ont également montré que la curcumine favorisait la prolifération des cellules progénitrices neurales, augmentait le nombre de cellules gliales radiales dans la zone sous-granulaire et améliorait la maturation des nouveaux neurones 1
L' administration prénatale de resvératrol a empêché l'exposition embryonnaire à l'acide valproïque de provoquer des caractéristiques comportementales de type autistique, notamment des déficits du comportement de recherche du nid, des interactions sociales et une hyperexcitation du système glutamatergique cérébral. 1,2 La mélatonine et la wortmannine (un inhibiteur de PI3K) ont amélioré les comportements de type autistique, favorisé la synthèse des protéines synaptiques et amélioré le développement des épines dendritiques. La wortmannine seule a permis de rétablir la densité des épines dendritiques, d'augmenter l'expression de la protéine de densité postsynaptique et d'inhiber la même voie que celle ciblée par la rapamycine.
D'autres agents améliorant les comportements de type autistique dans les modèles murins comprennent un antagoniste du récepteur 5-HT2A (qui a atténué l'auto-toilettage répétitif), un antagoniste du S1PR1 (qui a amélioré l'apprentissage et la mémoire tout en préservant la densité neuronale de l'hippocampe et l'intégrité microvasculaire), l'estradiol (qui a restauré l'empathie et l'affection sociale chez les souris ovariectomisées) et la baicaline ⬖ (qui a amélioré la reconnaissance et la mémoire spatiale de manière dose-dépendante tout en augmentant le BDNF et le nombre de neurones sains dans l'hippocampe).
Collectivement, ces études utilisant une grande variété de thérapies qui ont en commun le DMSO suggèrent que le DMSO pourrait également améliorer l'autisme de manière indépendante, mais comme le DMSO est rarement, voire jamais, comparé à un placebo salin dans ce type d'études, il est impossible de le savoir.
Remarque : des résumés complets de chaque étude sont disponibles dans mon Substack de référence ici .
Autres troubles du développement
Paralysie cérébrale : Compte tenu de la capacité du DMSO à réparer les lésions du système nerveux central, notamment celles dues à une interruption temporaire du flux sanguin (et de son effet bénéfique sur la spasticité musculaire), il semble plausible que le DMSO puisse être utile dans le traitement de la paralysie cérébrale. Malheureusement, cette hypothèse n’a pas été étudiée et la seule publication que j’ai trouvée sur le sujet indique que le DMSO associé à la vertéporfine restaure partiellement la capacité des cellules satellites musculaires à se différencier correctement, ce qui pourrait réduire leur spasticité.
Cependant, chez les chevaux, un article passant en revue des manuels vétérinaires a rapporté que le DMSO traite les lésions cérébrales néonatales (par exemple, l'encéphalopathie hypoxique-ischémique) et les coliques chez les poulains, tandis qu'un autre livre a rapporté que le vétérinaire Jack Metcalf avait constaté que des chevaux handicapés au développement à la naissance (au point de ne pas pouvoir téter) retrouvaient la capacité de téter après avoir reçu du DMSO par voie intraveineuse trois fois par jour et que le DMSO accélère leur développement global.
Enfin,
l'une des manifestations les plus fréquentes et invalidantes de la
paralysie cérébrale est une spasticité musculaire sévère (au point que
des mesures invasives comme les injections de toxine botulique sont
couramment utilisées). Chez des patients atteints de spasticité
musculaire sévère, des chercheurs russes ont rapporté des résultats
positifs avec l'application topique, facilitée par ultrasons, d'un
mélange de DMSO, d'oxybutyrate de sodium (GHB, un somnifère puissant que la
FDA a combattu) et de lidocaïne sur les muscles affectés et les
segments médullaires concernés. Dans le brevet détaillé (que j'ai
traduit ici ),
ils ont notamment évoqué le cas d'un patient ayant développé une
spasticité invalidante suite à une arachnoïdite, mais ont laissé
entendre que ce traitement pourrait être utilisé pour améliorer la
mobilité dans d'autres affections comme la poliomyélite ou la paralysie
cérébrale. Parallèlement, une lectrice, dont
la fillette de neuf ans, atteinte de paralysie cérébrale affectant
trois membres et sans déficience cognitive, a témoigné que sa fille lui
avait confié que l'application topique de DMSO détendait ses muscles
contractés et lui permettait de bouger plus facilement.
Note : un autre brevet russe proposait le
DMSO comme potentialisateur transdermique pour un patch de Botox
destiné au traitement de la spasticité associée à la maladie de
Parkinson, à la paralysie cérébrale, à la dystonie et à la sclérose en
plaques, permettant potentiellement d’éviter les injections répétées de
Botox actuellement nécessaires. En dehors de ce brevet, je n’ai observé
que des formulations de Botox à base de DMSO utilisées pour
l’hyperactivité vésicale idiopathique réfractaire (où elles se sont
avérées efficaces).
Fente palatine :
la phénytoïne, un des premiers antiépileptiques, était connue pour
provoquer diverses malformations congénitales, dont certaines (comme une
racine du nez plate et des plis épicanthiques) peuvent ressembler à des
caractéristiques du syndrome de Down. Une étude a montré que le DMSO prévenait certaines de ces malformations (par exemple, la fente palatine) induites par la phénytoïne.
Syndrome neurodéveloppemental lié à ACBD6 : cette maladie rare provoque également des troubles cognitifs et des malformations congénitales semblables à celles observées dans le syndrome de Down. Bien que le DMSO n’ait pas été testé chez les patients atteints de ce syndrome, ce dernier est causé par une activité déficiente de la N-myristoyltransférase, une enzyme dont l’activité est augmentée in vitro par le DMSO .
Maladie de Krabbe : il s’agit d’une maladie génétique lysosomale rare et incurable, responsable d’une neurodégénérescence sévère et d’un retard de développement important dès la naissance. Une publication de 1999 révélait que Stanley Jacob avait mis au point et appliqué un protocole d’administration orale de DMSO pour cette maladie, mais son efficacité reste incertaine.
Syndrome de Tourette : chez les rats modèles de la maladie , la vitamine D ⬖ (1,0 μg/kg/jour) dans le DMSO a diminué de manière significative les comportements locomoteurs (scores de 0,43 à 0,69 contre 0,92 à 1,33) et a inversé la diminution du contenu en dopamine striatale (tout en provoquant une augmentation attendue du calcium sérique induite par la vitamine D ⬖ ).
Remarque : beaucoup de personnes se demandent si le DMSO pourrait aider en cas de dystrophie musculaire. La seule étude que j’ai trouvée montre que la (-)-épicatéchine ⬖ présente dans le DMSO réduit la pathologie des fibres dystrophiques et favorise la régénération musculaire chez des souris atteintes de dystrophie musculaire, mais sans aborder le mécanisme sous-jacent de la maladie – ce qui, malheureusement, ne nous apprend pas grand-chose.
Un nouveau modèle de neurologie
J’espère que cette lecture vous aura non seulement donné l’espoir de traiter de nombreuses affections neurologiques « incurables », mais aussi que vous partagerez ma fascination pour la nouvelle perspective qu’elle offre sur les causes profondes de nombre de ces maladies.
Par
ailleurs, bien que cet article soit long, vous aurez peut-être remarqué
que de nombreuses affections neurologiques ont été omises. Ceci est dû à
sa longueur (en raison de tous ses liens), qui a provoqué la saturation
de Substack et a donc nécessité sa division en plusieurs parties.
Ainsi, en plus des articles précédents que j'ai écrits montrant que le
DMSO procure des bienfaits neurologiques similaires à chacun des organes
sensoriels (par exemple, les yeux et les oreilles ), les prochains articles de cette série aborderont les effets remarquables du DMSO sur :
•
Les problèmes de colonne vertébrale (par exemple, la paralysie, les
lésions de la moelle épinière, les hernies discales, les radiculopathies
et l'arachnoïdite).
• Troubles des nerfs périphériques (p. ex., régénération nerveuse, paralysies, neuropathies et douleurs neuropathiques).
• Accidents vasculaires cérébraux, hémorragies cérébrales, traumatismes crâniens et commotions cérébrales.
Dans la dernière partie de cet article, je partagerai des conseils pratiques pour obtenir correctement chaque qualité de DMSO (y compris le DMSO IV), je fournirai des protocoles spécifiques pour les affections neurologiques abordées ici — notamment la maladie de Parkinson, la maladie d'Alzheimer, les accidents vasculaires cérébraux, le stress chronique, les neuropathies, les troubles cognitifs, le brouillard cérébral, la toxicité de l'anesthésie et les troubles neurodéveloppementaux — et je mettrai en lumière les thérapies naturelles complémentaires que nous avons trouvées bénéfiques pour ces affections.
- Obtenir le lien
- X
- Autres applications

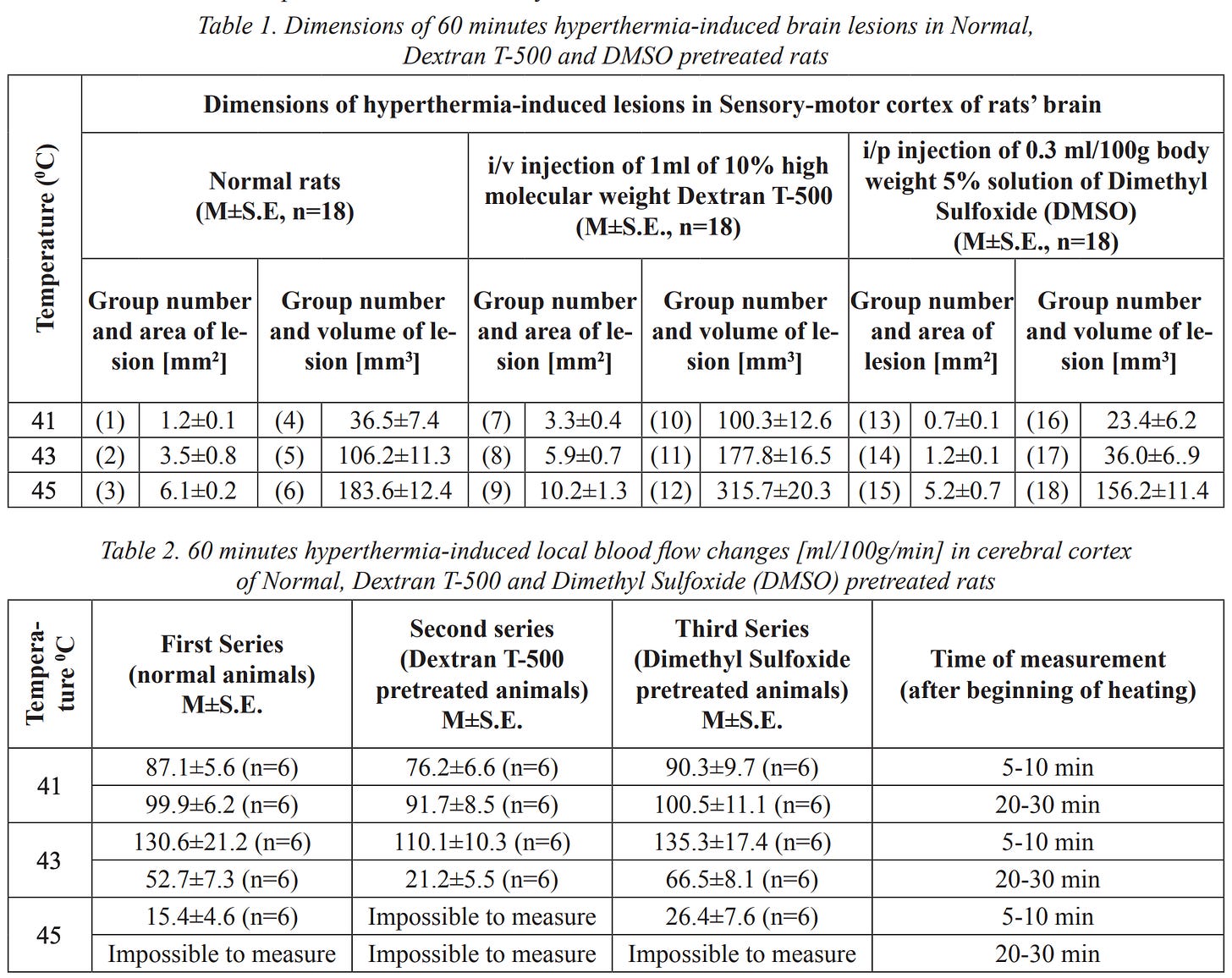
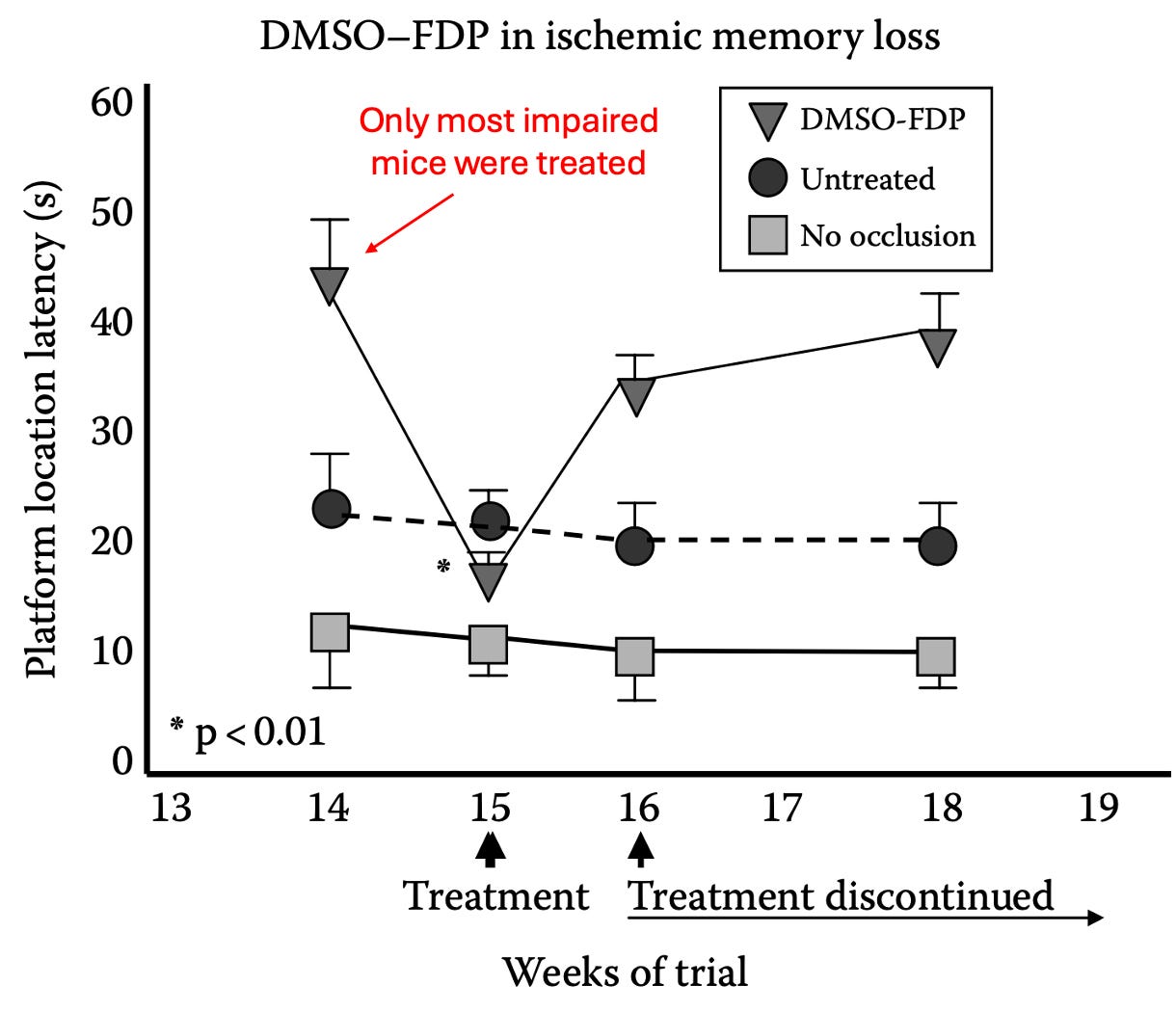






Commentaires
Enregistrer un commentaire