Le bleu de méthylène pour "inverser les symptômes neurocognitifs" et lutter contre les maladies à prions
De : https://anamihalceamdphd.substack.com/p/methylene-blue-prevents-and-reverses?
Le bleu de méthylène prévient et inverse la maladie à prions, la formation de caillots amyloïdes et caoutchouteux, lie les polymères des hydrogels et dissout les éléments constitutifs des nanotechnologies.
Image : Le bleu de méthylène inhibe la nucléation et l'élongation des fibrilles amyloïdes SOD1.
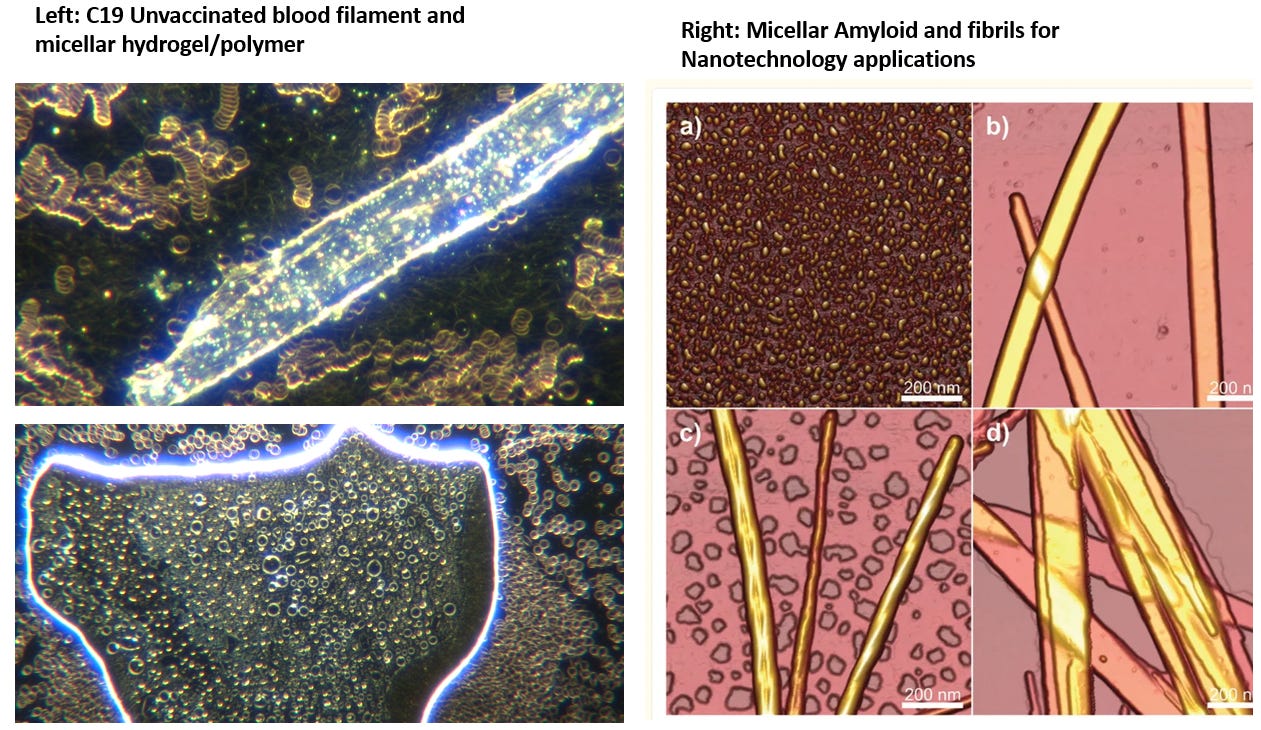
Dans les derniers numéros, j'ai parlé des protéines de type prion, des polymères de type amyloïde, de leur utilisation en nanotechnologie et de leur relation avec l'arme biologique C19. Ceci afin d'expliquer les récents résultats des recherches menées par le Dr. Diana Wojtkowiak sur les caillots sanguins vaccinés contre le C19 chez les personnes décédées. J'ai comparé ces résultats aux recherches de Clifford Carnicom et de moi-même sur les polymères protéiques polyamides, ainsi qu'à mes conclusions sur l'analyse du sang vivant, et l'on peut voir les similitudes apparentes :
Methylene blue inhibits amyloid Abeta oligomerization by promoting fibrillization
Le bleu de méthylène a inhibé l'oligomérisation lorsqu'il était utilisé à des concentrations substoichiométriques par rapport à celles du monomère Abeta. L'inhibition de l'oligomérisation de l'Abêta a été obtenue en même temps que la promotion de la fibrillation, ce qui suggère que la formation d'oligomères et de fibrilles sont des voies distinctes et concurrentes. La promotion de la formation de fibres par le bleu de méthylène s'est faite par une diminution dose-dépendante du temps de latence et une augmentation de la vitesse de fibrillation, ce qui est cohérent avec la promotion de la nucléation et de l'élongation des filaments. L'ajout de bleu de méthylène à des oligomères préformés a entraîné la perte d'oligomères et la promotion de la fibrillation. Ces données montrent que la formation d'oligomères Abeta est inhibée par la promotion de la formation de fibrilles, ce qui suggère que l'importance pathologique relative des oligomères et des fibrilles peut être testée in vivo en utilisant le bleu de méthylène. Si les oligomères Abeta représentent la principale espèce pathogène, l'inhibition de cette espèce hautement toxique par la promotion de la formation d'agrégats moins toxiques pourrait être utile sur le plan thérapeutique.
L'article suivant aborde également les différents mécanismes par lesquels le MB inhibe la formation de fibrilles ou de filaments amyloïdes.
Methylene blue inhibits amyloid Abeta oligomerization by promoting fibrillization
Le bleu de méthylène a inhibé l'oligomérisation lorsqu'il était utilisé à des concentrations substoichiométriques par rapport à celles du monomère Abeta. L'inhibition de l'oligomérisation de l'Abêta a été obtenue en même temps que la promotion de la fibrillation, ce qui suggère que la formation d'oligomères et de fibrilles sont des voies distinctes et concurrentes. La promotion de la formation de fibres par le bleu de méthylène s'est faite par une diminution dose-dépendante du temps de latence et une augmentation de la vitesse de fibrillation, ce qui est cohérent avec la promotion de la nucléation et de l'élongation des filaments. L'ajout de bleu de méthylène à des oligomères préformés a entraîné la perte d'oligomères et la promotion de la fibrillation. Ces données montrent que la formation d'oligomères Abeta est inhibée par la promotion de la formation de fibrilles, ce qui suggère que l'importance pathologique relative des oligomères et des fibrilles peut être testée in vivo en utilisant le bleu de méthylène. Si les oligomères Abeta représentent la principale espèce pathogène, l'inhibition de cette espèce hautement toxique par la promotion de la formation d'agrégats moins toxiques pourrait être utile sur le plan thérapeutique.
L'article suivant aborde également les différents mécanismes par lesquels le MB inhibe la formation de fibrilles ou de filaments amyloïdes.
Exploring the effects of methylene blue on amyloid fibrillogenesis of lysozyme
Il a été démontré que le lysozyme de 129 résidus forme des fibrilles amyloïdes in vitro. S'il a été démontré que le bleu de méthylène (MB), un composé de la famille des phénothiaziniums, dissocie la formation de fibrilles de tau, son effet antifibrillogène n'a pas été caractérisé de manière approfondie sur d'autres protéines/peptides. Cette étude examine les effets de la MB sur la fibrillogénèse in vitro du lysozyme à un pH de 2,0 et à 55 °C. Nos résultats ont montré qu'après 7 jours d'incubation, le plateau de fluorescence ThT de l'échantillon était de ~8,69 % ou ~2,98 % du contrôle lorsque le rapport molaire entre le lysozyme et la MB était de 1:1,11 ou de 1:3,33, respectivement, ce qui indique que le pouvoir inhibiteur de la MB contre la fibrillogénèse du lysozyme est positivement corrélé à sa concentration. Nous avons également constaté que la MB est capable de déstabiliser les fibrilles de lysozyme préformées. En outre, les résultats des simulations d'amarrage moléculaire et de dynamique moléculaire ont révélé que le mécanisme d'inhibition de la formation de fibrilles par la MB peut être déclenché par la liaison avec la région du lysozyme sujette à l'agrégation. Les résultats rapportés ici apportent un soutien solide à l'effet de la MB sur la fibrillogénèse amyloïde.
La MB est également considérée comme un agent thérapeutique efficace dans cet article de synthèse :
D'autres recherches montrent que l'élongation des filaments est inhibée ainsi que d'autres structures d'agrégats :
Methylene blue inhibits nucleation and elongation of SOD1 amyloid fibrils
L'agrégation de protéines en fibrilles amyloïdes hautement structurées est liée à plusieurs maladies neurodégénératives. La formation de fibrilles par la superoxyde dismutase I (SOD1) est considérée comme liée à la sclérose latérale amyotrophique, une maladie mortelle à déclenchement tardif. Malgré de nombreux efforts et la découverte de nombreux composés anti-amyloïdes, aucun traitement efficace n'est actuellement disponible. Il a été démontré que le bleu de méthylène (MB), un colorant phénothiazine, module l'agrégation de plusieurs protéines amyloïdogènes. Dans ce travail, nous montrons sa capacité à inhiber à la fois l'agrégation amyloïde spontanée de la SOD1 et l'élongation des fibrilles préformées.
Dans cet article, le mécanisme par lequel la MB inhibe la formation d'amyloïde dans la maladie d'Alzeimer est discuté.
Le bleu de méthylène (MB) de phénothiazine attire de plus en plus l'attention car il semble avoir des effets bénéfiques dans la pathogenèse de la maladie d'Alzheimer (MA). Entre autres facteurs, la présence de plaques neuritiques d'agrégats de peptide amyloïde-β (Aβ), d'enchevêtrements neurofibrilaires de tau et de perturbation du Ca2+ cytosolique sont des acteurs importants de la maladie. Il a été proposé que MB diminue la formation de plaques neuritiques dues à l'agrégation d'Aβ. Cependant, le mécanisme moléculaire qui sous-tend cet effet est loin d’être clair. Dans ce travail, nous montrons que MB stimule l'activité Ca2+-ATPase de la Ca2+-ATPase (PMCA) de la membrane plasmique dans les tissus humains provenant de cerveaux atteints de MA et de contrôles du même âge, ainsi que de cultures de cerveaux et de cellules de porc. De plus, MB prévient et même bloque l’effet inhibiteur de l’Aβ sur l’activité PMCA. L'analyse fonctionnelle avec des mutants et des expériences de fluorescence suggèrent fortement que MB se lie au PMCA, au niveau de la queue C-terminale, dans un site situé à proximité de la dernière hélice transmembranaire et également que MB se lie au peptide. En outre, Aβ augmente l’affinité du PMCA pour MB.
Il s’agit d’une étude animale qui montre que la SEP inverse réellement les dommages déjà causés par les dépôts amyloïdes dans le cerveau et améliore la fonction cérébrale.
La protéolyse de la protéine précurseur amyloïde (APP) est nécessaire à la production de peptides amyloïdes-β (Aβ) qui comprennent les plaques β-amyloïdes dans le cerveau des patients atteints de la maladie d'Alzheimer (MA). Ici, nous avons testé si l'agent expérimental bleu de méthylène (MB), utilisé pour le traitement de la méthémoglobinémie, pourrait améliorer la pathologie de type MA et les déficits comportementaux. Nous avons administré par voie orale du MB au modèle murin transgénique PSAPP âgé d'amylose cérébrale et évalué la fonction cognitive et la pathologie amyloïde cérébrale. À partir de l'âge de 15 mois, les animaux ont été gavageés avec du MB (3 mg/kg) ou un véhicule une fois par jour pendant 3 mois. Le traitement MB a empêché de manière significative les troubles du comportement associés aux transgènes, notamment l'hyperactivité, la diminution de la reconnaissance des objets et une mémoire de travail et de référence spatiale défectueuse, mais il n'a pas modifié le comportement des souris non transgéniques. De plus, les dépôts de β-amyloïde parenchymateux et vasculaires cérébraux ainsi que les niveaux de diverses espèces d'Aβ, y compris les oligomères, ont été atténués chez les souris PSAPP traitées au MB. Ces effets se sont produits avec l’inhibition de la protéolyse amyloïdogène de l’APP. Plus précisément, l’expression et l’activité du fragment APP β-carboxyl-terminal et de l’enzyme 1 de clivage du site β APP ont été atténuées. De plus, le traitement des cellules ovariennes de hamster chinois surexprimant l'APP de type sauvage humain avec du MB a considérablement réduit la production d'Aβ et la protéolyse amyloïdogène de l'APP. Ces résultats soulignent le potentiel du traitement oral par MB contre l’amylose cérébrale liée à la MA en modulant la voie amyloïdogène.
J'ai beaucoup écrit sur la thérapie photodynamique avec MB dans mon livre Light Medicine - A New Paradigm - The Science of Light, Spirit and Longevity. L'étude ci-dessous montre que le MB activé par la lumière inhibe l'auto-assemblage des nanoamyloïdes et dissout leurs structures.
L'agrégation anormale des peptides β-amyloïdes (Aβ) est une caractéristique majeure de la maladie d'Alzheimer (MA). Malgré de nombreuses tentatives visant à prévenir la β-amylose, aucun médicament efficace pour traiter la MA n’a été développé à ce jour. Parmi les nombreux produits chimiques candidats, le bleu de méthylène (MB) a prouvé son potentiel thérapeutique contre la MA dans un certain nombre d'études in vitro et in vivo ; mais le résultat des récents essais cliniques réalisés avec MB et ses dérivés s'est révélé négatif. Ici, à l’aide de multiples analyses photochimiques, nous rapportons d’abord que les molécules de MB photoexcitées peuvent bloquer l’agrégation de Aβ42 in vitro. De plus, notre étude in vivo utilisant le modèle Drosophila AD démontre que le MB photoexcité est très efficace pour supprimer la toxicité synaptique, entraînant une réduction des dommages à la jonction neuromusculaire (NMJ), une amélioration de la locomotion et une diminution de la vacuole dans le cerveau. L'effet d'entrave est attribué à l'oxydation de l'Aβ42 par l'oxygène singulet (1O2) généré à partir du MB photoexcité. Enfin, nous montrons que les MB photoexcités possèdent la capacité de désagréger les agrégats Aβ42 préexistants et de réduire la cytotoxicité induite par l'Aβ. Nos travaux suggèrent que l’éclairage peut offrir l’opportunité d’augmenter l’efficacité du MB en faveur d’une thérapie photodynamique de la MA à l’avenir.
Voici d’autres articles concernant mes observations et recherches sur le bleu de méthylène en tant que molécule puissante et utile en ces temps difficiles. J'avais également déjà discuté des effets sur les hydrogels polymères dans les articles ci-dessous :
Methylene Blue Prevents Rubbery Clot Formation, Essential Oils Help Too - Experiment Documentation
Il convient de noter que lors de la spectroscopie de torsion des caillots, du cuivre, du zinc et du sélénium ont été trouvés. Dans cette étude, l’EDTA bloque l’interaction du métal avec l’amyloïde, favorisant ainsi la dissolution. Je recommande toujours fortement l'EDTA car je l'ai trouvé cliniquement très utile pour éliminer les contaminants métalliques qui contribuent à la construction des biocapteurs nanotechnologiques.
L'accumulation d'agrégats β-amyloïde (Aβ) induite par Cu2+/Zn2+ en conjonction avec la toxicité est étroitement liée à la maladie d'Alzheimer (MA). Ici, nous avions l'intention d'améliorer l'efficacité et la sélectivité du chélateur traditionnel de l'acide éthylènediaminetétraacétique (EDTA) combiné à un groupe fluorescent acide 4-aminosalicylique (4-ASA) pour acquérir un nouveau chélateur potentiel 4,4′-((2,2′- (acide éthane-1,2-diylbis((carboxyméthyl)azanediyl))bis(acétyl))bis(azanediyl))bis(2-hydroxybenzoïque) (EDTA-ASA) capable de désagréger l'Aβ-Cu(II)/ Zn(II ) agrégats. L'EDTA-ASA combine le 4-ASA en tant que fluorophore et groupes aminés multidentés, hydroxyle et carboxyle pour chélater le Cu2+ des agrégats Aβ-Cu (II). La sélectivité spécifique de l'EDTA-ASA envers Cu2+ dans une solution tampon Tris-HCl a été étudiée par des mesures de fluorescence. Il présente une reconnaissance élevée du Cu2+ sans interférence significative d'autres ions métalliques compétitifs, ce qui surmonte les carences de l'EDTA. Il est important de noter que les sites de liaison et le mode de liaison du Cu2+ ont été clarifiés grâce aux calculs DFT. Les analyses de fluorescence de la thioflavine-T (ThT) et les résultats de la microscopie électronique à transmission (TEM) ont révélé que l'EDTA-ASA présentait une capacité de désagrégation améliorée sur les agrégats Aβ-Cu (II)/Zn (II) par rapport à l'EDTA. L'affinité chélatante du Cu2+ était suffisante pour que l'EDTA-ASA séquestre le Cu2+ des agrégats Aβ-Cu (II).
Résumé:
Dans cet article, je passe en revue plusieurs études qui discutent du bleu de méthylène en tant que dissolvant de polymères amyloïdes et prions qui sont non seulement créés par le corps « naturellement », mais peuvent être introduits de manière externe à des fins nanotechnologiques. Les prions sont hautement contagieux. Les peptides amyloïdes et prions ont été utilisés pour fabriquer des hydrogels, des dispositifs nanotechnologiques et des biocapteurs. Ce sont les éléments constitutifs de l’interface cerveau-ordinateur et de la surveillance par télémétrie bidirectionnelle WBAN.
Le bleu de méthylène doit être considéré comme une option préventive et thérapeutique en association avec de fortes doses de vitamine C, d'EDTA et d'autres traitements de soutien pour l'inhibition et la dissolution de la formation de caillots caoutchouteux, de la maladie à prions induite par les armes biologiques C19 et de l'amylose, ainsi qu'en tant que puissant dissolvant de l’assaut des nanotechnologies d’auto-assemblage contre l’humanité.
L'EDTA modifié a reconnu sélectivement Cu2+ et son application
Traduction non relue mais ENFIN complète



Commentaires
Enregistrer un commentaire