La chélation à l'EDTA dissout l'arme magnétique de l'intelligence artificielle
La chélation (prononcer kélassion ) est un processus physico-chimique au cours duquel est formé un complexe, le chélate, entre un ligand, dit « chélateur » (ou chélatant), et un cation (ou atome) métallique, alors complexé, dit « chélaté » Wikipedia
********************
De : https://anamihalceamdphd.substack.com/p/edta-chelation-dissolves-the-artificial?
L'examen des brevets montre des données qui permettent de l'espoir
Je préconise depuis des mois que la chelation EDTA soit une solution de traitement pour les injectés C19 , car il élimine efficacement les métaux et peut détoxifier le corps même du graphène. En tant que praticien certifié en chélation, il est évident pour moi que l'EDTA est nécessaire contre le bombardement environnemental de cette forme de vie parasitaire de l'IA, à laquelle nous sommes exposés via des injections de C19, des chemtrails, l'excrétion de vax, de la nourriture, des cosmétiques, des médicaments et de nombreux autres éléments.
Nous savons maintenant que la nanotechnologie d'auto-assemblage qui atteint la taille du micromètre se développe à partir des nanoparticules lipidiques. Karen Kingston a trouvé les brevets :
Mon collègue, le Dr Shimon Yanowitz, a montré que les nanoparticules métalliques s'auto-assemblent à partir des liposomes.
La seule chose qui n'est pas cohérente, c'est l'échelle. Nous voyons la taille du micromètre et ils parlent d'une taille de nanomètre. Cela montre que l'auto-assemblage est déjà actif lors de la décongélation des flacons de C19.
Le brevet précise :
HYDROGELS D'OPALE INVERSE RESPECTUEUX DES CELLULES POUR L'ENCAPSULATION CELLULAIRE, LA LIVRAISON DE MÉDICAMENTS ET DE PROTÉINES ET LES NANOPARTICULES FONCTIONNELLES
DOMAINE DE L'INVENTION
L'invention concerne des échafaudages polymères pour l'ingénierie tissulaire à base de cellules.
CONTEXTE
L'ingénierie tissulaire est une approche de régénération, de remplacement et d'amélioration des fonctions des tissus endommagés en manipulant des matériaux en fonction de la structure ou de la fonction spécifique des tissus souhaités. Des échafaudages polymères poreux et biodégradables, par exemple des échafaudages interconnectés en trois dimensions, sont utilisés comme matrice de support structurel ou comme substrat adhésif cellulaire pour l'ingénierie tissulaire à base de cellules. Une structure poreuse très ouverte avec des pores interconnectés est nécessaire pour obtenir un ensemencement et une migration cellulaire suffisants dans l'échafaudage, ainsi que pour faciliter le transfert de masse des nutriments, de l'oxygène et des déchets de métabolites pour la prolifération séquentielle et la différenciation d'une grande quantité de cellules. Les approches actuelles pour générer des réseaux poreux dans les échafaudages en polymère comprennent le moussage de gaz, la lixiviation au sel et la lyophilisation ; cependant, les limites de ces processus comprennent des tailles, des formes et des structures de pores irrégulières, ainsi qu'une interconnectivité limitée. En tant que tel, il existe un besoin pressant dans l'art de développer des échafaudages polymères structurés améliorés avec des pores interconnectés.
RÉSUMÉ DE L'INVENTION
L'invention décrite ici propose la fabrication d'hydrogels d'opale inverse respectueux des cellules qui permettent également l'encapsulation des cellules dans la matrice d'hydrogel. Dispositif d'échafaudage d'hydrogel opale inverse comprenant une matrice polymère et un porogène sacrificiel dans lequel le porogène comprend un polymère ioniquement réticulé, un polymère thermosensible, un polymère sensible au pH ou un polymère photoclivable. La matrice polymère est constituée d'un polymère durable par rapport au porogène sacrificiel de sorte que la matrice polymère résiste aux changements physiques ou chimiques qui provoquent le sacrifice du porogène. Par exemple, la matrice polymère est réticulée de manière covalente, résiste à un changement (par exemple, augmentation) de température, résiste à un changement de pH (par exemple, diminution) ou à un changement de force ionique ou de composition (par exemple, contact avec un chélateur de cation divalent), ou résiste à l'exposition à la lumière (par exemple, la lumière UV).
Pour les applications d'ingénierie tissulaire et d'échafaudage cellulaire, la matrice polymère comprend en outre une cellule isolée, par exemple une cellule eucaryote. Par « cellule isolée », on entend une cellule qui a été séparée des autres cellules, composants et/ou environnement qui l'accompagnent naturellement. En variante, la matrice contient des cellules procaryotes telles que des bactéries. Par exemple, la matrice polymère est réticulée et comprend une cellule isolée encapsulée dans la matrice polymère réticulée. Un exemple de matrice polymère comprend un polymère synthétique tel qu'un polymère réticulé de manière covalente. Des exemples de matrices polymères comprennent le poly(lactide-coglycolide) (PLGA ; un polymère copolyacide lactique/acide glycolique), le poly(acide acrylique), le polyéthylèneglycol (PEG), le poly(alcool vinylique) ou le polyphosphazène. Le porogène sacrificiel comprend un polymère ioniquement réticulé,Des exemples de polymères pour un porogène comprennent l'alginate, le collagène, la gélatine, la fibrine, l'agarose, l'acide hyaluronique ou le chitosane ainsi qu'un polymère thermosensible tel que l'agarose, la gélatine ou le collagène , le poly(N-isopropylacrylamide), le poly(N-éthylacrylamide), le poly (N- cyclopropyméthacrylamide), poly(N-méthyl-N-éthylacrylamide), poly(N- acryloylpyrrolidine) , poly(N-éthylméthacrylamide) , poly(N-cyclopropylacrylamide) , poly(N-cyclopropylacrylamide), poly (N,N-diéthylacrylamide), poly(N- isopropylacrylamide) , poly(N- inylcaprolactame) , poly(Nn-propylméthacrylamide) , poly(N-méthyl-N-isopropylacrylamide), poly(Nn-propylacrylamide) lamide), le poly(N-méthyl-Nn-propyl lacrylamide) et la poly(N-acryloylpipéridine).
L'hydrogel (également appelé aquagel) est un réseau de chaînes polymères hydrophiles et se présente parfois sous la forme d'un gel colloïdal dans lequel l'eau est le milieu de dispersion.
Les hydrogels sont des polymères naturels ou synthétiques très absorbants (ils peuvent contenir plus de 99% d'eau). Les hydrogels possèdent également un degré de flexibilité très similaire aux tissus naturels, en raison de leur importante teneur en eau. L'hydrogel en forme d'opale inversée présente des taux de gonflement beaucoup plus élevés, et sa cinétique de gonflement est également d'un ordre de grandeur plus rapide. Les échafaudages d'ingénierie (c'est-à-dire les hydrogels d'opale inverse) décrits ici possèdent des propriétés mécaniques et optiques souhaitables qui peuvent faciliter la régénération tissulaire tout en permettant une surveillance optique continue à haute résolution de la prolifération cellulaire et de l'interaction cellule-cellule dans l'échafaudage.
Des procédés de production d'un hydrogel d'opale inverse avec des pores ouverts et interconnectés sont mis en œuvre en comprimant une pluralité de particules de porogènes modèles dans un moule, puis en ajoutant une composition comprenant une solution de polymère et une pluralité de cellules à l'espace interstitiel entre les particules de porogènes modèles dans le moule pour polymériser les particules porogènes matrices. Les particules de porogène matrice sont retirées du moule, produisant ainsi un hydrogel d'opale inverse avec des pores ouverts et interconnectés, dans lequel les cellules sont encapsulées dans l'hydrogel d'opale inverse.Les particules porogènes matrices sont éliminées sans utiliser de solvants organiques toxiques ni de lyophilisation. Par exemple, les billes d'hydrogel thermosensibles sont éliminées en contrôlant la température pour changer la phase solide des billes. La particule porogène matrice est un polymère ioniquement réticulé, un polymère thermosensible, un polymère thermosensible, un polymère sensible au pH ou un polymère photoclivable.
Par exemple, le polymère ioniquement réticulé est l'alginate. Le polymère réticulé ioniquement est éliminé en ajoutant un agent chélatant les métaux choisi dans le groupe constitué par l'acide citrique, l'éthylènediamine, l'acide éthylènediaminetétraacétique (EDTA), l'acide diéthylènetriaminepentaacétique (DTP A) et la N,N-bis(carboxyméthyl)glycine (NTA) .
Des polymères thermosensibles appropriés comprennent l'agarose, la gélatine et le collagène. Le polymère thermosensible est éliminé en augmentant la température du polymère, modifiant ainsi la phase du polymère en phase liquide. Des exemples de polymères photoclivables comprennent des agents de réticulation à base de chromophores pour hydrogels photodégradables, (4-vinylpyridine) (P4VP) et poly (méthacrylate de méthyle). Des procédés de production d'un hydrogel d'opale inverse avec des pores ouverts et interconnectés sont mis en œuvre en comprimant une pluralité de particules de porogènes modèles dans un moule, en ajoutant une composition comprenant une solution de polymère et un agent à l'espace interstitiel entre les particules de porogènes modèles dans le moule pour polymériser les particules porogènes matrices, et éliminer les particules porogènes matrices, produisant ainsi un hydrogel d'opale inverse avec des pores ouverts interconnectés. JL'agent est choisi dans le groupe consistant en un médicament, une nanoparticule (par exemple, des nanoparticules magnétiques ou des nanoparticules d'or) , un facteur de croissance (par exemple, le facteur de croissance endothélial vasculaire (VEGF), le facteur de croissance dérivé des plaquettes (PDGF), le facteur neurotrophique dérivé du cerveau (BDNF), facteur de croissance épidermique (EGF) ou facteur de croissance des fibroblastes (FGF)), une cytokine (p. ex., interféron gamma (IFN-γ), érythropoïétine (EPO), thrombopoïétine (TPO), interleukine-1 (IL-1 ), IL-4), une chimiokine (p. ex., une chimiokine CC, une chimiokine CXC, une chimiokine C ou une chimiokine CX3C), une hormone (p. ex., insuline, hormone de croissance, vasopressine, testostérone ou cortisol), une protéine , un acide nucléique ou une petite molécule. Dans un exemple, des nanoparticules sont encapsulées dans la matrice d'hydrogel et des cellules sont dispersées dans les pores ouverts interconnectés.
Exemple 1 : billes d'alginate comme modèle sacrificiel
L'invention concerne un exemple de la fabrication d'un hydrogel d'opale inverse respectueux des cellules. Des billes d'alginate, formées à l'aide d'une réticulation au Ca2+ ont été utilisées comme porogène, et une solution d'EDTA 50 mM, un agent chélatant les métaux, a été utilisée comme solution d'élimination de la matrice. Pour évaluer si l'EDTA peut dissoudre efficacement les billes d'alginate, trois billes d'alginate de tailles différentes ont été préparées en utilisant une solution d'alginate à 2 % dans une solution de Ca2+ 100 mM (figure 3, rangée supérieure). L'albumine de sérum bovin marquée à la rhodamine (BSA) a été encapsulée dans des billes d'alginate pour visualiser les billes et leur dissolution. Les billes d'alginate résultantes ont été incubées dans une solution d'EDTA 50 mM sous agitation. Après 20 min, toutes les perles d'alginate se sont dissoutes dans une solution d'EDTA et ont perdu leur morphologie sphérique, ce qui a donné une solution rose en raison de la BSA marquée à la rhodamine libérée des perles d'alginate (figure 3, rangée inférieure). Cela démontre que les billes d'alginate ont été utilisées comme matrice sacrificielle en utilisant l'EDTA comme solution de lixiviation.
La figure 3 est une série de photomicrographies démontrant que l'acide éthylènediaminetétraacétique (EDTA) dissout efficacement les billes d'alginate dans les IOH.
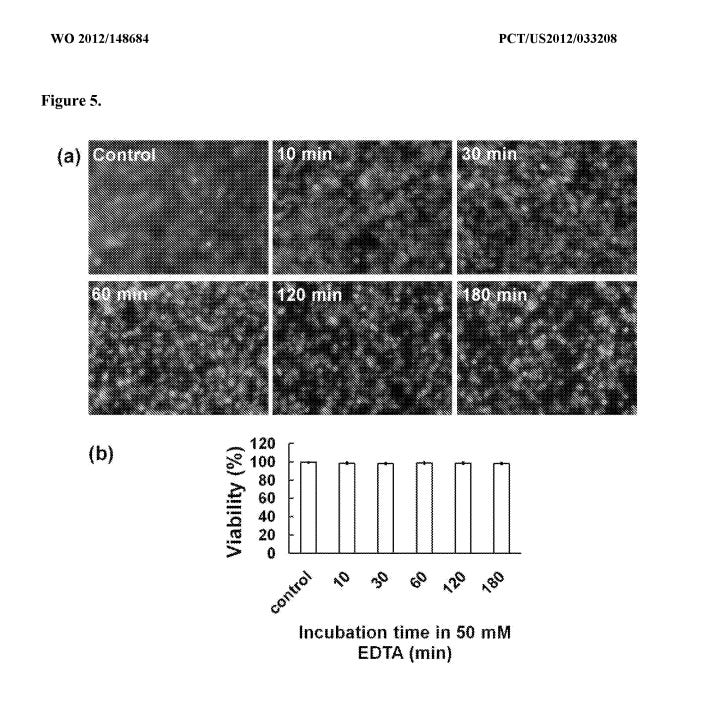
La figure 5a est une série de photomicrographies montrant la viabilité cellulaire après traitement avec de l'EDTA pendant 3 heures. La figure 5b est un histogramme montrant une viabilité d'environ 98 % des cellules après 3 heures d'incubation dans l'EDTA.
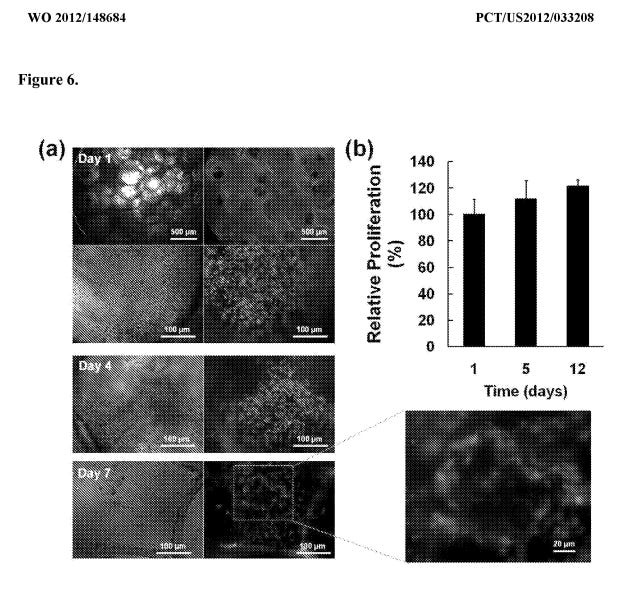
La figure 6a est une série de photomicrographies montrant la viabilité cellulaire après traitement avec de l'EDTA pendant 7 jours. La figure 6b est un diagramme à barres démontrant la prolifération de cellules encapsulées dans des IOH.
Exemple 3 : L'EDTA est non toxique pour les cellules encapsulées dans des IOH
Pour évaluer si l'incubation dans une solution d'EDTA est toxique pour les cellules, la viabilité cellulaire a été vérifiée après incubation dans une solution d'EDTA 50 mM. Des cellules souches mésenchymateuses de souris (CSM) ont été cultivées dans un flacon et incubées dans une solution d'EDTA 50 mM pendant 10, 30, 60, 120 ou 180 min. Par la suite, la viabilité des cellules a été mesurée avec un test de cellules vivantes/mortes en utilisant de la calcéine AM et de l'éthidium homodimère-1. Bien que la morphologie cellulaire ait changé en une forme ronde, les images fluorescentes représentatives de l'essai vivant/mort ont montré qu'il n'y avait pas de toxicité significative de la solution EDTA pour les cellules jusqu'à 3 h d'incubation (figure 5a). L'analyse quantitative a également montré une viabilité de -98 % même après 3 h d'incubation dans une solution EDTA (figure 5b).Sur la base de ces observations, l'incubation des gels dans une solution d'EDTA 50 mM pendant 3 h pour éliminer les billes d'alginate a été déterminée comme un processus non toxique pour les cellules encapsulées dans des IOH.
Les perles d'hydrogel réticulées ioniquement (par exemple, l'alginate) sont éliminées à l'aide de divers agents chélateurs de métaux, notamment l'acide citrique, l'éthylènediamine, l'acide éthylènediammetétraacétique (EDTA), l'acide diéthylènetriaminepentaacétique (DTP A), la N,N-bis(carboxyméthyl)glycine (NTA), etc. Les agents chélateurs se lient aux ions métalliques utilisés comme agent de réticulation des billes de gabarit, ce qui entraîne la génération de pores via la dissociation des ions métalliques et des polymères formant des billes.
Par exemple, divers médicaments chimiques, y compris de petites molécules et des protéines fonctionnelles (facteurs de croissance, cytokines, chimiokines, hormones, etc.) sont mélangés avec la solution de précurseur de polymère à ajouter dans les billes de matrice dans le moule. Après polymérisation des précurseurs polymères et élimination des billes matrices, les molécules encapsulées sont libérées lentement. Les profils de libération dépendent de la densité de réticulation, de l'affinité des molécules avec la chaîne polymère, de la taille des molécules, etc. Dans ce contexte, les hydrogels d'opale inverse sont utilisés comme systèmes de délivrance pour les cellules encapsulées dans l'hydrogel ou les cellules hors de l'hydrogel. .
Les procédés décrits ici encapsulent également des nanoparticules fonctionnelles pour actionner les systèmes d'hydrogel poreux afin de libérer des cellules, des médicaments, des protéines et des facteurs de croissance à la demande. Les nanoparticules sont encapsulées dans l'hydrogel de la même manière que les cellules et les médicaments sont encapsulés. Plus précisément, les nanoparticules fonctionnelles sont mélangées avec des précurseurs de polymères et ajoutées dans les billes de modèle dans le moule. Par exemple, des nanoparticules magnétiques ou des nanoparticules d'or sont encapsulées dans la matrice polymère et les hydrogels poreux résultants sont sensibles à un champ magnétique externe ou à la lumière, respectivement.Les molécules invitées sont libérées lors de la détection du stimulus externe. Dans le cas des nanoparticules magnétiques, la force magnétique externe module le volume des pores dans l'hydrogel d'opale inverse en raison de sa grande porosité. Les molécules invitées encapsulées ou ensemencées dans les hydrogels d'opale inverse sont libérées par les forces mécaniques via la convection. De plus, les nanoparticules magnétiques et les nanoparticules d'or sont utilisées comme fractions hyperthermiques. Les nanoparticules magnétiques et les nanoparticules d'or génèrent de la chaleur en alternant champs magnétiques et irradiation avec des lasers, respectivement. Ainsi, les nanoparticules magnétiques et d'or permettent le mouvement thermique de la matrice polymère et des molécules invitées encapsulées, ce qui accélère la vitesse de libération des molécules invitées.
Résumé et prochaines étapes :
Ce brevet montre que l'hydrogel peut être dissous avec une chélation EDTA. Les nanoparticules métalliques qui se trouvent dans l'hydrogel pour modifier ses propriétés magnétiques et réguler la libération de molécules invitées, par exemple des toxines ou d'autres substances, peuvent également être éliminées du corps par l'EDTA. Je soupçonne que les rubans que nous voyons dans l'analyse du sang vivant des personnes injectées au C19 ainsi que dans les injections non injectées via l'excrétion et l'exposition environnementale sont constitués de cet hydrogel qui peut également avoir des nanotubes de carbone sous diverses formes qui lui sont associés ainsi que des nanoparticules métalliques. NOUS DEVONS TESTER LES GROS CAILLOTS TROUVÉS DANS LE DÉCÉDÉ INJECTÉ POUR VOIR S'IL S'AGIT D'HYDROGEL AI COMME LE SUGGÈRE KAREN KINGSTON. Je soupçonne qu'elle a tout à fait raison.
La chélation EDTA devrait être utilisée dans tous les protocoles de traitement des blessures vax et de manière prophylactique pour les personnes injectées et non injectées - pour traiter cette attaque sans précédent de cette arme parasitaire diabolique de l'intelligence artificielle contre l'humanité.
Tous les médecins qui effectuent des analyses de sang vivant doivent examiner les échantillons avant et après pour voir si la dissolution des rubans se produit et combien de traitements il faut pour les éliminer du sang. La répétition systématique de la thérapie de chélation IV par EDTA doit être effectuée pour empêcher la réaccumulation de cette forme de vie artificielle dans le corps, d'autant plus que l'exposition vient maintenant de littéralement partout.
Si vous n'avez pas encore vu cette brillante interview de Karen Kinston avec Maria Zeee, faites-le dès maintenant :
ARRÊTEZ LES VACCINS. ARRÊTEZ LA GÉO-INGÉNIERIE. ARRÊTEZ LA 5G. ARRÊTEZ D'EMPOISONNER NOTRE APPROVISIONNEMENT EN NOURRITURE ET EN EAU. ARRÊTEZ D'EMPOISONNER LE CORPS AVEC DE GROSSES TOXINES PHARMA.
Remerciements particuliers à Karen Kingston pour son brillant travail dans la découverte de ces brevets.






Commentaires
Enregistrer un commentaire