Les souris des essais peuvent-elles mieux gérer la toxicité des vaccins ARNm que les humains ?
De : https://palexander.substack.com/p/of-mice-and-covid-mrna-vaccines-and?
Vaccins ARNm , Souris & COVID & virus CHIMÉRIQUES : avons-nous été induits en erreur dans l'interprétation des données ? Avons-nous tort? Il semble que les souris tolèrent mieux les vaccins à ARNm que les humains
Comparées aux humains, les souris C57BL/6 & Balb/c sont très tolérantes aux vaccins à ARN ; Pfizer et la FDA ont peut-être tort de fonder la décision de vaxx bivalent sur les données de 8 souris, même si les souris ont contracté le COVID et que 80% des souris sont mortes
Dire que les résultats chez la souris, et en tant que tels, ne s'appliquent pas vraiment aux humains peut être faux et une hypothèse incorrecte et même si j'ai toujours ressenti cela, cette étude ci-dessous est encore plus intrigante et soulève de nombreux problèmes avec les études actuelles sur les souris que nous avons face à nous et qui nous tort l'estomac (étude du virus chimérique de Boston et étude de rappel bivalent de Pfizer).
Aurions-nous mal interprété les données des souris bivalentes et des chimères de Boston ? Les humains courent-ils un risque beaucoup plus grand et sérieux par rapport aux souris étudiées qui ne se sont pourtant pas bien comportées si l'on en croit les rapports ? L'étude de rappel bivalent et l'étude de la chimère de Boston ont toutes deux échoué et les résultats ont été catastrophiques, de toute façon vous l'avez lu. Mais est-ce encore bien pire ? Avons-nous oublié cette étude qui sera discutée ci-dessous, montrant que les souris tolèrent mieux le vaccin à ARNm que les humains ? Y a-t-il des pépites d'or dans cette étude qui méritent d'être méditées ?
Je dis "pas si vite" à ceux qui rejettent l'étude sur le virus de la chimère de Boston comme n'étant pas pertinente pour les humains et pas grave pour les humains, etc. Je dis que c'est une une interprétation stupide. Lisez ce que le Dr Bridle, le Dr McCullough et moi avons écrit. Nous avons séparé les études et l'étude de Boston est une étude de gain de fonction dangereuse et imprudente et qui peut conduire à une catastrophe. Elle a également fourni un plan à tous les mauvais acteurs pour sortir et construire de telles chimères de coronavirus. C'était même dangereux de faire cette étude.
Retour à cette offre à portée de main :
Posons la question de cette façon : si les souris peuvent tolérer le vaccin à ARNm ( https://www.nature.com/articles/s41590-022-01160-y ) et l'ARNm (et probablement le virus) bien mieux que les humains, alors les résultats peuvent en fait indiquer la dévastation pour les humains du rappel bivalent et du virus chimérique de Boston, au-delà de la faible réaction des souris dans les études. En d'autres termes, si c'est le cas, alors les résultats du rappel bivalent sur 8 souris (où les souris sont tombées malades) utilisés pour approuver l'EUA et la mortalité de 80% des souris due à la chimère de Boston peuvent être terribles et la pointe de l'iceberg. Rien n'est bon à ce sujet et nous lisons peut-être mal les résultats. Les souris n'ont pas bien réussi dans les deux études, NON, mais la terrible performance des souris peut signaler une catastrophe pour les humains.
Est-ce une extrapolation ? Je dis peut-être que non et cela vaut la peine d'y prêter attention comme l'a fait un chercheur vraiment brillant qui mérite d'être félicité. Quelle est la preuve? Une étude fondamentale suggère que les souris peuvent en effet faire face aux effets toxiques des ARNm et des nanoparticules lipidiques et des vaccins à ARNm mieux que les humains. Les études sur les vaccins à ARNm de souris sont-elles sous-optimales et donc trompeuses ?
L'étude Tahtinen & Mellman ( https://www.nature.com/articles/s41590-022-01160-y ) suggère "oui" en effet, que les souris peuvent gérer l'ARNm et le vaccin LNP bien mieux que les humains et ce que cela signifie, c'est que nous pouvons nous tromper dans notre interprétation de :
i) l'étude bivalente de 8 souris (Wuhan et sous-variantes BA.4/BA.5) pour que Pfizer obteniennent de la FDA qu'elle approuve le rappel récent (notez que les souris ont été infectées et très malades et que l'infection a atteint les poumons distaux inférieurs, etc. et les narines) et
ii) l'étude du virus chimérique de Boston (spike omicron et chimère dorsale de Wuhan) où 80 % des souris sont mortes. Bref, dans les deux situations, les résultats peuvent être dévastateurs pour l'homme car les souris ont terriblement réagi et donc on peut extrapoler à l'homme. Nous interprétons peut-être mal les études. Les souris peuvent ne pas convenir lorsqu'il s'agit d'ARNm et de vaccins apparentés comme moyen d'étudier les effets et les décisions existantes peuvent être erronées et incorrectes. Cela peut être catastrophique pour l'homme.
Cette réflexion mérite réflexion et regardons de plus près cette étude de Tahtinen et Mellman et al. publié dans NATURE en 2022. Car cela peut nous dire que l'EUA approuvée par la FDA pour le rappel bivalent peut être entièrement imparfaite et incorrecte (ne comprenant pas vraiment la réponse chez les souris) et que la mortalité de 80% chez les souris due au Boston le virus chimérique peut éclipser une létalité réelle de 100% (effacement) chez l'homme si cette chimère était laissée pour compte. En d'autres termes, aussi mauvais que soient les résultats, cela indique une situation terrible pour les humains. En ce sens que les souris gèrent si bien les vaccins à ARNm et les nanoparticules lipidiques que nous manquons peut-être le message clé et que nous sommes complètement induits en erreur et que le résultat peut être bien plus catastrophique pour les humains.
A première vue (Joomi), on voit que :
«La même dose d'ARNm formulé avec un vaccin lipoplex (liposome cationique) a entraîné des symptômes pseudo-grippaux chez l'homme mais pas chez la souris, malgré la grande différence de taille.
Ce vaccin a induit une libération plus systémique de cytokines inflammatoires chez l'homme que chez la souris.
Ce vaccin a également conduit à moins de libération de cytokines anti-inflammatoires chez l'homme, par rapport aux souris.
LA SOURCE:
IL-1 et IL-1ra sont des régulateurs clés de la réponse inflammatoire aux vaccins à ARN
Déclarations clés :
"Contrairement aux humains, les souris C57BL/6 et Balb/c sont remarquablement tolérantes aux vaccins à ARN et ne présentent qu'une libération systémique limitée de cytokines après l'administration iv d'un vaccin liposomal contenant de l'ARN non modifié (ARN-LPX) 1 , 12 . Même à des doses d'ARN (50 µg) bien tolérées chez la souris, les patients présentent des symptômes pseudo-grippaux transitoires légers à modérés qui limitent l'exploration des doses à une plage étroite et limitent éventuellement les réponses optimales des lymphocytes T 2 , 4 , 5 ”
"Compte tenu des différences de taille évidentes, cela signifie que les doses d'ARN-LPX qui déclenchent de puissantes réponses inflammatoires systémiques chez l'homme sont plus de 1 000 fois plus faibles que chez les souris de laboratoire consanguines 2 "
« Nous avons étudié la capacité des vaccins à ARN formulés avec des lipides à déclencher l'immunité innée. Nous avons découvert le rôle clé de l'IL-1 dans le déclenchement de la libération d'autres cytokines pro-inflammatoires associées au syndrome de libération des cytokines (SRC), l'homme étant nettement plus sensible que la souris.
«Étonnamment, la réactogénicité des vaccins à ARN n'était pas nécessairement due à l'agonisme TLR7/8, car la libération d'IL-1 a été observée en utilisant des vaccins contenant de l'ARN modifié par N1-méthyl-pseudouridine (modARN). Au lieu de cela, les composants lipidiques utilisés pour formuler ces vaccins se sont substitués à l'ARN non modifié pour déclencher la réponse IL-1.
"L'ARN-LPX à haute dose (100 μg) a été bien toléré chez les souris de type sauvage sans aucun effet indésirable détectable."
"Nous avons découvert le rôle clé de l'IL-1 dans le déclenchement de la libération d'autres cytokines pro-inflammatoires associées au syndrome de libération des cytokines (SRC), les humains étant nettement plus sensibles que les souris."
"Contrairement aux humains, les leucocytes murins répondent aux vaccins à ARN en régulant à la hausse l'IL-1ra anti-inflammatoire par rapport à l'IL-1 (principalement l'IL-1α), protégeant les souris des toxicités médiées par les cytokines à des doses de vaccin > 1 000 fois plus élevées."
Figure 3d :
« Pour comparer la libération d'IL-1β à celle d'IL-1ra in vivo, nous avons calculé le facteur d'induction des niveaux de cytokines systémiques chez les souris C57BL/6 et chez les neuf patients atteints de cancer de l'étude de phase 1b, les deux groupes ayant été traités avec des quantités absolues comparables d'ARN-LPX. Comme prévu sur la base des données in vitro, les patients humains traités avec une dose tolérée de 25 μg ont montré une légère augmentation de l'induction de l'IL-1β par rapport à l'IL-1ra, alors que chez la souris, l'IL-1ra a été considérablement induite par rapport à l'IL-1β ( figure 3d ). À noter, plutôt que de normaliser les doses d'ARN-LPX par poids d'animal, les souris ont reçu des quantités absolues identiques d'ARN-LPX en tant que patients humains (25 μg par injection).
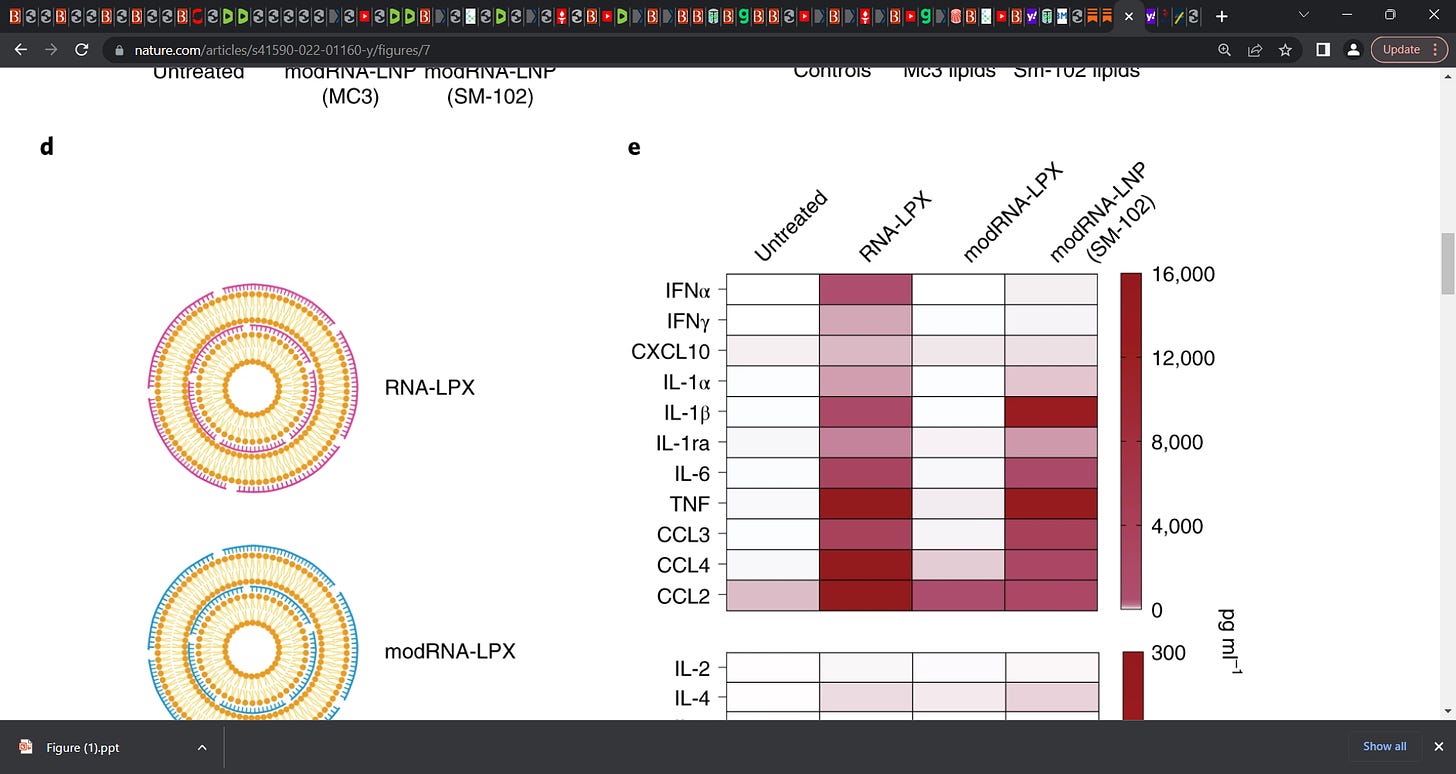
Figure 7e :
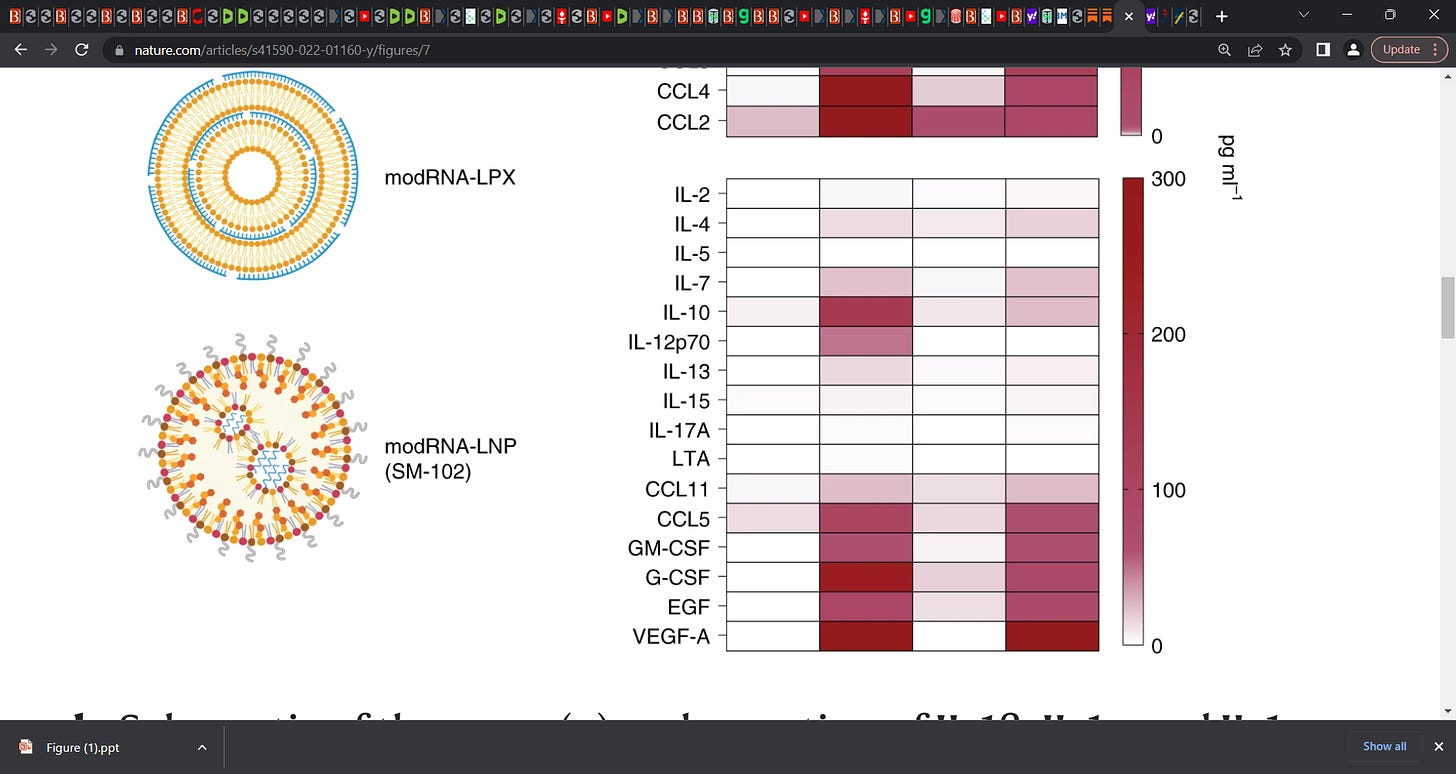
'La libération de cytokines à partir de PBMC traités avec de l'ARN-LPX non modifié, de l'ARN-LPX modifié par N1psU (modARN-LPX) ou du modARN-LNP (formulé avec des lipides SM-102)… L'ARN-LPX non modifié a induit une libération de cytokines robuste, alors que le modARN-LPX n'a pas réussi à induire l'IL-1β ou l'une de ses cytokines en aval (Fig. 7e ). En revanche, une puissante libération de cytokines a été détectée avec le modRNA-LNP (SM-102), entraînant un profil d'induction de cytokines similaire à celui de l'ARN-LPX (Fig. 7e ). Ces résultats suggèrent que la réactogénicité de l'ARN modifié dépend du contexte : l'ARNmod peut être non immunostimulant lorsqu'il est formulé dans des liposomes (LPX), induire une immunostimulation faible lorsqu'il est formulé dans LNP (MC3) ou initier une réponse innée puissante lorsqu'il est formulé dans LNP (SM -102).'
" (Citation de Joomi) Pour certains vaccins à ARNm, l'ARNm et le composant lipidique doivent être présents afin de provoquer la libération de cytokines inflammatoires, alors que dans d'autres, le lipide seul est suffisant. Cela dépend de la formulation lipidique spécifique et si l'ARNm est "modifié".
La modification de l'ARNm, où les uridines sont remplacées par la N1-méthyl-pseudouridine, comme cela a été fait avec les vaccins à ARNm COVID-19, permet à l'ARNm d'échapper à certains récepteurs de type péage dans les cellules, qui sont des protéines qui détectent l'ARN simple brin comme certains types d'ARN viral. Les vaccins à ARNm qui contiennent de l'ARNm non modifié stimuleront ces TLR et feront « penser » aux cellules qu'il y a eu une invasion virale. C'est l'un des signaux qui peuvent contribuer à la libération de cytokines inflammatoires.
L'image ci-dessus (Figure 7 e) montre les niveaux de cytokines avec différents vaccins à ARNm dans les PBMC humains. Partout où vous voyez "mod", cela signifie que l'ARNm a été modifié.
Nous voyons que l'ARNm avec le lipide lipoplex (ARN-LPX) conduit à la libération de beaucoup de cytokines inflammatoires, contrairement à l'ARNm modifié avec ce même lipide (modARN-LPX).
Cela indique que le lipoplex en lui-même ne provoque pas la libération de cytokines inflammatoires, et en effet, lorsqu'ils ont testé uniquement le lipide sans aucun ARNm, cela n'a entraîné la libération d'aucune IL-1β inflammatoire (Fig. 1f).
Je dois donner un énorme crédit à Joomi (et vous soutenez Joomi) pour ce beau reportage et cette bourse car j'ai lu cet article et il est très technique et nécessite une relecture, mais il y a ici d'énormes pépites et découvertes qui soulèvent de nombreuses questions quant à l'interprétation que nous avons faite sur les études sur les souris :
Message clé (Soyons clairs) :
«La même dose d'ARNm formulé avec un vaccin lipoplex (liposome cationique) a entraîné des symptômes pseudo-grippaux chez l'homme mais pas chez la souris, malgré la grande différence de taille.
Ce vaccin a induit une libération plus systémique de cytokines inflammatoires chez l'homme que chez la souris.
Ce vaccin a également entraîné une libération moindre de cytokines anti-inflammatoires chez l'homme, par rapport aux souris.
Ce modèle de cytokine a également été observé lors de la comparaison in vitro de cellules sanguines humaines avec des cellules sanguines de souris.
Le modèle a également été observé dans plusieurs souches différentes de souris de laboratoire.
Le schéma a également été observé dans des cellules de primates non humains in vitro.
La modification de l'ARNm dans le vaccin à ARNm formulé avec le lipoplex n'induit pas de cytokines inflammatoires dans les cellules sanguines humaines.
Les vaccins à ARNm formulés avec des LNP ont induit des cytokines inflammatoires dans les cellules sanguines humaines, malgré la modification de l'ARNm.
Le LNP formulé avec SM-102, qui a été utilisé dans le vaccin à ARNm Moderna COVID-19, était le plus inflammatoire parmi les différentes formulations lipidiques testées.
Le LNP vide de SM-102 était inflammatoire.
Voir la sous-stack de Joomi et soutenir si possible son excellent travail :






Commentaires
Enregistrer un commentaire